Omkostningseffektiv analyse af brug af højfrekvent brystvægoscillation (HFCWO) hos patienter med ikke-cystisk Fibrose Bronchiectasis
Abstrakt
Bronchiectasis er en kronisk progressiv sygdom, der er karakteriseret ved irreversibel patologisk udvidelse af lungebronchi. Behandlinger for bronchiectasis sigter mod at mobilisere luftvejssekretioner, reducere betændelse, forhindre luftvejsinfektioner, forbedre ventilation, minimere antallet af forværringer og forbedre en persons livskvalitet. Højfrekvent brystvægssvingning (HFCWO) er en luftvejsbehandling, der i øjeblikket anvendes til et antal kroniske luftveje, der kompromitterer sygdomme, herunder ikke-cystisk fibrose bronchiectasis. Denne undersøgelse evaluerede den økonomiske indvirkning af HFCWO-behandling leveret af SmartVest® Airway Clearance System på bronchiectasis-relateret sundhedsudnyttelse og omkostninger.
Metoder
Resultaterne af et tidligere offentliggjort resultat af sagsanmeldelse -baseret klinisk undersøgelse foretaget af forfatterne danner grundlaget for denne omkostningseffektivitetsanalyse. Bronchiectasis-relaterede eksacerbationer inklusive antal indlæggelser, akutafdeling (ED) besøg og hyppighed af antibiotikarecepter blev registreret for hver patient i et års periode før SmartVest-brug (standard for plejekontrol) og i et års periode efter start af SmartVest brug. Forværringsfrekvensen for et år før SmartVest og et år efter SmartVest blev sammenlignet. Forværringer blev verificeret fra både patientens medicinske journaler og via telefoninterview. Antibiotiske omkostninger blev bestemt ved hjælp af “on-line rabat på apotekspriser”, mens hospitalsindlæggelse og ED-omkostninger blev bestemt ved hjælp af Healthcare Cost and Utilization Project (HCUP) Statistical Brief # 146 og HCUP National Inpatient Sample (NIS) 2013-databasen.
Resultater
De tidligere offentliggjorte kliniske resultater fra 59 SmartVest-patienter med ikke-cystisk fibrose bronchiectasis tjente som basis for denne analyse. Når resultatdata blev analyseret, anvendte SmartVest sammenlignet med standarden af plejekontrol var forbundet med statistisk signifikante resultater; et fald på 58% i antibiotikaomkostninger, et 63% fald i ED besøgsomkostninger og et 60% fald i hospitalsindlæggelsesomkostninger. I alt resulterede omkostningsanalysen i en årlig besparelse på $ 3.045 pr. patient pr. år med SmartVest-brug.
Konklusioner
Den kliniske effektivitet ved at bruge SmartVest som behandling for ikke-cystisk fibrose bronchiectasis-patienter blev tidligere verificeret af en signifikant reduktio n i bronchiectasis-relaterede eksacerbationer, hvilket direkte oversættes til en signifikant 60% samlet reduktion i sundhedsudnyttelse og omkostninger i denne befolkning. Desuden kan sekundære fordele såsom potentialet til at reducere genoptagelse på hospitalet og potentialet for indvirkning på at afskrække antibiotikaresistens have endnu større fordele end faldende omkostninger.
Søgeord
SmartVest, højfrekvent brystkasse vægoscillation, HFCWO, bronchiectasis, omkostninger
Introduktion
Bronchiectasis er en kronisk og etiologisk heterogen sygdom. Almindelige kendetegn ved bronchiectasis er åndenød, hyppige forværringer, kronisk hoste, hæmoptyse og overdreven sputumproduktion. Sygdommen er typisk karakteriseret ved cyklusser med nedsat slimhindeclearance, bronchial infektion og betændelse, der resulterer i strukturelle skader på luftvejene med permanent og unormal dilatation.1 Bronchiectasis kan være resultatet af en række forskellige respiratoriske og systemiske sygdomme, herunder cystisk fibrose, dyskinetiske ciliære syndromer, inhalations- / aspirationsskader, primære og erhvervede immundefekttilstande og et antal reumatiske og inflammatoriske tilstande.2 Bronchiectasis observeres hos 7% til 52% af patienter med astma eller kronisk obstruktiv lungesygdom (KOL) .3,4 , 37
Seitz, et al., Analyserede en 5% prøve af Medicare ambulant skadedatabase for bronchiectasis blandt modtagere i alderen ≥ 65 år fra 2000 til 2007.6 Databasen indeholder kravsinformation fra ikke-institutionel ambulant sundhedspleje udbydere. Bronchiectasis blev identificeret ved hjælp af den internationale klassifikation af sygdomme, niende revision, ICD-9-CM-koder. Undersøgelsespopulationen omfattede > 2 millioner unikke individer indskrevet i Medicare del B i mindst en måned fra 2000 til 2007. Undersøgelsen fastslog, at forekomsten af bronchiectasis i den samlede befolkning var 1.106 tilfælde pr. 100.000 mennesker over den otte-årige gennemgangsperiode. Undersøgelsen viste også, at forekomsten af bronchiectasis hos Medicare-modtagere steg med 8,7% mellem 2000 og 2007, og hospitaliseringsgraden for bronchiectasis steg årligt med en hastighed på 2.4% blandt mænd og 3,0% blandt kvinder.
Den samlede byrde ved avanceret lungesygdom stiger, og hvor der findes data, synes omkostningerne i forbindelse med sygdommen og dødeligheden af disse sygdomme betydelige.2 Dette kan, delvist være en afspejling af den stigende aldrende befolkning med kronisk lungesygdom, der har en uforholdsmæssig stigning i sundhedsomkostningerne; indlæggelsesgraden på grund af kronisk lungesygdom stiger markant over 50 års alderen, og især hos ældre kvinder.2,7 Ved hjælp af udskrivningsregistreringer fra 1997-2010 blev det anslået, at den gennemsnitlige hospitalsomkostning for indlæggelse hos patienter med en Forværring af lungebetændelse var $ 9.300,28 I 2001 blev det også anslået, at de årlige medicinske omkostninger ved pleje af personer i USA med bronchiectasis var $ 13.244, hvilket er større end de årlige omkostninger for mange andre kroniske sygdomme, såsom hjertesygdomme ($ 12.000) og KOL ($ 11.000) .38 En undersøgelse fra 2005 viste, at patienter med ikke-cystisk fibrose bronchiectasis gennemsnitligt havde 2,0 ekstra dage om året på hospitalet, havde 6,1 ekstra ambulante møder og 27,2 dage mere antibiotikabehandling sammenlignet med patienter uden sygdommen.9 I 2005 var behandlingsomkostningerne for ikke-cystisk fibrose bronchiectasis $ 630 millioner årligt.5
Patienter med ikke-cystisk fibrose bronchiectasis kan have svært ved at rydde luft ay sekreter og kan i væsentlig grad drage fordel af luftvejs clearance-terapi.2 Formålet med behandling for bronchiectasis er at mobilisere luftvejssekretioner for at reducere inflammation, forhindre luftvejsinfektioner, øge ventilation, minimere antallet af forværringer og forbedre patientens livskvalitet. 10-12 En række terapeutiske metoder anvendes i øjeblikket til at rense luftvejssekretioner hos patienter med lungesygdom, nedsat luftvejsslimhæmning eller som er i risiko for at udvikle en af disse tilstande.8 Disse metoder sigter generelt mod at fremme sekretionsclearance ved at reducere slimviskositet og anvendelse af forskydningskræfter for at frigøre slim fra lungevæggen for at lette mobilisering for at lette ekspektorering. Omsorgsstandard involverer kombinationsbehandling med mucolytiske og mucokinetiske midler, bronkodilatatorer, antiinflammatorisk terapi og en eller anden form for fysisk / mekanisk luftvejsrensningsbehandling.2 Luftvejsrensningsbehandling spiller en kritisk rolle, da det hjælper med at undgå fastholdelse af patogenbelastet slim, som er den underliggende oprindelse af tilbagevendende infektion, der forårsager progressiv lungeforringelse.2,13,14 Luftvejsfrigørelsesmetoder spiller en kritisk rolle i opretholdelse af åndedrætssundhed gennem hele patientens levetid. metoder er tilgængelige, herunder brystfysioterapi, positive end-ekspiratoriske trykmasker, orale højfrekvente enheder og højfrekvente brystvægssvingninger (HFCWO) .2 Positive end-ekspiratoriske trykmasker og orale højfrekvente enheder kræver aktiv indsats, beherskelse af teknik og / eller fysisk smidighed, der kan begrænse deres anvendelse.2
HFCWO bruges til luftvejsgodkendelse hos patienter med en bred vifte af luftvejskompromis ng sygdomme og tilstande, herunder genetiske og immunologiske lidelser, neuromuskulære sygdomme og obstruktive lungesygdomme, såsom astma og KOL.15-18 I modsætning til nogle andre metoder kræver HFCWO minimal aktivitet fra brugeren og er ikke afhængig af en sundhedsudbyder teknik for at være effektiv.2 Kliniske undersøgelser, primært hos patienter med cystisk fibrose, har vist, at HFCWO er sikker og effektiv.2,15,19-22 HFCWO leverer kompressionsimpulser til brystvæggen gennem en oppustelig vest forbundet til en luftimpulsgenerator .2 Generatoren producerer en skiftevis strøm af luft ind i og ud af vesten, der hurtigt komprimerer og frigiver brystvæggen inden for en række valgbare frekvenser og tryk. Den oscillerende kompression, der tilføres brystvæggen, er blevet rapporteret at tynde tyktflydende slim, afbryde slim fra lungens væg og fremdrive slim fra de mindre luftveje i lungerne mod de største luftveje, hvor det kan ekspektoreres eller suges væk.2,23, 24 HFCWO kan føre til signifikant forbedring i lungevolumen på 15 til 57 ml og i flow op til 1,6 liter / sek.22
En tidligere case review-undersøgelse evaluerede de kliniske resultater af SmartVest® Airway Clearance System-terapi ved forværring -relateret sundhedsudnyttelse og medicinbrug hos forsøgspersoner med ikke-cystisk fibrose bronchiectasis.25 Undersøgelsen viste, at brugen af SmartVest resulterede i en statistisk signifikant reduktion på 60% i bronchiectasis-relaterede forværringer inklusive brug af antibiotika, akutafdeling (ED) og hospitalsindlæggelser . Den nuværende undersøgelse er designet til at vurdere den økonomiske virkning af SmartVest-terapi på bronchiectasis-relaterede sundheds- og antibiotikakostnader.
Metoder
En nylig SmartVest (Electromed, Inc., New Prague, MN , USA) casebedømmelse resultatbaseret klinisk undersøgelse tjente som grundlag for denne analyse.25 Undersøgelsen registrerede alle bronchiectasis-relaterede eksacerbationer for at omfatte antallet af indlæggelser, ED-besøg og antibiotikabrug i et års periode før SmartVest-brug (standard for plejekontrol) og til sammenligning i et års periode efter starten af SmartVest-brug (behandling). Undersøgelsen omfattede kun de forsøgspersoner med en diagnose af ikke-cystisk fibrose bronchiectasis, som havde brugt SmartVest i mindst et år, og hvis medicinske optegnelser var tilgængelige i et år inden påbegyndelse af SmartVest-terapi. Patienter blev udelukket, hvis de ikke havde overholdt deres ordinerede SmartVest-terapiregime, ikke var i stand til at blive kontaktet via telefon eller var udløbet. Alle data, der blev indsamlet før SmartVest-brug, blev registreret via patientens medicinske journaler.
Patientens medicinske journaler blev gennemgået for alle bronchiectasis-relaterede forværringer, der opstod i løbet af et års periode inden SmartVest-terapien startede. Emner blev kontaktet og interviewet telefonisk for at indsamle bronchiectasis-relaterede forværringer i et års periode efter påbegyndelse af SmartVest-terapi. Spørgeskemaet til telefonundersøgelsen blev udviklet til det eksklusive formål med undersøgelsen. Under telefoninterviewet blev emnet stillet specifikke spørgsmål vedrørende respiratorisk relateret antibiotikabrug, ED-besøg og indlæggelser. Interviewet spurgte også, om patienten brugte SmartVest i henhold til lægens receptregime.
Antibiotiske omkostninger blev bestemt ved hjælp af “on-line rabat på apotekspriser”, men omkostningerne til kontorbesøg og lægeafgifter var ikke inkluderet. Hospitaliserings- og ED-omkostninger blev bestemt ved hjælp af de vægtede nationale skøn fra Healthcare Cost and Utilization Project (HCUP) National Inpatient Sample (NIS), 2013, Agency for Healthcare Research and Quality (AHRQ), baseret på data indsamlet af de enkelte stater og leveret til AHRQ fra staterne. 26 NIS-databasen inkluderer en stratificeret sandsynlighedsprøve af hospitaler fra statslige indlæggelsesdatabaser, der inkluderer hospitalsindlæggelser af patienter med Medicare, Medicaid, privat forsikring og uforsikrede.27 NIS indeholder data fra 5 til 8 millioner hospitalsophold fra ca. 1000 hospitaler. Det er udpeget til at tilnærme en prøve på 20% af de amerikanske ikke-føderale, kortvarige hospitaler som defineret af American Medical Associ ation. NIS er hentet fra stater, der deltager i Healthcare Cost and Utilization Project. NIS indeholder ensartede data om indlæggelse fra sygehusudskrivningsdatabaser, der vedligeholdes af statslige agenturer, hospitalssammenslutninger og andre private organisationer. Samlet antal vægtede udledninger i USA baseret på HCUP NIS var 35.597.792,28
Resultater
Gennemgang af HCUP- og Medicare-databaser afslørede tilknyttede sundhedsomkostninger for en bronchiektaserelateret forværring
at være $ 450 (2012) for et ED-besøg og $ 9.300 (2010) for en indlæggelse med lungebetændelse. Forlænget hospitalsophold baseret på komplikationer eller comorbiditeter blev ikke beregnet. Ved hjælp af online-beregninger af prisfastsættelser af apoteker var omkostningerne ved et standard antibiotikakur for lungebetændelse $ 290 (2016). Lægeudgifter for et kontorbesøg og efterfølgende recept var ikke tilgængelige til beregning.
Af de 104 identificerede SmartVest-patienter med bronkiektasi opfyldte ni og halvtreds patienter inklusion / eksklusionskriterierne.25 I undersøgelsespopulationen var det gennemsnitlige antal af antibiotikarecepter pr. år var 58% mindre for SmartVest (0,6 / år) sammenlignet med standardplejekontrol (1,4 / år) (se tabel 1). SmartVest-brug reducerede også signifikant ED-besøg med 63% (0,08 / år vers 0,03 / år) og indlæggelser med 60% (0,5 / år vers 0,2 / år). De årlige omkostninger pr. Patient til antibiotika for patienter behandlet med SmartVest var ca. $ 233 lavere sammenlignet med dem, der blev behandlet med standardpleje (se tabel 1). Indlæggelser efter et års brug af SmartVest blev også reduceret betydeligt med $ 2.790 pr. Patient pr. År. I alt afslørede de samlede resultater en årlig besparelse på $ 3.045 pr. Patient pr. År ved brug af SmartVest.
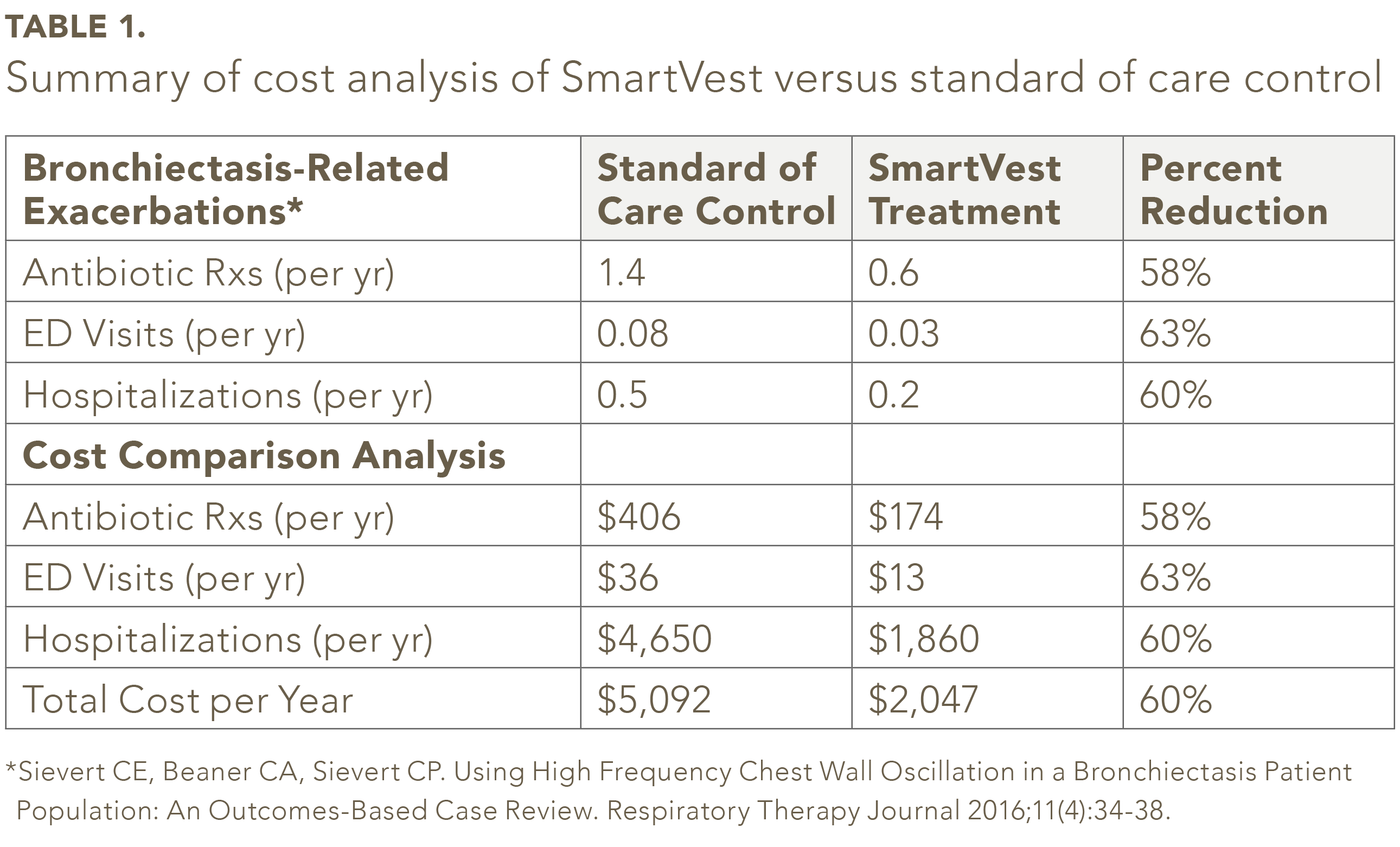
Analysen gjorde ikke redegøre for eventuelle lægeafgifter, der er afholdt for at få en antibiotikarecept uden indlæggelse. Analysen tog heller ikke højde for et kontorbesøg for en potentiel forværring, der ikke resulterede i recept eller indlæggelse. Derudover tog analysen ikke højde for ekstra udgifter, hvis forværringen var en antibiotikaresistent bakteriestamme lungebetændelse, der angiveligt kan koste mere end $ 15.000 for hver episode.
Diskussion
Formålet med analysen var at evaluere den økonomiske indvirkning af SmartVest-brug på bronchiectasis-relaterede medicinske omkostninger sammenlignet med en standard for plejekontrol. Så vidt vi ved, er dette den første undersøgelse, der vurderer sundhedsomkostningerne ved behandling af ikke-cystisk fibrose bronchiectasis-patienter med HFCWO.De samlede omkostninger inkluderede omkostningerne ved antibiotika, ED-besøg og hospitalsindlæggelser relateret til forværringer forbundet med ikke-cystisk fibrose bronchiectasis. Undersøgelsen viste en signifikant reduktion i sundhedsudnyttelsen og de dermed forbundne omkostninger, når patienter med bronchiectasis blev behandlet med SmartVest i et år. De samlede omkostninger blev reduceret med 60%, hvilket svarer til en besparelse på $ 3.045 pr. Patient pr. År.
En nylig undersøgelse, der evaluerede hospitalsudskrivninger, genindlæggelser og ED-besøg for KOL eller bronkiektase hos voksne i USA fundet fra 2001 til 2012 steg antallet af udskrivninger på hospitalet med 88.000.31 Undersøgelsen viste også, at ca. 7% af patienterne med KOL eller bronkiektasi blev genindlagt inden for 30 dage med KOL eller bronkiektase som den primære diagnose.31 I modsætning hertil faldt udskrivningshastigheden for andre sygdomme.31 Årsagen til den signifikante stigning i KOL og bronchiectasis hospital- og ED-besøg er ikke klar, da der er observeret et signifikant fald i antallet af rygning. Det kan imidlertid afspejle potentialet under diagnosen af sygdommen og den langsigtede karakter af KOL og bronkiektase i en aldrende befolkning.31
En tidligere case review resultatbaseret undersøgelse rapporterede, at SmartVest-brug reducerede hospitalsindlæggelser med 1,5 gange, 25 angiver omkostningsfordelen ved HFCWO ved at reducere sundhedsudnyttelsesbyrden. Andre undersøgelser har også vurderet faktorer (både system og patient), der kan nedsætte tilbagetagelse hos patienter med KOL, og som i det mindste delvist er relevante for patienter med bronkiektasi. Disse faktorer inkluderer kontinuitet med patientens primære pleje eller pulmonolog, udskrivningskoordinatorintervention og omfanget eller typen af respiratorisk terapi.32-34
Reduktion i antallet af bronchiectasis-relaterede eksacerbationer kan også påvirke en patientens livskvalitet.35,36 I en population af patienter med KOL var brugen af SmartVest forbundet med signifikant forbedring i fem-symptom-score P = 0,002 (vurdering af sputum, hvæsen, hoste, åndenød og træningstolerance ) .36 SmartVest-behandling viste også en signifikant forbedring i St. George’s Respiratory Questionnaire (SGRQ) P = 0,02, mens der ikke blev observeret nogen forbedring hos patienter behandlet med konventionel behandling.36 Ligeledes viste vores tidligere case review resultatbaseret undersøgelse, at 68 % af forsøgspersonerne angav under telefonopkaldssamtalen, at brugen af SmartVest havde forbedret deres livskvalitet markant.25
Flere begrænsninger i undersøgelsesdesignet bør overvejes rød, når man fortolker resultaterne. Undersøgelsens patientstørrelse var lille, og indlæggelsesdata, ED-besøg og antibiotikabrugsdata efter initiering af SmartVest-terapi blev primært opnået gennem patientinterview. Undersøgelsen kan betragtes som konservativ på grund af, at der ikke lægges nogen omkostninger til lægeudgifter i forbindelse med et kontorbesøg, hvilket resulterer i en antibiotikarecept eller ingen ekstraomkostninger tilføjet til et kontorbesøg, der ikke resulterede i en antibiotikarecept. Derudover kan afhængighed af HCUP-, NIS- og AHRQ-databaser, der afhænger af de diagnoser, der er angivet på krav, være kodet forkert eller slet ikke kodet og derved potentielt indføre målefejl med hensyn til ICD-9-CM-baserede variabler. / p>
Reduktion af udgifter til sundhedsudnyttelse, såsom brug af antibiotika, ED-besøg og indlæggelser, er prioriterede mål for nylige sundhedsdirektiver som f.eks. lov om overkommelig pleje (ACA). F.eks. Har ACA oprettet et reduktionsprogram for hospitaler (HRRP), som har instrueret CMS om at straffe hospitaler ved at reducere godtgørelser for overskydende patientindlæggelser for den samme tilstand. HRRP identificerede oprindeligt de tre øverste “anvendelige betingelser” for målrettet tilbagetagelsesmåling til også at omfatte akut myokardieinfarkt, hjertesvigt og lungebetændelse. Desuden afsluttede CMS for nylig udvidelsen af yderligere anvendelige tilstande, der begyndte med regnskabsåret 2015 til at omfatte patienter, der blev optaget til akut forværring af KOL. Den betydelige reduktion i sundhedsudnyttelse og hospitalsindlæggelse for ikke-cystisk bronkiektasepatienter, der bruger SmartVest, som vist i denne undersøgelse og andre, kan spille en kritisk rolle i at hjælpe hospitaler med at reducere genindlæggelser og dermed ikke straffes.
For patienter, der har luftvejsinfektioner, der er resistente over for orale antibiotika, er byrden meget større og mere alvorlig. Intravenøs antibiotika komplicerer pleje meget, fordi hospitalsindlæggelse eller hjemmeovervågning er påkrævet. Behandling for disse patienter inkluderer placering af et centralt venekateter, koordinering af doserne af lægemidler, der ofte skal gives flere flere gange om dagen, regelmæssige blodprøver for at overvåge bivirkninger og måling af antibiotikumets blodniveauer i mange dage, trin, der bliver dyre og forstyrrer patienters liv.
Verdenssundhedsorganisationen (WHO) har erklæret, at mikrobiel resistens over for antibiotika udgør en “større global trussel med ødelæggende konsekvenser for folkesundheden.” Antimikrobiel resistens truer effektiv forebyggelse og behandling af et stadigt stigende udvalg af infektioner forårsaget af ikke kun bakterier, men også vira og svampe. De amerikanske centre for sygdomsbekæmpelse og forebyggelse (CDC) betragter antimikrobiel resistens som en af deres største bekymringer og prioriteter. Alene i USA bliver mindst 2 millioner mennesker inficeret med bakterier, der er resistente over for antibiotika, og mindst 23.000 mennesker dør hvert år som et direkte resultat af disse infektioner.39 Som svar på den verdensomspændende bekymring, US Centers for Medicare & Medicaid Services (CMS) udgav for nylig en foreslået regelændring i sine deltagelsesbetingelser, som blandt andet ville kræve, at hospitaler gennemfører antibiotikastyringsprogrammer for at kunne deltage i Medicare- og Medicaid-programmerne. Antibiotikastyring inkluderer forbedring af patientresultater ved vedtagelse af processer og procedurer, der reducerer forekomsten af infektioner med pa særlig opmærksomhed på lungebetændelse såsom forebyggende behandling. Som en sekundær fordel for cost-benefit-resultaterne af denne undersøgelse kan en signifikant reduktion i behovet for antibiotika hos bronchiectasis-patienter ved brug af SmartVest have endnu større fordele end faldende omkostninger. En tilgængelig behandling, der signifikant kunne reducere luftvejsinfektioner og dermed behovet for antibiotika, passer godt ind i hospitalets infektionskontrolprogrammer.
Sammenfattende er den kliniske effektivitet af HFCWO-luftvejsclearance påvist af SmartVest hos patienter med KOL 36 og dem bronchiectasis, 25 og den signifikante reduktion i antibiotikum, ED og hospitalsindlæggelsesomkostninger observeret i denne undersøgelse understøtter omkostningsfordelen ved SmartVest-brug og argumenterer for forsikringsdækning af SmartVest af betalere. Derudover kan sekundære fordele såsom potentialet til at reducere genoptagelse på hospitalet og potentialet for indvirkning på at afskrække antibiotikaresistens have endnu større fordele end faldende omkostninger.
Download undersøgelsesteksten
Anerkendelser
Forfatterne vil gerne takke Elizabeth Goodwin PhD for redaktionel støtte.
- King P. Pathogenesis of bronchiectasis. Paediatr Respir Rev 2011; 12 (2): 104-110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Højfrekvent brystkompression: en praktisk terapi til patienter med bronchiectasis. Respiratorisk terapi 2008; 3 (1): 22-26.
- Patel IS, Vlahos I, Wilkinson TM, et al. Bronchiectasis, forværringsindeks og betændelse ved kronisk obstruktiv lungesygdom. Am J Respir Crit Care Med 2004; 170 (4): 400-407. 10.1164 / rccm.200305-648OC
- Gono H, Fujimoto K, Kawakami S, et al. Evaluering af tykkelse af luftvejene og luftfangst ved HRCT ved asymptomatisk astma. Eur Respir J 2003; 22 (6): 965-971.
- Weycker D, Edelsberg J, Oster G, et al. Udbredelse og økonomisk byrde ved bronchiectasis. Klinisk lungemedicin 2005; 12 (4): 205-209.
- Seitz AE, Olivier KN, Adjemian J, et al. Tendenser i bronchiectasis blandt medicare-modtagere i USA, 2000 til 2007. CHEST Journal 2012; 142 (2): 432-439.
- Seitz AE, Olivier KN, Steiner CA, et al. Tendenser og byrder ved bronkiektaseassocierede hospitalsindlæggelser i USA, 1993-2006. Bryst 2010; 138 (4): 944-949. 10.1378 / chest.10-0099
- Seitz AE, Olivier KN, Steiner CA, et al. Tendenser og byrder ved bronkiektaseassocierede hospitalsindlæggelser i USA, 1993-2006. CHEST Journal 2010; 138 (4): 944-949.
- Weycker D, Edelsberg J, Oster G, et al. Udbredelse og økonomisk byrde ved bronchiectasis. Klinisk lungemedicin 2005; 12: 205-209.
- Fibrose. AoCPiC. Standarder for pleje og god klinisk praksis for behandling af fysioterapi ff cystisk fibrose 2011. Tilgængelig fra: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio 11. juni.
- O’Donnell AE. Bronchiectasis. Bryst 2008; 134 (4): 815-823. 10.1378 / chest.08-0776
- Barker AF. Bronchiectasis. N Engl J Med 2002; 346 (18): 1383-1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Ikke-farmakologiske luftvejsbehandlinger: ACCP evidensbaseret klinisk praksis. Bryst 2006; 129 (1 Suppl): 250S-259S. 10.1378 / chest.129.1 suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Behandling af slimhindedysfunktion. Bryst 1996; 110 (4): 1048-1057.
- Arens R, Gozal D, Omlin KJ, et al. Sammenligning af højfrekvent brystkompression og konventionel brystfysioterapi hos indlagte patienter med cystisk fibrose. Am J Respir Crit Care Med 1994; 150 (4): 1154-1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Højfrekvent svingning af luftvejene og brystvæggen. Respir Care 2002; 47 (7): 797-807.
- Hansen LG, Warwick WJ.Højfrekvent brystkompressionssystem for at hjælpe med at fjerne slim fra lungerne. Biomed Instrum Technol 1990; 24 (4): 289-294.
- Lange DJ, Lechtzin N, Davey C, et al. Højfrekvent brystvægssvingning i ALS: et sonderende randomiseret, kontrolleret forsøg. Neurologi 2006; 67 (6): 991-997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. Den langsigtede effekt af højfrekvent brystkompressionsterapi på lungekomplikationer af cystisk fibrose. Pediatr Pulmonol 1991; 11 (3): 265-271.
- Kluft J, Beker L, Castagnino M, et al. En sammenligning af behandlinger med bronchial dræning i cystisk fibrose. Pediatr Pulmonol 1996; 22 (4): 271-274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P
- Scherer TA, Barandun J, Martinez E, et al. Effekt af højfrekvent oral luftvej og brystvægssvingning og konventionel brystfysioterapi på ekspektoration hos patienter med stabil cystisk fibrose. Bryst 1998; 113 (4): 1019-1027.
- Nicolini A, Cardini F, Landucci N, et al. Effektivitet af behandling med højfrekvent svingning i brystvæggen hos patienter med bronchiectasis. BMC Pulm Med 2013; 13: 21. 10.1186 / 1471-2466-13-21
- Osman LP, Roughton M, Hodson ME, et al. Kortvarig komparativ undersøgelse af højfrekvent brystvægssvingning og europæiske luftvejsfrigørelsesteknikker hos patienter med cystisk fibrose. Thorax 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Højfrekvent assisteret luftvejsgodkendelse. Respir Care 2007; 52 (9): 1224-1235; diskussion 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Brug af højfrekvent brystvægoscillation i en bronchiectasis patientpopulation: En resultatorienteret sagsanmeldelse. Respiratory Therapy Journal 2016; 11 (4): 34-38.
- HCUP. Oversigt over den landsdækkende nødafdelingsprøve (NEDS) 2016. Tilgængelig fra: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Oversigt over de nationale (landsdækkende) stationære prøver. Tilgængelig fra: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C. Omkostninger til hospitalsophold i USA, 2010: Statistisk brief # 146. Sundhedsomkostnings- og udnyttelsesprojekt (HCUP) Statistiske briefinger. Rockville (MD): Agency for Healthcare Research and Quality (US); 2006.
- Stein PD, Matta F. Udgifter til akutafdelingsbesøg og hospitalsindlæggelser for pulmonal arteriel hypertension.
J Epidemiol Public Health Rev 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Refusion for behandling af overgangsbehandling for at reducere KOL-tilbagetagelse. Bryst
2014; 145 (1): 149-155. 10.1378 / chest.13-0787 - Ford ES. Hospitaludskrivninger, genindlæggelser og ED-besøg for KOL eller bronkiektasi blandt amerikanske voksne: fund fra den landsdækkende hospitalsprøve 2001-2012 og Nationwide Emergency Department Sample 2006-2011. Bryst 2015; 147 (4): 989-998. 10.1378 / chest.14-2146
- Sharma G, Kuo YF, Freeman JL, et al. Poliklinisk opfølgningsbesøg og 30-dages akutafdelingsbesøg og genoptagelse hos patienter indlagt på grund af kronisk obstruktiv lungesygdom. Arch Intern Med 2010; 170 (18): 1664-1670. 10.1001 / archinternmed.2010.345
- Lainscak M, Kadivec S, Kosnik M, et al. Udskrivningskoordinatorintervention forhindrer indlæggelser hos patienter med KOL: et randomiseret kontrolleret forsøg. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O, Sewell L, Morgan MD, et al. Kort poliklinisk lungerehabiliteringsprogram reducerer genindlæggelse efter indlæggelse på grund af en forværring af kronisk obstruktiv lungesygdom. Respirologi 2013; 18 (7): 1063-1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. Langvarig luftfugtningsterapi er omkostningseffektiv for patienter med moderat eller svær kronisk obstruktiv lungesygdom eller bronkiektase. Værdisundhed 2014; 17 (4): 320-327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. En pilotundersøgelse af virkningen af højfrekvent brystvægssvingning hos patienter med kronisk obstruktiv lungesygdom med slimhypersekretion. Int J Chron Obstruct Pulmon Dis 2011; 6: 693-699. 10.2147 / KOL. S22896.
- Martınez-Garcıa MA, et al. Prognostisk værdi af bronchiectasis hos patienter med moderat til svær kronisk obstruktiv lungesygdom. Am J Respir Crit Care Med 2013; Bind 187, udg. 8, s. 823–831.
- O’Donnell AE. Bronchiectasis. Bryst 2008; 134: 815–82.
- Centers for Disease Control and Prevention – Antibiotic / Antimicrobial Resistance website https://www .cdc.gov / drugresistance /