Análisis rentable del uso de la oscilación de la pared torácica de alta frecuencia (HFCWO) en pacientes no quísticos Fibrosis Bronquiectasia
Resumen
La bronquiectasia es una enfermedad crónica progresiva caracterizada por dilatación patológica irreversible de los bronquios pulmonares. Los tratamientos para la bronquiectasia tienen como objetivo movilizar las secreciones de las vías respiratorias, reducir la inflamación, prevenir las infecciones respiratorias, mejorar la ventilación, minimizar el número de exacerbaciones y mejorar la calidad de vida de una persona. La oscilación de la pared torácica de alta frecuencia (HFCWO) es un tratamiento de limpieza de las vías respiratorias que se utiliza actualmente para una serie de enfermedades crónicas que comprometen las vías respiratorias, incluida la bronquiectasia por fibrosis no quística. Este estudio evaluó el impacto económico del tratamiento con HFCWO administrado por el SmartVest® Airway Clearance System sobre la utilización y el costo de la atención médica relacionada con la bronquiectasia.
Métodos
Los resultados de un resultado de revisión de caso publicado anteriormente El estudio clínico realizado por los autores proporcionó la base para este análisis de rentabilidad. Las exacerbaciones relacionadas con las bronquiectasias, incluido el número de hospitalizaciones, las visitas al servicio de urgencias (SU) y la frecuencia de las prescripciones de antibióticos, se registraron para cada paciente durante un período de un año antes del uso de SmartVest (control estándar de atención) y durante un período de un año después de comenzar SmartVest usar. Se compararon las tasas de exacerbación durante un año antes de SmartVest y un año después de SmartVest. Las exacerbaciones se verificaron tanto a partir de los registros médicos del paciente como por entrevista telefónica. Los costos de los antibióticos se determinaron utilizando «precios de farmacia con descuento en línea», mientras que los costos de hospitalización y servicios de urgencias se determinaron mediante el Resumen estadístico n. ° 146 del Healthcare Cost and Utilization Project (HCUP) y la base de datos HCUP National Inpatient Sample (NIS) 2013.
Resultados
Los resultados clínicos publicados anteriormente de cincuenta y nueve pacientes de SmartVest con bronquiectasias por fibrosis no quística sirvieron como base para este análisis. Cuando se analizaron los datos de resultado, el uso de SmartVest, en comparación con el estándar del control de la atención, se asoció con resultados estadísticamente significativos; una disminución del 58% en el costo de los antibióticos, una disminución del 63% en el costo de la visita al DE y una disminución del 60% en el costo de la hospitalización. En total, el análisis de costos resultó en un ahorro anual de $ 3,045 por paciente por año de uso de SmartVest.
Conclusiones
La eficacia clínica del uso de SmartVest como tratamiento para pacientes con bronquiectasias con fibrosis no quística se verificó previamente mediante una reducción significativa n en las exacerbaciones relacionadas con las bronquiectasias, lo que se traduce directamente en una reducción general significativa del 60% en la utilización y el costo de la atención médica en esta población. Además, los beneficios secundarios, como la posibilidad de reducir los reingresos hospitalarios y el impacto potencial para disuadir la resistencia a los antibióticos, pueden tener beneficios incluso mayores que la reducción de costes.
Palabras clave
SmartVest, cofre de alta frecuencia oscilación de la pared, HFCWO, bronquiectasias, coste
Introducción
La bronquiectasia es una enfermedad crónica y etiológicamente heterogénea. Las características comunes de las bronquiectasias son dificultad para respirar, exacerbaciones frecuentes, tos crónica, hemoptisis y producción excesiva de esputo. La enfermedad se caracteriza típicamente por ciclos de alteración del aclaramiento mucociliar, infección bronquial e inflamación que resulta en daño estructural de las vías respiratorias con dilatación permanente y anormal.1 Las bronquiectasias pueden ser el resultado de una amplia gama de enfermedades respiratorias y sistémicas, incluida la fibrosis quística, síndromes ciliares discinéticos, lesiones por inhalación / aspiración, estados de inmunodeficiencia primaria y adquirida y una serie de afecciones reumáticas e inflamatorias2. Se observa bronquiectasia en el 7% al 52% de los pacientes con asma o enfermedad pulmonar obstructiva crónica (EPOC) .3,4 , 37
Seitz, et al, analizaron una muestra del 5% de la base de datos de reclamaciones de pacientes ambulatorios de Medicare por bronquiectasia entre beneficiarios de ≥65 años de 2000 a 2007.6 La base de datos contiene información a nivel de reclamaciones de atención médica ambulatoria no institucional proveedores. La base de datos identificó las bronquiectasias utilizando los códigos de la Clasificación Internacional de Enfermedades, Novena Revisión, Modificación Clínica (ICD-9-CM). La población del estudio incluyó > 2 millones de personas únicas inscritas en la Parte B de Medicare durante al menos un mes entre 2000 y 2007. El estudio determinó que la prevalencia de bronquiectasias en la población general era de 1.106 casos por 100.000 personas durante el período de revisión de ocho años. El estudio también encontró que la prevalencia de bronquiectasias en los beneficiarios de Medicare aumentó en un 8,7% entre 2000 y 2007 y la tasa de hospitalización por bronquiectasias aumentó anualmente a una tasa de 2.4% entre hombres y 3,0% entre mujeres.
La carga general de enfermedad pulmonar avanzada está aumentando y, cuando existen datos, los costos relacionados con la morbilidad y mortalidad de estas enfermedades parecen ser significativos.2 Esto podría, en parte, ser un reflejo del creciente envejecimiento de la población con enfermedad pulmonar crónica que tiene un aumento desproporcionado de los costos de la atención médica; la tasa de hospitalización por enfermedad pulmonar crónica aumenta notablemente por encima de los 50 años, y particularmente en mujeres mayores.2,7 Utilizando los registros de alta de 1997-2010, se calculó el costo hospitalario promedio para la atención hospitalaria en pacientes con un La exacerbación de la neumonía fue de $ 9,300.28 En 2001, también se estimó que el costo médico anual de la atención para las personas en los Estados Unidos con bronquiectasia fue de $ 13,244, que es mayor que el costo anual de muchas otras enfermedades crónicas, como las enfermedades cardíacas ($ 12,000) y EPOC ($ 11,000) .38 Un estudio de 2005 encontró que los pacientes con bronquiectasias por fibrosis no quística promediaban 2.0 días adicionales por año en el hospital, tenían 6.1 consultas ambulatorias adicionales y 27.2 días más de terapia con antibióticos en comparación con pacientes sin la enfermedad.9 En 2005 , el costo del tratamiento para la bronquiectasia por fibrosis no quística fue de $ 630 millones anuales.5
Los pacientes con bronquiectasia por fibrosis no quística pueden tener dificultades para aclarar el aire. ay secreciones y pueden beneficiarse significativamente de la terapia de limpieza de las vías respiratorias.2 Los objetivos del tratamiento de la bronquiectasia son movilizar las secreciones de las vías respiratorias para reducir la inflamación, prevenir infecciones respiratorias, mejorar la ventilación, minimizar el número de exacerbaciones y mejorar la calidad de vida del paciente. 10-12 Actualmente se utilizan varios métodos terapéuticos para eliminar las secreciones de las vías respiratorias en pacientes con enfermedad pulmonar, alteración del aclaramiento del moco respiratorio o que están en riesgo de desarrollar cualquiera de estas afecciones.8 Estos métodos generalmente tienen como objetivo promover el aclaramiento de las secreciones al reducir viscosidad del moco y uso de fuerzas de cizallamiento para liberar el moco de la pared pulmonar para facilitar la movilización y facilitar la expectoración. El estándar de atención incluye la terapia combinada con agentes mucolíticos y mucocinéticos, broncodilatadores, terapia antiinflamatoria y alguna forma de terapia física / mecánica de depuración de las vías respiratorias.2 La terapia de depuración de las vías respiratorias juega un papel crítico ya que ayuda a evitar la retención de moco cargado de patógenos que es el origen subyacente de la infección recurrente que causa un deterioro pulmonar progresivo.2,13,14 Los métodos de limpieza de las vías respiratorias desempeñan un papel fundamental en el mantenimiento de la salud respiratoria durante toda la vida del paciente.
Varias vías respiratorias Los métodos disponibles incluyen fisioterapia torácica, máscaras de presión espiratoria final positiva, dispositivos orales de alta frecuencia y oscilación de la pared torácica de alta frecuencia (HFCWO) .2 Las máscaras de presión espiratoria final positiva y los dispositivos orales de alta frecuencia requieren un esfuerzo activo, el dominio de técnica y / o agilidad física que puede limitar su uso.2
HFCWO se utiliza para la limpieza de las vías respiratorias en pacientes con una amplia gama de compromisos de las vías respiratorias enfermedades y afecciones, incluidos los trastornos genéticos e inmunológicos, las enfermedades neuromusculares y las afecciones pulmonares obstructivas, como el asma y la EPOC.15-18 A diferencia de algunos otros métodos, el HFCWO requiere una actividad mínima por parte del usuario y no depende de un proveedor de atención médica. técnica para ser eficaz.2 Los estudios clínicos, principalmente en pacientes con fibrosis quística, han demostrado que el HFCWO es seguro y eficaz.2,15,19-22 El HFCWO administra pulsos de compresión a la pared torácica a través de un chaleco inflable conectado a un generador de pulsos de aire .2 El generador produce un flujo alterno de aire que entra y sale del chaleco que comprime y libera rápidamente la pared torácica dentro de una gama de frecuencias y presiones seleccionables. Se ha informado que la compresión oscilatoria impartida a la pared torácica diluye el moco viscoso, desconecta el moco de la pared del pulmón e impulsa el moco de las vías respiratorias menores de los pulmones hacia las vías respiratorias principales donde puede expectorarse o succionarse2,23. 24 HFCWO puede conducir a una mejora significativa en el volumen pulmonar de 15 a 57 ml y en el flujo de hasta 1,6 l / seg.22
Un estudio de revisión de caso anterior evaluó los resultados clínicos de la terapia del Sistema de limpieza de las vías respiratorias SmartVest® en la exacerbación -Uso de la atención médica y el uso de medicamentos relacionados en sujetos con bronquiectasias sin fibrosis quística.25 El estudio encontró que el uso de SmartVest resultó en una reducción estadísticamente significativa del 60% en las exacerbaciones relacionadas con las bronquiectasias, incluido el uso de antibióticos, visitas al departamento de emergencias (SU) y hospitalizaciones . El estudio actual está diseñado para evaluar el impacto económico de la terapia SmartVest en los costos de los antibióticos y la atención médica relacionados con la bronquiectasia.
Métodos
Un SmartVest reciente (Electromed, Inc., New Prague, MN , EE.UU.) estudio clínico basado en resultados de revisión de casos sirvió como base para este análisis.25 El estudio registró todas las exacerbaciones relacionadas con las bronquiectasias para incluir el número de hospitalizaciones, visitas al servicio de urgencias y el uso de antibióticos durante un período de un año antes del uso de SmartVest (control estándar de atención) y, a modo de comparación, durante un período de un año después del inicio del tratamiento. Uso (tratamiento) de SmartVest. El estudio incluyó solo a aquellos sujetos con un diagnóstico de bronquiectasia por fibrosis no quística que habían estado usando SmartVest durante al menos un año y cuyos registros médicos estaban disponibles durante un año antes del inicio de la terapia SmartVest. Los pacientes fueron excluidos si no habían cumplido con su régimen de terapia SmartVest prescrito, no podían ser contactados por teléfono o habían expirado. Todos los datos recopilados antes del uso de SmartVest se capturaron a través de los registros médicos del paciente.
Se revisaron los registros médicos del paciente para detectar todas las exacerbaciones relacionadas con las bronquiectasias que ocurrieron durante un período de un año antes de comenzar la terapia con SmartVest. Los sujetos fueron contactados y entrevistados por teléfono para recopilar las exacerbaciones relacionadas con las bronquiectasias durante el período de un año después de comenzar la terapia con SmartVest. El cuestionario para la encuesta telefónica fue desarrollado con el propósito exclusivo del estudio. Durante la entrevista telefónica, al sujeto se le hicieron preguntas específicas sobre el uso de antibióticos respiratorios, visitas al servicio de urgencias y hospitalizaciones. La entrevista también preguntó si el paciente estaba usando SmartVest de acuerdo con el régimen de prescripción del médico.
Los costos de los antibióticos se determinaron utilizando «precios de farmacia con descuento en línea», sin embargo, el costo de las visitas al consultorio y los honorarios del médico no se incluyeron . Los costos de hospitalización y urgencias se determinaron utilizando las estimaciones nacionales ponderadas de Healthcare Cost and Utilization Project (HCUP) National Inpatient Sample (NIS), 2013, Agency for Healthcare Research and Quality (AHRQ), según los datos recopilados por los estados individuales y proporcionados a AHRQ por los estados.26 La base de datos del NIS incluye una muestra probabilística estratificada de hospitales de las bases de datos estatales de pacientes hospitalizados que incluyen hospitalizaciones de pacientes con Medicare, Medicaid, seguros privados y personas sin seguro.27 El NIS contiene datos de 5 a 8 millones de estadías en hospitales de aproximadamente 1000 hospitales. Está designado para aproximar una muestra del 20% de los hospitales de corto plazo no federales de EE. UU. Según lo define la American Medical Associ ación. El NIS proviene de los estados que participan en el Proyecto de Utilización y Costo de la Atención Médica. El NIS contiene datos uniformes de estadías de pacientes hospitalizados de bases de datos de alta hospitalaria mantenidas por agencias estatales, asociaciones de hospitales y otras organizaciones privadas. El número total de altas ponderadas en los EE. UU. Basado en HCUP NIS fue 35,597,792.28
Resultados
La revisión de las bases de datos de HCUP y Medicare reveló costos de atención médica asociados para una exacerbación relacionada con bronquiectasias. $ 450 (2012) por una visita al DE y $ 9,300 (2010) por una hospitalización con neumonía. No se calcularon las estancias hospitalarias prolongadas basadas en complicaciones o comorbilidades. Utilizando los cálculos de precios de farmacia con descuento en línea, el costo de un régimen de antibióticos estándar para la neumonía fue de $ 290 (2016). Los honorarios del médico para una visita al consultorio y la prescripción posterior no estaban disponibles para el cálculo.
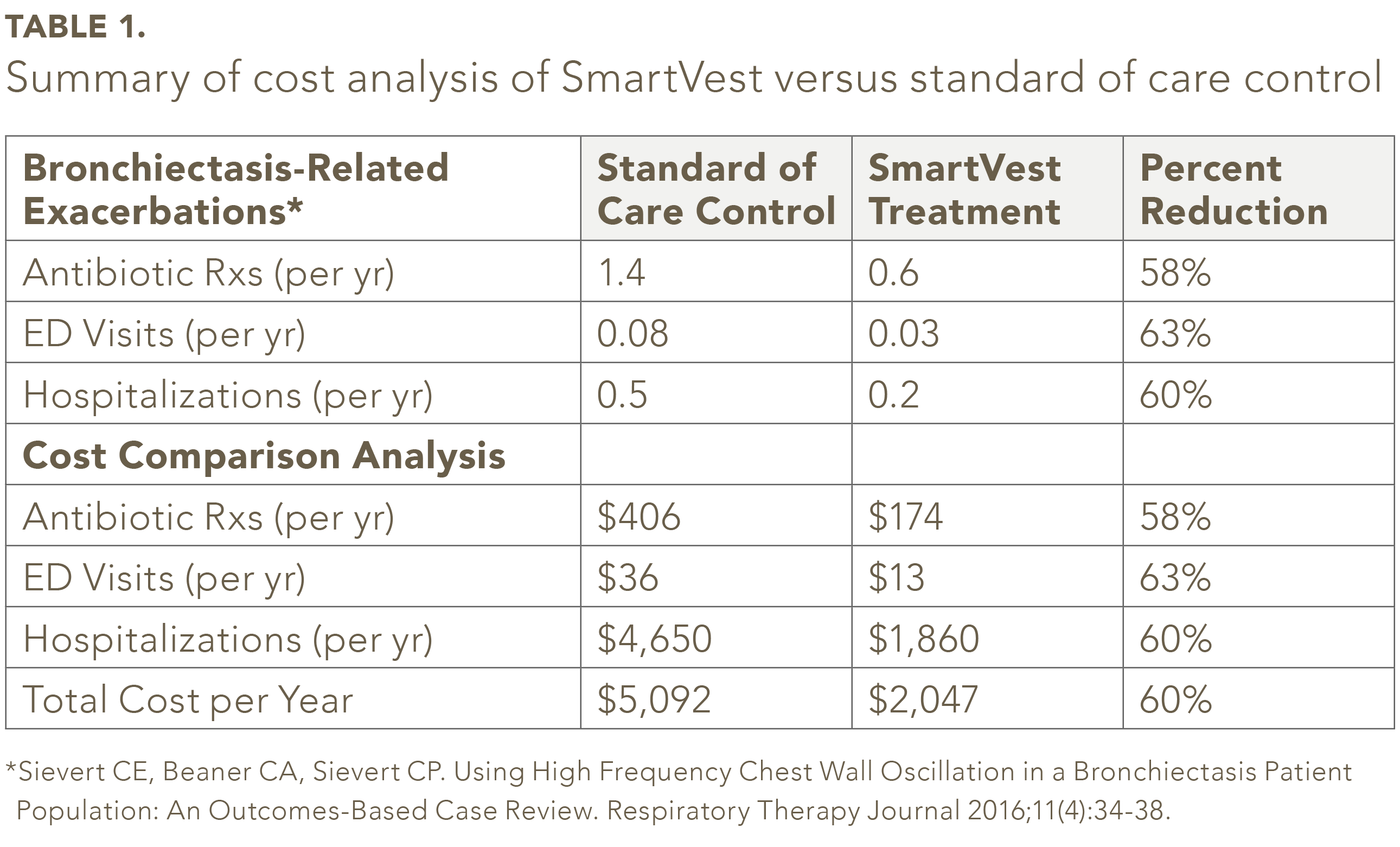
De los 104 pacientes con bronquiectasia SmartVest identificados, cincuenta y nueve pacientes cumplieron los criterios de inclusión / exclusión.25 En la población del estudio, el número promedio de prescripciones de antibióticos por año fue 58% menor para SmartVest (0,6 / año) en comparación con el control estándar de atención (1,4 / año) (ver Tabla 1). El uso de SmartVest también redujo significativamente las visitas al servicio de urgencias en un 63% (0,08 / año frente a 0,03 / año) y las hospitalizaciones en un 60% (0,5 / año frente a 0,2 / año). Los costos anuales por paciente de antibióticos para los pacientes tratados con SmartVest fueron aproximadamente $ 233 más bajos en comparación con los tratados con el estándar de atención (consulte la Tabla 1). Las hospitalizaciones, después de un año de uso de SmartVest, también se redujeron significativamente en $ 2,790 por paciente por año. En total, los resultados generales revelaron un ahorro anual de $ 3,045 por paciente por año de uso de SmartVest.
El análisis no Tenga en cuenta los honorarios del médico / consultorio incurridos para obtener una receta de antibióticos sin hospitalización. Además, el análisis no tuvo en cuenta una visita al consultorio por una posible exacerbación que no resultó en una prescripción u hospitalización. Además, el análisis no tuvo en cuenta los gastos adicionales si la exacerbación fue una neumonía por cepa bacteriana resistente a los antibióticos que, según se informa, puede costar más de $ 15,000 por cada episodio.
Discusión
El propósito de el análisis fue para evaluar el impacto económico del uso de SmartVest en los costos médicos asociados con la bronquiectasia en comparación con un control estándar de atención. Hasta donde sabemos, este es el primer estudio que evalúa los costes sanitarios del tratamiento de pacientes con bronquiectasia no fibrosis quística con HFCWO.El costo general incluyó el costo de los antibióticos, las visitas al servicio de urgencias y las hospitalizaciones relacionadas con las exacerbaciones asociadas con las bronquiectasias por fibrosis no quística. El estudio demostró una reducción significativa en la utilización de la atención médica y su costo asociado cuando los pacientes con bronquiectasias fueron tratados con SmartVest durante un año. El costo total se redujo en un 60%, lo que se traduce en un ahorro de $ 3,045 por paciente por año.
Un estudio reciente que evaluó las altas hospitalarias, los reingresos y las visitas al servicio de urgencias por EPOC o bronquiectasias en adultos en los Estados Unidos encontraron que entre 2001 y 2012 el número de altas hospitalarias aumentó en 88.000.31 El estudio también encontró que alrededor del 7% de los pacientes con EPOC o bronquiectasias fueron readmitidos dentro de los 30 días con EPOC o bronquiectasias como diagnóstico principal31. En contraste, la tasa de altas disminuyó para otras enfermedades31. El motivo del aumento significativo de la EPOC y las visitas al hospital y al servicio de urgencias no está claro, ya que se ha observado una disminución significativa en las tasas de tabaquismo. Sin embargo, puede reflejar el potencial infradiagnóstico de la enfermedad y la naturaleza a largo plazo de la EPOC y las bronquiectasias en una población que envejece.31
Un estudio de revisión de casos anterior basado en resultados informó que el uso de SmartVest redujo las hospitalizaciones en 1,5 veces, lo que indica el costo-beneficio de HFCWO en la reducción de la carga de utilización de la atención médica. Otros estudios también han evaluado factores (tanto del sistema como del paciente) que pueden reducir el reingreso en pacientes con EPOC y son, al menos en parte, relevantes para pacientes con bronquiectasias. Estos factores incluyen la continuidad con la atención primaria del paciente o el neumólogo, la intervención del coordinador de altas y la extensión o el tipo de terapia respiratoria32-34
La reducción en el número de exacerbaciones relacionadas con bronquiectasias también puede afectar a 35,36 En una población de pacientes con EPOC, el uso de SmartVest se asoció con una mejora significativa en la puntuación de cinco síntomas P = 0,002 (calificación de esputo, sibilancias, tos, dificultad para respirar y tolerancia al ejercicio ) .36 El tratamiento con SmartVest también demostró una mejora significativa en el Cuestionario Respiratorio de St. George (SGRQ) P = 0,02, mientras que no se observó ninguna mejora en los pacientes tratados con el tratamiento convencional36. De manera similar, nuestro estudio anterior de revisión de casos basado en resultados encontró que 68 El% de los sujetos indicaron durante la entrevista telefónica que el uso de SmartVest había mejorado significativamente su calidad de vida.25
Se deben considerar varias limitaciones al diseño del estudio rojo al interpretar los resultados. El tamaño de los pacientes del estudio fue pequeño, y los datos de hospitalizaciones, visitas al servicio de urgencias y uso de antibióticos después del inicio de la terapia SmartVest se obtuvieron principalmente a través de una entrevista al paciente. El estudio puede considerarse conservador debido a que no se agregan costos a los honorarios del médico asociados a una visita al consultorio que resulta en una prescripción de antibióticos o, a que no se agregan costos a una visita al consultorio que no resultó en una prescripción de antibióticos. Además, la dependencia de las bases de datos de HCUP, NIS y AHRQ, que dependen de los diagnósticos ingresados en las reclamaciones, pueden estar codificadas incorrectamente o no codificadas en absoluto, lo que podría introducir un error de medición con respecto a las variables basadas en ICD-9-CM.
La reducción de los costos de utilización de la atención médica, como el uso de antibióticos, las visitas a los servicios de urgencias y las hospitalizaciones, son objetivos prioritarios de las directivas de atención médica recientes, como la Ley de Cuidado de Salud Asequible (ACA). Por ejemplo, la ACA ha establecido el Programa de reducción de readmisiones hospitalarias (HRRP), que ha ordenado a CMS que penalice a los hospitales reduciendo los pagos de reembolso por el exceso de readmisiones de pacientes por la misma afección. El HRRP identificó originalmente las tres principales «condiciones aplicables» para la medición de readmisión enfocada para incluir infarto agudo de miocardio, insuficiencia cardíaca y neumonía. Además, CMS finalizó recientemente la expansión de condiciones adicionales aplicables a partir del programa del año fiscal 2015 para incluir pacientes readmitidos por un exacerbación aguda de la EPOC. La reducción significativa en la utilización de atención médica y las hospitalizaciones para pacientes con bronquiectasias no quísticas que usan SmartVest, como se demostró en este estudio y otros, puede desempeñar un papel fundamental para ayudar a los hospitales a reducir los reingresos y, por lo tanto, no ser penalizados.
Para los pacientes que tienen infecciones de las vías respiratorias resistentes a los antibióticos orales, la carga es mucho mayor y más grave. Los antibióticos intravenosos complican enormemente la atención porque se requiere hospitalización o control domiciliario. El tratamiento para estos pacientes incluye la colocación de un catéter venoso central, la coordinación de las dosis de medicamentos que a menudo deben administrarse múltiples varias veces al día, análisis de sangre periódicos para controlar los efectos secundarios y medición de los niveles sanguíneos del antibiótico durante muchos días, pasos que se vuelven costosos y perturban la vida de los pacientes.
La Organización Mundial de la Salud (OMS) ha declarado que la resistencia microbiana a los antibióticos representa una «gran amenaza mundial con consecuencias devastadoras para la salud pública». La resistencia a los antimicrobianos amenaza la prevención y el tratamiento eficaces de una gama cada vez mayor de infecciones causadas no solo por bacterias, sino también por virus y hongos.Los Centros para el Control y la Prevención de Enfermedades (CDC) de EE. UU. Consideran que la resistencia a los antimicrobianos es una de sus principales preocupaciones y prioridades. Solo en los EE. UU., Al menos 2 millones de personas se infectan con bacterias que son resistentes a los antibióticos y al menos 23,000 personas mueren cada año como resultado directo de esas infecciones.39 En respuesta a la preocupación mundial, los Centros para Medicare de EE. UU. & Medicaid Services (CMS) publicó recientemente un cambio de regla propuesto a sus Condiciones de participación que, entre otros cambios, requeriría que los hospitales implementen programas de administración de antibióticos para poder participar en los programas de Medicare y Medicaid. La administración de antibióticos incluye la mejora de los resultados de los pacientes mediante la adopción de procesos y procedimientos que reducen la incidencia de infecciones con pa atención especial a la neumonía, como la atención del tratamiento preventivo. Como beneficio secundario de los resultados de costo-beneficio de este estudio, una reducción significativa en la necesidad de antibióticos en pacientes con bronquiectasias mediante el uso de SmartVest puede tener beneficios aún mayores que la disminución del costo. Un tratamiento disponible que podría reducir significativamente las infecciones respiratorias y, por lo tanto, la necesidad de antibióticos encaja bien en los programas de control de infecciones del hospital.
En resumen, la efectividad clínica de la depuración de las vías respiratorias con HFCWO demostrada por SmartVest en pacientes con EPOC36 y aquellos con bronquiectasias, 25 y la reducción significativa en los costos de antibióticos, urgencias y hospitalización observada en este estudio respalda el costo-beneficio del uso de SmartVest y aboga por la cobertura de seguro de SmartVest por parte de los pagadores. Además, los beneficios secundarios, como el potencial de reducir las reingresos hospitalarios y el potencial de impacto en la disuasión de la resistencia a los antibióticos, pueden tener beneficios aún mayores que la disminución de costos.
Descargue el texto del estudio
Agradecimientos
Los autores desean agradecer a Elizabeth Goodwin PhD por su apoyo editorial.
- King P. Patogénesis de las bronquiectasias. Paediatr Respir Rev 2011; 12 (2): 104-110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Compresión torácica de alta frecuencia: una terapia práctica para pacientes con bronquiectasia. Terapia respiratoria 2008; 3 (1): 22-26.
- Patel IS, Vlahos I, Wilkinson TM, et al. Bronquiectasia, índices de exacerbación e inflamación en la enfermedad pulmonar obstructiva crónica. Am J Respir Crit Care Med 2004; 170 (4): 400-407. 10.1164 / rccm.200305-648OC
- Gono H, Fujimoto K, Kawakami S, et al. Evaluación del espesor de la pared de las vías respiratorias y el atrapamiento de aire por TCAR en el asma asintomática. Eur Respir J 2003; 22 (6): 965-971.
- Weycker D, Edelsberg J, Oster G, et al. Prevalencia y carga económica de las bronquiectasias. Clinical Pulmonary Medicine 2005; 12 (4): 205-209.
- Seitz AE, Olivier KN, Adjemian J, et al. Tendencias en bronquiectasias entre los beneficiarios de Medicare en los Estados Unidos, 2000 a 2007. CHEST Journal 2012; 142 (2): 432-439.
- Seitz AE, Olivier KN, Steiner CA, et al. Tendencias y carga de hospitalizaciones asociadas a bronquiectasias en Estados Unidos, 1993-2006. Pecho 2010; 138 (4): 944-949. 10.1378 / chest.10-0099
- Seitz AE, Olivier KN, Steiner CA, et al. Tendencias y carga de hospitalizaciones asociadas a bronquiectasias en Estados Unidos, 1993-2006. CHEST Journal 2010; 138 (4): 944-949.
- Weycker D, Edelsberg J, Oster G, et al. Prevalencia y carga económica de las bronquiectasias. Clinical Pulmonary Medicine 2005; 12: 205-209.
- Fibrosis. AoCPiC. Estándares de atención y buenas prácticas clínicas para el manejo de fisioterapia de la fibrosis quística 2011. Disponible en: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio 11 de junio .pdf.
- O’Donnell AE. Bronquiectasias. Pecho 2008; 134 (4): 815-823. 10.1378 / chest.08-0776
- Barker AF. Bronquiectasias. N Engl J Med 2002; 346 (18): 1383-1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Terapias no farmacológicas de depuración de las vías respiratorias: guías de práctica clínica basadas en la evidencia de la ACCP. Cofre 2006; 129 (1 Suplemento): 250S-259S. 10.1378 / chest.129.1 suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Tratamiento de la disfunción mucociliar. Chest 1996; 110 (4): 1048-1057.
- Arens R, Gozal D, Omlin KJ, et al. Comparación de la compresión torácica de alta frecuencia y la fisioterapia torácica convencional en pacientes hospitalizados con fibrosis quística. Am J Respir Crit Care Med 1994; 150 (4): 1154-1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Oscilación de alta frecuencia de la vía aérea y la pared torácica. Respir Care 2002; 47 (7): 797-807.
- Hansen LG, Warwick WJ.Sistema de compresión torácica de alta frecuencia para ayudar a eliminar la mucosidad del pulmón. Biomed Instrum Technol 1990; 24 (4): 289-294.
- Lange DJ, Lechtzin N, Davey C, et al. Oscilación de la pared torácica de alta frecuencia en ELA: un ensayo exploratorio, aleatorizado y controlado. Neurología 2006; 67 (6): 991-997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. El efecto a largo plazo de la terapia de compresión torácica de alta frecuencia sobre las complicaciones pulmonares de la fibrosis quística. Pediatr Pulmonol 1991; 11 (3): 265-271.
- Kluft J, Beker L, Castagnino M, et al. Una comparación de los tratamientos de drenaje bronquial en la fibrosis quística. Pediatr Pulmonol 1996; 22 (4): 271-274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P
- Scherer TA, Barandun J, Martinez E, et al. Efecto de la oscilación de alta frecuencia de las vías respiratorias orales y la pared torácica y la fisioterapia torácica convencional sobre la expectoración en pacientes con fibrosis quística estable. Chest 1998; 113 (4): 1019-1027.
- Nicolini A, Cardini F, Landucci N, et al. Efectividad del tratamiento con oscilación de la pared torácica de alta frecuencia en pacientes con bronquiectasias. BMC Pulm Med 2013; 13: 21. 10.1186 / 1471-2466-13-21
- Osman LP, Roughton M, Hodson ME, et al. Estudio comparativo a corto plazo de la oscilación de la pared torácica de alta frecuencia y las técnicas europeas de limpieza de las vías respiratorias en pacientes con fibrosis quística. Tórax 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Despeje de las vías respiratorias asistido por alta frecuencia. Respir Care 2007; 52 (9): 1224-1235; discusión 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Uso de la oscilación de alta frecuencia de la pared torácica en una población de pacientes con bronquiectasias: una revisión de casos basada en resultados. Respiratory Therapy Journal 2016; 11 (4): 34-38.
- HCUP. Descripción general de la muestra del Departamento de Emergencias Nacional (NEDS) 2016. Disponible en: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Descripción general de las muestras de pacientes hospitalizados a nivel nacional (a nivel nacional). Disponible en: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C.Cost for Hospital Stays in the Estados Unidos, 2010: Resumen estadístico # 146. Resúmenes estadísticos del proyecto de costo y utilización de la atención médica (HCUP). Rockville (MD): Agencia para la Investigación y la Calidad de la Atención Médica (EE. UU.); 2006.
- Stein PD, Matta F. Costos de visitas al departamento de emergencias y hospitalizaciones por hipertensión arterial pulmonar.
J Epidemiol Public Health Rev 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Reembolso por administración de atención de transición para reducir la readmisión por EPOC. Pecho
2014; 145 (1): 149-155. 10.1378 / cofre.13-0787 - Ford ES. Egresos hospitalarios, readmisiones y visitas al servicio de urgencias por EPOC o bronquiectasias entre adultos estadounidenses: resultados de la muestra nacional de pacientes hospitalizados 2001-2012 y la muestra nacional del departamento de emergencias 2006-2011. Pecho 2015; 147 (4): 989-998. 10.1378 / chest.14-2146
- Sharma G, Kuo YF, Freeman JL, et al. Visita de seguimiento ambulatorio y visita a urgencias de 30 días y reingreso en pacientes hospitalizados por enfermedad pulmonar obstructiva crónica. Arch Intern Med 2010; 170 (18): 1664-1670. 10.1001 / archinternmed.2010.345
- Lainscak M, Kadivec S, Kosnik M, et al. La intervención del coordinador del alta evita las hospitalizaciones en pacientes con EPOC: un ensayo controlado aleatorizado. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O, Sewell L, Morgan MD, et al. El programa corto de rehabilitación pulmonar ambulatoria reduce la readmisión después de una hospitalización por una exacerbación de la enfermedad pulmonar obstructiva crónica. Respirología 2013; 18 (7): 1063-1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. La terapia de humidificación de aire a largo plazo es rentable para pacientes con enfermedad pulmonar obstructiva crónica moderada o grave o bronquiectasia. Value Health 2014; 17 (4): 320-327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. Un estudio piloto del impacto de la oscilación de la pared torácica de alta frecuencia en pacientes con enfermedad pulmonar obstructiva crónica con hipersecreción de moco. Int J Chron Obstruct Pulmon Dis 2011; 6: 693-699. 10.2147 / EPOC. S22896.
- Martınez-Garcıa MA, et al. Valor pronóstico de las bronquiectasias en pacientes con enfermedad pulmonar obstructiva crónica de moderada a grave. Am J Respir Crit Care Med 2013; Vol. 187, edición. 8, págs. 823–831.
- O’Donnell AE. Bronquiectasias. Chest 2008; 134: 815–82.
- Centros para el Control y la Prevención de Enfermedades – Sitio web de resistencia a antibióticos / antimicrobianos https://www .cdc.gov / drugresistance /