Molécula de ATP
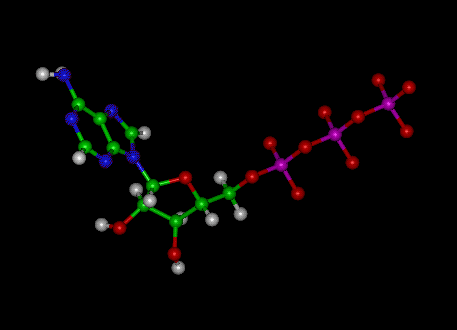
La molécula de trifosfato de adenosina (ATP) es el nucleótido conocido en bioquímica como la «moneda molecular» de la transferencia de energía intracelular; es decir, el ATP puede almacenar y transportar energía química dentro de las células. El ATP también juega un papel importante en la síntesis de ácidos nucleicos.
Para la estructura 3-D de esta imagen usando JsmolHaga clic aquí
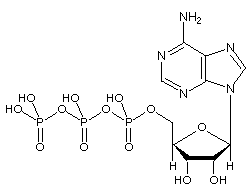
Imagen: Estructura molecular del ATP
La energía se libera por hidrólisis del tercer grupo fosfato. Después de que se libera este tercer grupo fosfato, el ADP resultante (difosfato de adenosina) puede absorber energía y recuperar el grupo, regenerando así una molécula de ATP; esto permite que el ATP almacene energía como una batería recargable.
Posiciones de fosforilo
Los grupos fosforilo que comienzan con el del AMP se denominan fosfatos alfa, beta y gamma.
Propiedades físicas y químicas
El ATP consta de adenosina, compuesta por un anillo de adenina y un azúcar ribosa, y tres grupos fosfato (trifosfato). Los grupos fosforilo, comenzando por el grupo más cercano a la ribosa, se denominan fosfatos alfa (α), beta (β) y gamma (γ). En consecuencia, está estrechamente relacionado con el nucleótido de adenina, un monómero del ARN. El ATP es muy soluble en agua y es bastante estable en soluciones entre pH 6,8 y 7,4, pero se hidroliza rápidamente a pH extremo. En consecuencia, el ATP se almacena mejor como una sal anhidra.
El ATP es una molécula inestable en agua no tamponada, en la que se hidroliza a ADP y fosfato. Esto se debe a que la fuerza de los enlaces entre los grupos fosfato del ATP es menor que la fuerza de los enlaces de hidrógeno (enlaces de hidratación), entre sus productos (ADP y fosfato) y el agua. Por lo tanto, si el ATP y el ADP están en equilibrio químico en el agua, casi todo el ATP eventualmente se convertirá en ADP. Un sistema que está lejos del equilibrio contiene energía libre de Gibbs y es capaz de realizar un trabajo. Las células vivas mantienen la proporción de ATP a ADP en un punto diez órdenes de magnitud desde el equilibrio, con concentraciones de ATP cinco veces más altas que la concentración de ADP. Este desplazamiento del equilibrio significa que la hidrólisis del ATP en la célula libera una gran cantidad de energía libre.
Dos enlaces fosfoanhídrido (los que conectan fosfatos adyacentes) en una molécula de ATP son responsables del alto contenido energético de esta molécula. En el contexto de las reacciones bioquímicas, estos enlaces de anhídrido se conocen con frecuencia, y a veces de manera controvertida, como enlaces de alta energía (a pesar de que se necesita energía para romper los enlaces). La energía almacenada en ATP puede liberarse tras la hidrólisis de los enlaces anhídrido. El grupo fosfato primario en la molécula de ATP que se hidroliza cuando se necesita energía para impulsar reacciones anabólicas es el grupo γ-fosfato. Ubicado más lejos del azúcar ribosa, tiene una energía de hidrólisis más alta que el α- o β-fosfato. Los enlaces formados después de la hidrólisis, o la fosforilación de un residuo por ATP, son más bajos en energía que los enlaces fosfoanhídrido de ATP. Durante la hidrólisis de ATP catalizada por enzimas o la fosforilación por ATP, un sistema vivo puede aprovechar la energía libre disponible para realizar su trabajo.
Cualquier sistema inestable de moléculas potencialmente reactivas podría potencialmente servir como una forma de almacenamiento libre energía, si la célula mantuvo su concentración lejos del punto de equilibrio de la reacción. Sin embargo, como es el caso de la mayoría de las biomoléculas poliméricas, la descomposición de ARN, ADN y ATP en monómeros más simples está impulsada por consideraciones de liberación de energía y aumento de entropía, tanto en concentraciones estándar como en las concentraciones encontradas dentro de la célula.
La cantidad estándar de energía liberada por la hidrólisis de ATP se puede calcular a partir de los cambios de energía en condiciones no naturales (estándar), y luego se corrige a concentraciones biológicas. El cambio neto en energía térmica (entalpía) a temperatura y presión estándar de la descomposición de ATP en ADP hidratado y fosfato inorgánico hidratado es -30.5 kJ / mol, con un cambio en energía libre de 3.4 kJ / mol. La energía liberada al escindir una unidad de fosfato (Pi) o pirofosfato (PPi) del ATP en el estado estándar de 1 M es:
ATP + H
2O → ADP + Pi ΔG ° = −30.5 kJ / mol (−7,3 kcal / mol)
ATP + H
2O → AMP + PPi ΔG ° = −45,6 kJ / mol (−10,9 kcal / mol)
Estos valores pueden ser utilizado para calcular el cambio de energía en condiciones fisiológicas y la relación celular ATP / ADP. Sin embargo, cada vez se utiliza más un valor más representativo (que tiene en cuenta la AMP) denominado cargo de energía. Los valores dados para la energía libre de Gibbs para esta reacción dependen de varios factores, incluida la fuerza iónica general y la presencia de iones de metales alcalinotérreos como Mg2 +
y Ca2 +
.En condiciones celulares típicas, ΔG es aproximadamente -57 kJ / mol (-14 kcal / mol).
Síntesis
El ATP puede ser producido por varios procesos celulares, más típicamente en las mitocondrias por fosforilación oxidativa bajo la influencia catalítica de la ATP sintasa o en el caso de las plantas en cloroplastos por fotosíntesis.
Los principales combustibles para la síntesis de ATP son la glucosa y los ácidos grasos. Inicialmente, la glucosa se descompone en piruvato en el citosol. Se generan dos moléculas de ATP por cada molécula de glucosa. Las etapas terminales de la síntesis de ATP se llevan a cabo en la mitocondria y pueden generar hasta 34 ATP.
ATP en el cuerpo humano
La cantidad total de ATP en el cuerpo humano es aproximadamente 0,1 mol. La energía que consume diariamente un adulto requiere la hidrólisis de 200 a 300 moles de ATP. Esto significa que cada molécula de ATP debe reciclarse de 2000 a 3000 veces durante el día. El ATP no se puede almacenar, por lo que su síntesis debe seguir de cerca su consumo.
Otros trifosfatos
Las células vivas también tienen otros nucleósidos trifosfatos de «alta energía», como el trifosfato de guanina. Entre ellos y el ATP, la energía se puede transferir fácilmente con reacciones como las catalizadas por la nucleósido difosfoquinasa: la energía se libera cuando se lleva a cabo la hidrólisis de los enlaces fosfato-fosfato. Esta energía puede ser utilizada por una variedad de enzimas, proteínas motoras y proteínas de transporte para realizar el trabajo de la célula. Además, la hidrólisis produce fosfato inorgánico libre y difosfato de adenosina, que se pueden descomponer aún más en otro ion fosfato y monofosfato de adenosina. El ATP también se puede descomponer directamente en monofosfato de adenosina, con la formación de pirofosfato. Esta última reacción tiene la ventaja de ser un proceso efectivamente irreversible en solución acuosa.
Reacción de ADP con GTP
ADP + GTP > ATP + GDP