Fysiologian rajat
Johdanto
Valtimoiden baroretseptorit toimivat etulinjan antureina verenpaineen muutosten havaitsemiseksi verenkierrossa. Verenpaineen muutokset stimuloivat mekanosensitiivisiä hermopäätteitä, jotka sijaitsevat valtimon seinämissä. Mekaaninen voima siirretään sähköisiin signaaleihin hermopäätteissä, mikä johtaa paineesta riippuviin toimintapotentiaalien laukauksiin baroreceptorihermoneissa. Hermosignaalit etenevät sitten aivorungon sydän- ja verisuonikontrollikeskukseen verenpaineen barorefleksi säätelyä varten (Levy MN, 2007). Lisäksi supra-medullaarisilla rakenteilla, mukaan lukien keskiaivojen cuneiform-ydin ja ventraalinen mediaalinen prefrontaalinen aivokuori, on myös estävä rooli baroreflex-säätelyssä (Verberne et ai., 1997).
On olemassa kaksi valtimoiden baroretseptoria, nimittäin aortan baroreceptorit ja kaulavaltimon baroreceptorit, jotka sijaitsevat aortan kaaren adventitia-kerroksessa ja kaulavaltimot. Aortan baroretseptorit havaitsevat verenpaineen aortassa. Aortan baroretseptorien solurungot (soma) sijaitsevat nodoosiganglionissa (NG) (kuva 1). Aortan baroreseptorin hermopäätteistä tulevat hermosignaalit välitetään nodoosiganglioniin aistinhermon, aortan depressorihermon (ADN), kautta (kuva 1). Kaulavaltimon baroreceptorit havaitsevat verenpaineen kaulavaltimosta, joka toimittaa verta aivoihin. Kaulavaltimon baroretseptorien hermoterminaalit sijaitsevat kahdenvälisesti kaulavaltimon haarautumissa lähellä sisäistä kaulavaltimoa. Kaulavaltimon baroretseptoreiden hermosignaalit kulkevat kaulavaltimon sinushermoja (CSN) pitkin somaansa, joka on lokalisoitu petrosaalisessa ganglionissa (PG). Petrosaalinen ganglioni työntyy kaula-aukon ulkopuolelle (kuva 1) (McDonald, 1983; Shoukas et ai., 1991; Vander ym., 1998; Sato et ai., 1999; Donnelly ja Rigual, 2000; Weijnen et ai., 2000) . Koska aortan baroretseptorit aistivat verenpaineen aortassa, joka toimittaa verta koko systeemiseen verenkiertoon, näillä baroretseptoreilla odotetaan olevan tärkeä toiminnallinen rooli yleisen systeemisen verenpaineen ylläpitämisessä. Toisaalta kaulavaltimon baroretseptorit havaitsevat aivoihin toimitettavan veren paineen. Nämä baroretseptorit voivat olla tärkeämpiä ylläpitämään vakaa aivoverenpaine ja aivoverenkierto.
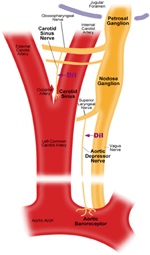
Kuva 1. Kaavio aortan ja kaulavaltimon baroreseptorin terminaaleista ja hermoista. Kaavio, joka kuvaa aortan ja kaulavaltimon baroretseptoreiden hermopäätteiden, niiden hermokuitujen ja somata-alueiden anatomisia asemia. Aortan baroretseptoripäätteet sijaitsevat aortan kaaressa. Sen afferentti hermokuitu on aortan depressorihermo. Soma on nodoosiganglionissa (NG). Kaulavaltimon baroretseptori on sijoitettu sisäiseen kaulavaltimoon kaulavaltimon haarautumisen vieressä. Sen afferentti hermo on kaulavaltimon sinushermo. Soma sijaitsee petrosaalisessa ganglionissa (PG).
On olemassa ristiriitaisia raportteja siitä, mitkä baroretseptorit, aortan baroretseptorit tai kaulavaltimo baroretseptorit, ovat herkempiä verenpaineen muutokselle. Jotkut tutkijat kertoivat, että kaulavaltimon baroretseptorit ovat herkempiä paineelle (Donald ja Edis, 1971; Fadel ym., 2003), kun taas toiset uskovat, että aortan baroretseptorit ovat herkempiä paineelle (Glick ja Covell, 1968; Pickering et ai., 2008), ja toiset taas eivät ole ilmoittaneet eroa näiden kahden baroretseptorin välisessä paineherkkyydessä (Hainswor et ai., 1970; James ja Daly, 1970). Lähes kaikissa näissä aikaisemmissa tutkimuksissa kuitenkin baroreflexivasteita (kuten syke ja munuaisten sympaattinen hermoaktiivisuus) käytettiin baroretseptorin herkkyysmäärityksen päätepisteinä. Vielä ei ole tutkimusta, joka rekisteröi ja vertaa suoraan aortan ja kaulavaltimon baroretseptorin hermosolujen paineherkkyyttä sinänsä.
Tässä olemme käyttäneet suurnopeuspainekiinnikettä muuttamaan baroreseptorin hermosolujen sisällä olevaa hydrostaattista painetta näiden neuronien vastaavat elektrofysiologiset vasteet kokosolujen kiinnittämällä. Käytimme myös yksiaksiaalista venytyskammiota baroreceptorihermosolujen venyttämiseen ja mitasimme vastaavat muutokset sytosolisessa Ca2 +: ssa näissä neuroneissa. Lisäksi in vivo eläintutkimuksia varten mitasimme paineen aiheuttamat toimintapotentiaalipotkut aortan depressorissa ja kaulavaltimon hermosoluissa, jotka ovat aortan ja kaulavaltimon baroretseptorien aistihermot.
Materiaalit ja menetelmät
Eläimet
Kaikki eläinkokeet tehtiin Hongkongin erityishallintoalueen hallituksen myöntämän luvan nojalla ja Hongkongin Kiinan yliopiston eläinkokeiden eettisen komitean hyväksynnällä.Sprague-Dawley (S / D) urosrotat (180–200 g) toimitti Hongkongin kiinalaisen yliopiston laboratorioeläinten palvelukeskus.
Ensikulttuuri
S / D rotat nukutettiin pentobarbitaalinatriumilla (100 mg / kg). Vasen kohdunkaulan alue paljastettiin keskiviivan viillolla steriloidussa tilassa. Kuten kuvassa 1 on esitetty, aortan depressorihermo tai kaulavaltimon sinushermo paljastettiin ja 2-3 mm hermosta irrotettiin varovasti ympäröivistä kudoksista tylpällä leikkauksella. Fluoresoivia lipofiilisiä merkkiaineita 1,1-dioktadekyyli-3,3,3 ’, 3’-tetrametyyli-indokarbosyaniini (DiI) -kiteitä (Invitrogen) levitettiin hermon ympärille ja peitettiin Kwik-Silillä (World Precision Instruments, USA). Viilto ommeltiin sen jälkeen. Rottien annettiin toipua 5–7 päivän ajan, jotta DiI-väriaine diffundoitui taaksepäin aortan depressorihermoa tai kaulavaltimon sinushermoa pitkin somataan, joka sijaitsee vastaavasti nodoosiganglionissa tai petrosaaliranglionissa. neuronit eristettiin DiI-leimattuista rotista ja leikattiin palasiksi jääkylmässä EBSS: ssä. Ne pilkottiin yhden tunnin ajan 37 ° C: ssa trypsiinillä (1 mg / ml) ja kollagenaasi IA: lla (1 mg / ml). Yksittäiset neuronit dispergoitiin varovaisella hieronnalla Glass Pasteur -pipetillä, mitä seurasi sentrifugointi. Neuronit suspendoitiin uudelleen ja viljeltiin DMEM / F-12-elatusaineessa, johon oli lisätty 5% FBS: ää, 1% antibiootti-antimykoottista ja 7S NGF: ää (100 ng / ml). Sytosiiniarabinofuranosidia (Ara-C; 10 μM) lisättiin elatusaineeseen estämään jakautuvien solujen kasvua. Neuroneja viljeltiin vähintään 3 päivää ennen kokeita. Toimintapotentiaalin kirjaamista varten neuronit eristettiin juuri ja inkuboitiin F12: ssa vähintään 30 minuuttia ennen kokeita. Kaikkia kokeita varten soluja inkuboitiin lasilevyillä, jotka oli esipinnoitettu 0,1 mg / ml poly-L-lysiinillä, lukuun ottamatta solujen venytyskokeita, joissa silikonikammioissa oli esipäällystetty 2% gelatiinia. h3> Patch Clamp
Koko solun virtapihtien tallennus saavutettiin EPC7-patch-puristusvahvistimella (HEKA, Saksa). Patch-pipetit, joiden vastus on 3–5 MΩ, täytettiin pipettiliuoksella (mM): 130 K-glukonaattia, 10 KCl, 2 MgCl2, 2 Na2ATP, 0,4 Tris GTP, 1 EGTA, 10 HEPES, pH 7,25-7,3 KOH: lla. Solut kylvettiin keinotekoisessa aivo-selkäydinnesteessä (ACSF) (mM): 120 NaCl, 2 KCl, 1,2 MgSO4 · 7H2O, 1,2 KH2PO4, 26 NaHCO3, 2,5 CaCl2, 11 glukoosia, tasapainotettu karbogeenilla (95% O2 ja 5 % CO2). Nykyisessä puristintallennuksessa soluja pidettiin lepokalvopotentiaalissaan. Nopean paineen kiinnitysjärjestelmää (HSPC-1, ALA Scientific Instruments, USA) käytettiin positiivisen paineen tuottamiseksi soluun mikropipetin kautta. Tallenteista otettiin näyte 50 kHz: llä ja suodatettiin 5 kHz: llä. Tiedot analysoitiin PulseFitillä (HEKA). Kaikki kokeet suoritettiin huoneen lämpötilassa.
Kalsiumkuvantaminen
Sytosolinen Ca2 + -mittaus suoritettiin muualla kuvatulla tavalla (Wong et ai., 2010). Lyhyesti, soluihin ladattiin 5 μM Fluo-4 / AM 40 minuutin ajan. Sytosolinen Ca2 + -mittaus suoritettiin HEPES-puskuroidulla liuoksella (mM): 140 NaCl, 2,5 KCl, 1 MgCl2, 1 CaCl2,10 HEPES, 10 glukoosi, pH 7,4 NaOH: lla. Sytosolinen Ca2 + -muutos vasteena yksiaksiaaliselle venytykselle suoritettiin STREX-solujen venytysjärjestelmällä (ST-150, B-Bridge International, Inc.). Soluja stimuloitiin 10, 20 tai 30%: lla yksisuuntaisella venytyksellä 1 sekunnin ajan. Sytosolinen Ca2 + -vaste mitattiin huoneen lämpötilassa. Fluo-4-fluoresenssi kirjattiin ja analysoitiin FV1000-laserskannaus-konfokaalisella kuvantamisjärjestelmällä. Muutos sytosolisessa Ca2 + -fluoresenssivasteessa ilmaistiin reaaliaikaisen fluoresenssin suhteena (Fx / F0), jossa Fx on reaaliaikainen fluo-4 / AM-signaali ja F0 on lähtötilanteen fluo-4 / AM-signaali ennen venymistä. / p>
Hermoston aktiivisuuden kirjaaminen
Rotat nukutettiin 100 mg / kg pentobarbitaalinatriumilla. Kohdunkaulan alue paljastettiin viivan viillolla. Oikea kaulavaltimo eristettiin ja kanyloitiin katetrilla, joka liitettiin paineanturiin (ML221, ADInstruments, USA) verenpaineen kirjaamista varten. Vasen reisilaskimo kanyloitiin fenyyliefriini- ja SNP-injektiota varten. Vasen aortan depressorihermo tai kaulavaltimon hermo liitettiin kaksisuuntaiseen hopeaelektrodiin, jota seurasi vahvistin (malli 1700 Differential AC Amplifier, A-M Systems Inc., USA). Sekä verenpaine että hermoaktiivisuus rekisteröitiin jatkuvasti kaaviossa 5.0 (AD Instruments). Hermoaktiivisuus vahvistettiin 10000 kertaa ja suodatettiin kaistanpäästöllä 100–5000 Hz. Keskimääräisen valtimopaineen, sykkeen ja piikin taajuuden arvot vastauksena fenyyliefriiniin analysoitiin kaavion 5.0 ohjelmistolla. Piikkitaajuuden muutos (piikkitaajuus fenyyliefriinin jälkeen – piikkitaajuus ennen fenyyliefriiniä) vasteena maksimaaliseen verenpaineen muutokseen (keskimääräinen valtimoverenpaine fenyyliefriinin jälkeen – keskimääräinen valtimoverenpaine ennen fenyyliefriiniä) laskettuna fenyyliefriinin injektiolla (Lau et al., 2016) .
Tilastollinen analyysi
Edustavat jäljet piirrettiin aikarajan jälkeinä. Kaikkien kokeiden tulokset koottiin pylväsdiagrammiksi, joka ilmaistiin yksittäisten kokeiden keskiarvona ± sem. Tilastolliseen analyysiin käytettiin Studentin t-testiä. Parinmukaista t-testiä käytettiin tarvittaessa.
Tulokset
Aortan masennusneuronien ja kaulavaltimon sinusneuronien ominaisuudet
Dil levitettiin joko aortan depressor-hermoon tai kaulavaltimon sinus-hermoon.Siksi Dil-leimattuihin neuroneihin nodoosiganglionissa sisältyivät aortan kaarta innervoivat baroreceptor-neuronit ja aortan runkoa innervoivat kemoreceptorihermot. Toisaalta Dil-leimatut neuronit petrosaaliranglioniin sisältyivät kaulavaltimoa innervoivat baroreceptorihermonot ja kaulavaltimon runkoa innervoivat kemoreceptorihermot. Tutkimme ensin näiden Dil-leimattujen neuronien perusominaisuudet. DiI-leimatut hermosolut nodoosissa ja petrosaaliranglionissa viljeltiin erikseen ja alistettiin depolarisoivalle sähkövirralle Kuvassa 2 on kirjattu kahden tyyppisiä vasteita, yksi vastasi yhdellä ja toinen jatkuvalla potentiaalilla depolarisoivan virran jälkeen (kuva 2) (Belmonte ja Gallego, 1983). Näille hermosoluille tehtiin sen jälkeen hydrostaattinen paineprotokolla niiden herkkyyden testaamiseksi hydrostaattisen paineen muutoksille. Positiivista hydrostaattista paineramppua levitettiin solunsisäisesti lasimikropipetin läpi suurnopeuspaineen kiinnitysjärjestelmällä (HSPC-1, ALA Scientific Instruments, USA), kunnes toimintapotentiaalit syntyivät. Tulokset osoittivat, että 45% aortan baroreceptorihermoneista ampui jatkuvaa toimintapotentiaalia vasteena depolarisoivalle sähkövirralle (taulukko 1A). Niistä 91% (41% / 45%) reagoi myös hydrostaattiseen paineenmuutokseen ja osoitti paineesta riippuvia toimintapotentiaalipaloja (taulukko 1A). Loput 55% aortan baroreceptorihermoneista laukaisivat vain yhden toimintapotentiaalin vasteena depolarisoivalle virralle (taulukko 1A), ja 40% (22% / 55%) pystyi vastaamaan paineen muutokseen (taulukko 1A). Karotidibaroreseptorihermoneille 45% soluista antoi jatkuvaa toimintapotentiaalia, kun niitä stimuloitiin depolarisoivalla virralla (taulukko 1B). Heistä 82% (37% / 45%) oli myös herkkä paineen muutokselle (taulukko 1B). Lisäksi kaulavaltimon baroreceptorihermoneista, jotka vain antoivat yhden toimintapotentiaalin vasteena depolarisoivalle virralle, 24% (13% / 55%) pystyi vastaamaan paineen muutokseen (taulukko 1B).
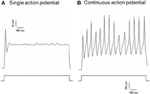
Kuva 2. Toimintapotentiaalin tallennus viljellyistä aortan depressorista ja kaulavaltimon sinusneuroneista. Esitetyt ovat toimintapotentiaalien jäljet, jotka kirjattiin kahdesta edustavasta aortan masennus- / kaulavaltimon sinusneuronista depolarisoivalla virralla. (A) edustavat neuronit, jotka sytyttävät vain yhden toimintapotentiaalin nykyisen stimulaation yhteydessä; (B) Edustavat neuronit, jotka sytyttävät vain jatkuvaa toimintapotentiaalia nykyisen stimulaation yhteydessä. Alempi paneeli: nykyisen injektion protokolla. Mittapalkki, vaakasuora, 100 ms, pystysuora, 10 mV (ylemmät jäljet) ja 500 pA (alemmat jäljet). n = 27 ja n = 38 aortan depressorille ja kaulavaltimon sinusneuroneille.

Taulukko 1. Aortan depressorin ja kaulavaltimon sinusneuronien ominaisuudet.
Riippumatta siitä, laukaisivatko ne yksittäisen vai jatkuvan toimintapotentiaalin, 63% Dil-leimattujen aortan baroretseptorihermosolujen havaittiin olevan herkkiä paineenmuutokselle, kun taas vain 50% Dil-leimattuja kaulavaltimon baroretseptorihermoneita oli paineen muutos (taulukko 1).
Aortan ja kaulavaltimon baroretseptorineuronien venytysherkkyys
Aktiivipotentiaalin purkautumisen painekynnys analysoitiin. Kuten kuviosta 3 käy ilmi, aortan baroreceptorihermosolujen painekynnys (24 ± 4 mmHg) oli matalampi kuin kaulavaltimon baroreceptorihermosolujen (39 ± 4 mmHg).

Kuva 3. Aortan ja kaulavaltimon baroretseptorin hermosolujen herkkyys hydrostaattiselle paineelle. (A, B) Ylempi paneeli, edustavat aikarajan jäljet, jotka havainnollistavat paineesta riippuvaisia toimintapotentiaalipoltoksia aortan (A) ja kaulavaltimon (B) baroreseptorin hermosoluissa. Paineramppi (alempi paneeli) levitettiin solujen sisäpuolelle mikropipetin kautta käyttämällä suurnopeuspaineen kiinnitysjärjestelmää (HSPC). Asteikon vaaka, 1 s, pystysuora, 20 mV ja 20 mmHg. (C) Yhteenveto, joka osoittaa painekynnyksen, joka aloittaa toimintapotentiaalien laukaukset aortan ja kaulavaltimon baroreceptorihermoissa. n = 13 aortan baroreseptorin hermosoluille ja n = 15 kaulavaltimon baroreceptorihermoneille. *** p < 0,01, opiskelijan t-testillä.
Stretchin aiheuttama Ca2 + -vaste baroreceptorihermoneissa
Viljellyille aortan depressoreille tai kaulavaltimon sinusneuroneille tehtiin 10, 20 tai 30% yksiaksiaalisesta venytyksestä STREX-solujen venytysjärjestelmällä, yrittäen jäljitellä verisuonia venyttämällä verenpaineessa. Tulokset osoittivat, että 20-prosenttinen yksiakselinen venytys aiheutti merkittävän sytosolisen Ca2 + -fluoresenssin lisääntymisen aortan baroreseptorin hermosoluissa, mutta ei kaulavaltimon baroreseptorin hermosoluissa (kuviot 4A – C). Lisäksi Ca2 + -fluoresenssin suuruus nousee vastauksena 30-prosenttiseen yksiaksiaaliseen venytykseen oli paljon suurempi aortan baroreseptorin hermosoluissa kuin kaulavaltimon baroretseptorin hermosoluissa (kuvat 4A – C).
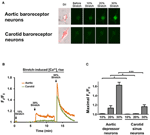
Kuva 4. Aortan depressorin ja kaulavaltimon sinusneuronien herkkyys yksiaksiaaliselle venytykselle. Solut ladattiin Ca2 + -herkällä fluoresoivalla väriaineella Fluo-4 / AM. Esitetyt ovat edustavia kuvia (A) ja aikajakson jäljet (B) suhteellisesta sytosolisesta Ca2 +: sta nousee vastauksena 10, 20 ja 30 prosentin yksiaksiaaliseen venytykseen aortan depressorissa ja kaulavaltimon sinusneuroneissa. (C) Yhteenveto maksimaalisesta sytosolisesta Ca2 + -noususta vasteena erilaiseen venytysasteeseen. Muutos sytosolisessa Ca2 +: ssa ilmaistiin muodossa Fx / F0, missä Fx on reaaliaikainen fluo-4 / AM-signaali ja F0 on lähtötilanteen fluo-4 / AM-signaali ennen venymistä. Keskiarvo ± s.t. (n = 5). * p < 0,05, *** p < 0,01 vastaavaan kontrolliin verrattuna pareittain t-testillä.
Baroretseptorin hermotoiminta in vivo
Kahden baroretseptorin hermoaktiivisuutta tutkittiin in vivo. Fenyyliefriini injektoitiin laskimoon. Verenpaineen muutokset fenyyliefriinin käytön yhteydessä on esitetty kuvioiden 5A, B yläpaneelissa. Baroreceptorin hermoaktiviteetin muutokset näkyvät alapaneelissa (kuviot 5A, B). Paineen aiheuttama hermoaktiivisuus oli paljon suurempi aortan depressorihermossa kuin kaulavaltimon sinushermossa (kuviot 5A, B). Piikkitaajuuden muutos / mmHg: n kasvu on esitetty yhteenvetona kuvassa 5C. Tulos osoitti, että aortan baroreseptorit ovat herkempiä hydrostaattiselle paineelle kuin kaulavaltimon baroreseptorit in vivo.
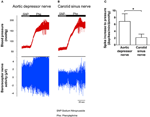
Kuva 5. Baroretseptorin hermoaktiivisuus rotalla in vivo. (A, B) Edustavat jäljet, jotka osoittavat muutoksen aortan depressorihermon (A) ja kaulavaltimon sinushermon (B) aktiivisuudessa verenpaineen kohotessa. Molemmissa (A, B) yläpaneeli oli verenpaineen muutos ennen Phe-levitystä ja sen jälkeen, kuten vaakapalkit osoittavat. Alempi paneeli oli vastaava muutos hermoaktiivisuudessa. (C) Yhteenveto tiedoista, jotka osoittavat hermoaktiivisuuden muutoksen verenpaineen muutosyksikköä kohti. Keskiarvo ± s.t. (n = 8). * p < 0,05 verrattuna vertailuun aortan baroretseptoreissa, pareittain suoritettavan t-testin avulla.
TRP-kanavien ilmentäminen
Useiden TRP-kanavien on raportoitu olevan mekaanisesti herkkiä, mukaan lukien TRPC1, -C3, -C5, -C6, -V1, -V4, -P2 (O ”Neil ja Heller, 2005; Christensen ja Corey, 2007; Pedersen ja Nilius, 2007; Patel ym., 2010; Lau ym., 2016). Tässä tutkittiin näiden mekanisensitiivisten TRP-kanavien mahdollista roolia suhteessa aortaan ja kaulavaltimon baroreseptorin herkkyys. Näiden kanavien mRNA-ilmentymiä nodoosissa ja petrosaalisessa ganglionissa verrattiin. Todettiin, että TRPV4: n ja TRPC6: n ilmentymät olivat korkeammat nodoosiganglionissa verrattuna petrosaaliseen ganglioniin (kuva 6). On mahdollista, että korkeampi mekanisensitiivisten kanavien ilmentyminen nodoosiganglionissa voi lisätä herkkyyttä.
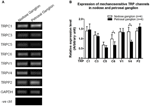
Kuva 6. mekaaniherkät TRP-kanavat nodoosissa ja petrosaalisessa ganglionissa. (A) Edustavat geelikuvat, joissa verrataan mekanisensitiivisten TRP-kanavien (TRPC1, -C3, -C5, -C6, -V1, -V4, -P2) mRNA-ekspressiotasoa nodoosin ja petrosaalisen ganglionneuronin välillä. Puolikvantitatiivista RT-PCR-analyysiä käytettiin useiden TRP-kanavien mRNA-ilmentymistasojen vertaamiseen GAPDH-mRNA-ilmentymiseen. Yhdeksän kokeen tulokset tiivistettiin kohdassa (B). Arvot olivat keskiarvossa ± sem. * p < 0,05, pareittain suoritettavan t-testin avulla.
Keskustelu
Tässä tutkimuksessa verrattiin aortan ja kaulavaltimon baroretseptoreiden mekaanisia herkistäviä ominaisuuksia. Kokosolujen laastarikiinnitystutkimukset osoittivat, että verrattuna kaulavaltimon sinusneuroneihin, suurempi prosenttiosuus aortan depressorihermoneista oli venytysherkkiä. Lisäksi painekynnyksen, joka saattoi aloittaa toimintapotentiaalin, havaittiin olevan alhaisemmat aortan baroreseptorin hermosoluissa kuin kaulavaltimon baroretseptorin hermosoluissa. Yksiaksiaalista venytyksen aiheuttamaa sytosolista Ca2 +: n nousua verrattiin myös aortan depressorin ja kaulavaltimon sinusneuronien välillä.Sytosolisen Ca2 + -nousun suuruus vasteena yksiaksiaaliselle venytykselle oli paljon suurempi aortan baroreseptorin hermosoluissa kuin kaulavaltimon baroretseptorin hermosoluissa. Aortan baroreceptorihermoneilla oli myös alempi sytosolisten Ca2 + -vasteiden kynnys yksiaksiaaliseen venytykseen. Toisessa kokeiden sarjassa havaitsimme, että paineen aiheuttama toimintapotentiaalien lisäys oli suurempi aortan depressorihermossa kuin kaulavaltimon sinushermossa. Yhdessä tiedot antavat vahvaa näyttöä siitä, että aortan baroretseptorit ovat herkempiä verenpaineelle kuin kaulavaltimon baroretseptorit.
Aikaisemmin on pyritty ymmärtämään kahden baroretseptorin herkkyyserot. Tulokset ovat kuitenkin kiistanalaisia. Joissakin raporteissa todettiin, että aortan baroretseptorit ovat herkempiä paineen muutoksille (Glick ja Covell, 1968; Fan ym., 1996; Pickering ym., 2008), kun taas toiset totesivat, että kaulavaltimon baroretseptorit ovat herkempiä paineen muutoksille (Donald ja Edis, 1971; Fadel et ai., 2003). Kuitenkin melkein kaikki nämä aiemmat tutkimukset liittyivät erittäin monimutkaisiin kirurgisiin toimenpiteisiin ja käyttivät lopulta barorefleksivasteita, kuten syke ja munuaisten sympaattinen lähtö, baroretseptorin herkkyysmäärityksen päätepisteinä. Monimutkaiset kirurgiset toimenpiteet aiheuttavat kokeellisia virheitä, jotka voivat johtaa kiistanalaisiin johtopäätöksiin. Lisäksi eläinlajista riippuvainen vaihtelu baroreseptorin herkkyydessä on myös mahdollista. Lisäksi barorefleksivasteeseen eivät vaikuta pelkästään baroretseptorin herkkyys, vaan myös monet muut tekijät, kuten hermon johtuminen, keskeinen välitys, verisuonten supistuvuus ja sydämen toiminta. Siksi aiempien tutkimusten todisteet ovat epäsuoria ja tuskin ihanteellisia. Tähän asti ei ole suoria tutkimuksia, joissa verrataan aortan ja kaulavaltimon baroretseptorin hermosolujen paineherkkyyttä. Tässä tutkimuksessa mekaanista herkkyyttä tutkittiin suoraan baroreceptorihermoneissa. Tiedot viittaavat vahvasti siihen, että aortan baroretseptorit ovat herkempiä paineelle kuin kaulavaltimon baroretseptorit. Näillä tiedoilla voi olla tärkeä fysiologinen merkitys verenpaineen säätelyssä.
On epäselvää, mitkä mekanismit ovat aortan ja kaulavaltimon baroretseptoreiden paineherkkyyserojen taustalla. Verrattiin useiden mekaaniherkkien TRP-kanavien ilmentymistasoa (kuva 6) (O ”Neil ja Heller, 2005; Christensen ja Corey, 2007; Pedersen ja Nilius, 2007; Patel et ai., 2010). Tuloksemme osoittivat, että aortan baroreseptorihermot niillä on korkeampi ilmentyminen useista mekaanisesti herkistä TRP-kanavista, mukaan lukien TRPV4 ja TRPC6. On mahdollista, että korkeampi TRPV4: n ja / tai TRPC6: n ilmentyminen voi vaikuttaa aortan baroretseptorien korkeaan paineherkkyyteen. Lisätutkimuksia tarvitaan näiden ionikanavien roolin todentamiseksi.
Aiemmin ilmoitettiin, että nodoosiganglionissa ja petrosaaliranglionissa on kahta erityyppistä hermosolua (Belmonte ja Gallego, 1983), joista toinen antaa jatkuvaa toimintapotentiaalia sähköstimulaation yhteydessä, kun taas toinen antaa vain yhden toiminnan kirjoittajat määrittivät ensimmäisen paineherkiksi neuroneiksi ja jälkimmäiset kemoherkiksi neuroneiksi. Tuloksemme osoittavat, että se ei välttämättä ole sopiva Voit määrittää paineherkät neuronit ja paineherkät neuronit vain sen perusteella, laukaisevatko ne yksittäisen vai jatkuvan toimintapotentiaalin vasteena depolarisoivalle virralle. Itse asiassa suuri prosenttiosuus soluista, jotka sytyttävät yhden toimintapotentiaalin vastauksena sähköstimulaatioon, ovat myös herkkiä paineelle, ja siten ne kuuluvat paineentunnistaviin baroreceptorihermoneihin (kuva 2 ja taulukko 1).
Yhteenvetona voidaan todeta, että tämä tutkimus antaa todisteita siitä, että aortan baroretseptorit ovat herkempiä paineelle kuin kaulavaltimon baroretseptorit, ja lisää uutta tietoa perusfysiologian ymmärtämiseen.
Kirjoittajan panokset
EL ja XY suunnitella kokeet ja luonnos käsikirjoitus. EL, CL ja YY suorittavat kokeet. XY, YH, AM ja LJ tarkensivat käsikirjoitusta. Kaikki kirjoittajat hyväksyivät käsikirjoituksen lopullisen version.
Rahoitus
Tätä työtä tukivat Hongkongin tutkimusapurahakomitean apurahat CUHK478710, CUHK478413, AoE / M-05/12, TBRS / T13-706 / 11, Kiinan kansallisen tiedesäätiön apuraha 31470912 ja RGC-NSFC: n yhteisapuraha N_CUHK439 / 13.
Eturistiriita-ilmoitus
Kirjoittajat ilmoittavat tutkimuksen toteutuneen ilman kaupallisia tai taloudellisia suhteita, jotka voitaisiin tulkita mahdollisiksi eturistiriidoiksi.
James, JEA ja Daly, MDB (1970). Reflex-vasomotoristen reaktioiden vertailu kaulavaltimon ja aortan kaaren baroretseptoreiden erilliseen ja yhdistettyyn stimulointiin sykkivällä ja ei-pulsoivalla paineella koiralla. J. Physiol. 209, 257–293. doi: 10.1113 / jphysiol.1970.sp009165
PubMed-tiivistelmä | CrossRef-kokoteksti | Google Scholar
Levy MN, P. A. (2007). Sydän- ja verisuonifysiologia. Philadelphia, PA: Mosby Elsevier.
Vander, A. J., Sherman, J. H. ja Luciano, D. S. (1998). Ihmisen fysiologia: kehon toimintamekanismi. Boston, MA: WCB McGraw-Hill.