Molécule ATP
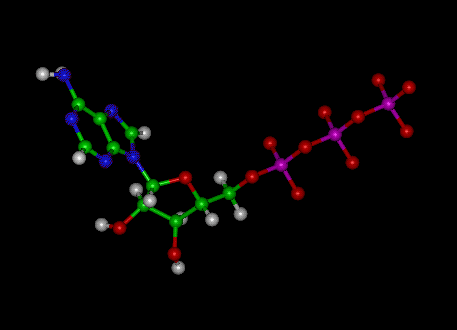
La molécule d’adénosine triphosphate (ATP) est le nucléotide connu en biochimie comme «monnaie moléculaire» du transfert d’énergie intracellulaire; autrement dit, l’ATP est capable de stocker et de transporter de l’énergie chimique dans les cellules. L’ATP joue également un rôle important dans la synthèse des acides nucléiques.
Pour la structure 3-D de cette image en utilisant JsmolCliquez ici
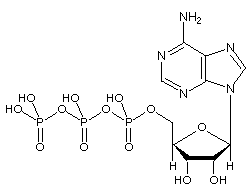
Image: Structure moléculaire de l’ATP
L’énergie est libérée par l’hydrolyse du troisième groupe phosphate. Après la libération de ce troisième groupe phosphate, l’ADP résultant (adénosine diphosphate) peut absorber de l’énergie et regagner le groupe, régénérant ainsi une molécule d’ATP; cela permet à l’ATP de stocker de l’énergie comme une batterie rechargeable.
Positions du phosphoryle
Les groupes phosphoryle commençant par celui sur AMP sont appelés phosphates alpha, bêta et gamma.
Propriétés physiques et chimiques
L’ATP se compose d’adénosine – composée d’un anneau adénine et d’un sucre ribose – et de trois groupes phosphate (triphosphate). Les groupes phosphoryle, en commençant par le groupe le plus proche du ribose, sont appelés phosphates alpha (α), bêta (β) et gamma (γ). Par conséquent, il est étroitement lié au nucléotide adénine, un monomère de l’ARN. L’ATP est très soluble dans l’eau et est assez stable dans les solutions entre pH 6,8 et 7,4, mais est rapidement hydrolysé à pH extrême. Par conséquent, l’ATP est mieux stocké sous forme de sel anhydre.
L’ATP est une molécule instable dans l’eau non tamponnée, dans laquelle il s’hydrolyse en ADP et phosphate. En effet, la force des liaisons entre les groupes phosphate dans l’ATP est inférieure à la force des liaisons hydrogène (liaisons d’hydratation), entre ses produits (ADP et phosphate) et l’eau. Ainsi, si l’ATP et l’ADP sont en équilibre chimique dans l’eau, la quasi-totalité de l’ATP sera finalement convertie en ADP. Un système qui est loin de l’équilibre contient de l’énergie libre de Gibbs et est capable de travailler. Les cellules vivantes maintiennent le rapport ATP / ADP à dix ordres de grandeur de l’équilibre, avec des concentrations d’ATP cinq fois plus élevées que la concentration d’ADP. Ce déplacement de l’équilibre signifie que l’hydrolyse de l’ATP dans la cellule libère une grande quantité d’énergie libre.
Deux liaisons phosphoanhydride (celles qui relient les phosphates adjacents) dans une molécule d’ATP sont responsables du contenu énergétique élevé de cette molécule. Dans le contexte des réactions biochimiques, ces liaisons anhydrides sont fréquemment – et parfois controversées – appelées liaisons à haute énergie (malgré le fait qu’il faut de l’énergie pour rompre les liaisons). L’énergie stockée dans l’ATP peut être libérée lors de l’hydrolyse des liaisons anhydride. Le groupe phosphate primaire sur la molécule d’ATP qui est hydrolysé lorsque l’énergie est nécessaire pour provoquer des réactions anaboliques est le groupe γ-phosphate. Situé le plus éloigné du sucre ribose, il a une énergie d’hydrolyse plus élevée que l’α ou le β-phosphate. Les liaisons formées après l’hydrolyse – ou la phosphorylation d’un résidu par l’ATP – sont plus faibles en énergie que les liaisons phosphoanhydride de l’ATP. Pendant l’hydrolyse catalysée par une enzyme de l’ATP ou la phosphorylation par l’ATP, l’énergie libre disponible peut être exploitée par un système vivant pour faire le travail.
Tout système instable de molécules potentiellement réactives pourrait potentiellement servir de moyen de stockage gratuit l’énergie, si la cellule maintenait sa concentration loin du point d’équilibre de la réaction. Cependant, comme c’est le cas avec la plupart des biomolécules polymères, la décomposition de l’ARN, de l’ADN et de l’ATP en monomères plus simples est motivée à la fois par des considérations de libération d’énergie et d’augmentation d’entropie, dans les deux concentrations standard, ainsi que les concentrations rencontrées dans la cellule.
La quantité standard d’énergie libérée par l’hydrolyse de l’ATP peut être calculée à partir des changements d’énergie dans des conditions non naturelles (standard), puis en corrigeant les concentrations biologiques. Le changement net d’énergie thermique (enthalpie) à température et pression standard de la décomposition de l’ATP en ADP hydraté et phosphate inorganique hydraté est de -30,5 kJ / mol, avec un changement d’énergie libre de 3,4 kJ / mol. L’énergie libérée par le clivage d’une unité phosphate (Pi) ou pyrophosphate (PPi) de l’ATP à l’état standard de 1 M est:
ATP + H
2O → ADP + Pi ΔG ° = −30,5 kJ / mol (−7,3 kcal / mol)
ATP + H
2O → AMP + PPi ΔG ° = −45,6 kJ / mol (−10,9 kcal / mol)
Ces valeurs peuvent être utilisé pour calculer le changement d’énergie dans des conditions physiologiques et le rapport ATP / ADP cellulaire. Cependant, une valeur plus représentative (qui prend en considération l’AMP) appelée charge d’énergie est de plus en plus utilisée. Les valeurs données pour l’énergie libre de Gibbs pour cette réaction dépendent d’un certain nombre de facteurs, y compris la force ionique globale et la présence d’ions de métaux alcalino-terreux tels que Mg2 +
et Ca2 +
.Dans des conditions cellulaires typiques, ΔG est d’environ -57 kJ / mol (-14 kcal / mol).
Synthèse
L’ATP peut être produit par divers processus cellulaires, le plus souvent dans les mitochondries par phosphorylation oxydative sous l’influence catalytique de l’ATP synthase ou dans le cas des plantes en chloroplastes par photosynthèse.
Les principaux carburants pour la synthèse de l’ATP sont le glucose et les acides gras. Initialement, le glucose est décomposé en pyruvate dans le cytosol. Deux molécules d’ATP sont générées pour chaque molécule de glucose. Les étapes terminales de la synthèse d’ATP sont effectuées dans la mitochondrie et peuvent générer jusqu’à 34 ATP.
ATP dans le corps humain
La quantité totale d’ATP dans le corps humain est d’environ 0,1 mole. L’énergie consommée quotidiennement par un adulte nécessite l’hydrolyse de 200 à 300 moles d’ATP. Cela signifie que chaque molécule d’ATP doit être recyclée de 2000 à 3000 fois par jour. L’ATP ne peut pas être stocké et sa synthèse doit donc suivre de près sa consommation.
D’autres triphosphates
Les cellules vivantes ont également d’autres nucléosides triphosphates «à haute énergie», comme le guanine triphosphate. Entre eux et l’ATP, l’énergie peut être facilement transférée avec des réactions telles que celles catalysées par la nucléoside diphosphokinase: de l’énergie est libérée lors de l’hydrolyse des liaisons phosphate-phosphate. Cette énergie peut être utilisée par une variété d’enzymes, de protéines motrices et de protéines de transport pour effectuer le travail de la cellule. De plus, l’hydrolyse produit du phosphate inorganique libre et de l’adénosine diphosphate, qui peuvent être décomposés en un autre ion phosphate et en adénosine monophosphate. L’ATP peut également être décomposé en adénosine monophosphate directement, avec la formation de pyrophosphate. Cette dernière réaction a l’avantage d’être un processus effectivement irréversible en solution aqueuse.
Réaction de l’ADP avec le GTP
ADP + GTP > ATP + GDP