ATP分子
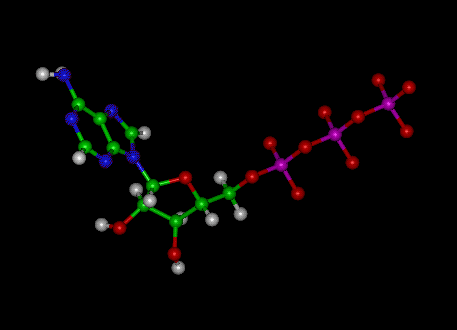
アデノシン三リン酸(ATP)分子は既知のヌクレオチドです細胞内エネルギー伝達の「分子通貨」としての生化学。つまり、ATPは細胞内で化学エネルギーを貯蔵および輸送することができます。 ATPは核酸の合成にも重要な役割を果たします。
Jsmolを使用したこの画像の3D構造についてはここをクリック
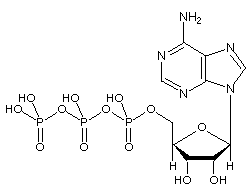
画像:ATPの分子構造
エネルギーは、3番目のリン酸基の加水分解によって放出されます。この3番目のリン酸基が放出された後、結果として生じるADP(アデノシン二リン酸)はエネルギーを吸収して基を取り戻し、ATP分子を再生します。これにより、ATPは充電式電池のようにエネルギーを蓄えることができます。
リン酸の位置
AMPのリン酸基で始まるリン酸基は、アルファ、ベータ、ガンマリン酸と呼ばれます。
物理的および化学的特性
ATPは、アデノシン(アデニン環とリボース糖で構成される)と3つのリン酸基(三リン酸)で構成されています。リボースに最も近い基から始まるホスホリル基は、アルファ(α)、ベータ(β)、およびガンマ(γ)リン酸と呼ばれる。その結果、RNAのモノマーであるアデニンヌクレオチドと密接に関連しています。 ATPは水に非常に溶けやすく、pH 6.8〜7.4の溶液では非常に安定していますが、極端なpHでは急速に加水分解されます。したがって、ATPは無水塩として保存するのが最適です。
ATPは、緩衝されていない水中では不安定な分子であり、ADPとリン酸塩に加水分解されます。これは、ATPのリン酸基間の結合の強度が、その生成物(ADPとリン酸)と水の間の水素結合(水和結合)の強度よりも弱いためです。したがって、ATPとADPが水中で化学平衡にある場合、ほとんどすべてのATPが最終的にADPに変換されます。平衡状態からかけ離れたシステムにはギブズの自由エネルギーが含まれており、仕事をすることができます。生細胞は、ATPとADPの比率を平衡状態から10桁維持し、ATP濃度はADPの濃度の5倍になります。この平衡状態からのずれは、細胞内のATPの加水分解が大量の自由エネルギーを放出することを意味します。
ATP分子内の2つのリン酸無水物結合(隣接するリン酸を接続する結合)が、この分子。生化学反応の文脈では、これらの無水物結合は、しばしば(そして時には物議を醸すように)高エネルギー結合と呼ばれます(結合を切断するのにエネルギーが必要であるという事実にもかかわらず)。 ATPに蓄積されたエネルギーは、無水物結合の加水分解時に放出される可能性があります。同化反応を促進するためにエネルギーが必要なときに加水分解されるATP分子の主要なリン酸基はγ-リン酸基です。リボース糖から最も遠い位置にあり、α-またはβ-リン酸よりも高い加水分解エネルギーを持っています。加水分解後に形成される結合、またはATPによる残基のリン酸化は、ATPのホスホ無水物結合よりもエネルギーが低くなります。 ATPの酵素触媒による加水分解またはATPによるリン酸化の際、利用可能な自由エネルギーを生体システムで利用して作業を行うことができます。
潜在的に反応性の分子の不安定なシステムは、自由エネルギーを保存する方法として役立つ可能性がありますセルが反応の平衡点から遠く離れた濃度を維持した場合、エネルギー。ただし、ほとんどの高分子生体分子の場合と同様に、RNA、DNA、およびATPのより単純なモノマーへの分解は、標準濃度と細胞内で遭遇する濃度の両方で、エネルギー放出とエントロピー増加の両方の考慮事項によって促進されます。
ATPの加水分解から放出されるエネルギーの標準量は、非天然(標準)条件下でのエネルギーの変化から計算し、生体濃度に補正することができます。 ATPの水和ADPと水和無機リン酸塩への分解の標準温度と圧力での熱エネルギー(エンタルピー)の正味の変化は-30.5 kJ / molであり、自由エネルギーの変化は3.4 kJ / molです。 1 Mの標準状態でATPからリン酸(Pi)またはピロリン酸(PPi)ユニットを切断することによって放出されるエネルギーは、次のとおりです。
ATP + H
2O→ADP +PiΔG°= -30.5 kJ / mol(-7.3 kcal / mol)
ATP + H
2O→AMP +PPiΔG°= -45.6 kJ / mol(-10.9 kcal / mol)
これらの値は次のようになります。生理学的条件下でのエネルギーの変化と細胞のATP / ADP比を計算するために使用されます。ただし、エネルギーチャージと呼ばれるより代表的な値(AMPを考慮)がますます採用されています。この反応のギブズの自由エネルギーに与えられた値は、全体的なイオン強度や、Mg2 +
やCa2 +
などのアルカリ土類金属イオンの存在などの多くの要因に依存します。典型的な細胞条件下では、ΔGは約-57 kJ / mol(-14 kcal / mol)です。
合成
ATPは、さまざまな細胞プロセスによって、最も一般的にはミトコンドリアで生成されます。 ATP合成酵素の触媒作用下での酸化的リン酸化、または光合成による葉緑体の植物の場合。
ATP合成の主な燃料はグルコースと脂肪酸です。最初に、グルコースは細胞質ゾルでピルビン酸に分解されます。グルコースの各分子に対して2分子のATPが生成されます。 ATP合成の最終段階はミトコンドリアで行われ、最大34個のATPを生成することができます。
人体のATP
人体のATPの総量は約0.1モル。成人が毎日使用するエネルギーは、200から300モルのATPの加水分解を必要とします。これは、各ATP分子が1日に2000〜3000回リサイクルされる必要があることを意味します。 ATPは保存できないため、その合成はその消費に厳密に従う必要があります。
他の三リン酸
生細胞には、グアニン三リン酸などの他の「高エネルギー」ヌクレオシド三リン酸もあります。それらとATPの間では、ヌクレオシドジホスホキナーゼによって触媒されるような反応でエネルギーを簡単に伝達できます。リン酸-リン酸結合の加水分解が行われると、エネルギーが放出されます。このエネルギーは、細胞の働きを実行するために、さまざまな酵素、モータータンパク質、および輸送タンパク質によって使用されます。また、加水分解により遊離の無機リン酸とアデノシン二リン酸が生成され、さらに別のリン酸イオンとアデノシン一リン酸に分解されます。 ATPは、ピロリン酸を形成して、アデノシン一リン酸に直接分解することもできます。この最後の反応には、水溶液中で効果的に不可逆的なプロセスであるという利点があります。
ADPとGTPの反応
ADP + GTP > ATP + GDP