物理的地質学
地球の地殻の岩石を構成する鉱物の大部分は、ケイ酸塩鉱物です。これらには、石英、長石、雲母、角閃石、輝石、かんらん石などの鉱物、および多種多様な粘土鉱物が含まれます。これらすべての鉱物の構成要素は、4つの酸素原子と1つのシリコン原子の組み合わせであるシリカ四面体です。これらは、酸素原子を介して描かれた平面が四面体を形成するように配置されています(図2.6)。シリコンイオンの電荷は+4で、4つの酸素イオンの電荷はそれぞれ–2であるため、シリカ四面体の正味電荷は–4です。
ケイ酸塩鉱物では、これらの四面体が配置されます。単一のユニットから複雑なフレームワークまで、さまざまな方法で相互にリンクされます(図2.9)。最も単純なケイ酸塩構造である鉱物かんらん石の構造は、鉄および/またはマグネシウムイオンに結合した孤立した四面体で構成されています。かんらん石では、各シリカ四面体の–4電荷は、2つの2価(つまり、+ 2)の鉄またはマグネシウムカチオンによってバランスがとられています。かんらん石は、Mg2SiO4またはFe2SiO4のいずれか、あるいは2つの(Mg、Fe)2SiO4の組み合わせにすることができます。マグネシウムと鉄の二価陽イオンは半径が非常に近い(0.73オングストローム対0.62オングストローム)。このサイズの類似性と、両方とも2価の陽イオン(両方とも+2の電荷を持つ)であるため、鉄とマグネシウムは、かんらん石や他の多くの鉱物で互いに容易に置換できます。
| 四面体構成 | 鉱物の例 | |
|---|---|---|
 |
分離(ネソ珪酸塩) | オリビン、ガーネット、ジルコン、キアナイト |
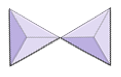 |
ペア(ソロシリケート) | エピドート、ゾイサイト |
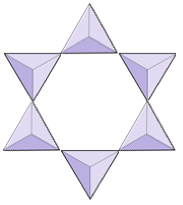 |
リング(シクロシリケート) | トルマリン |
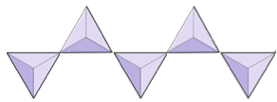 |
単鎖(イノシリケート) | 輝石、ウォラストナイト |
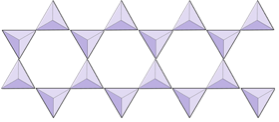 |
二重鎖(イノシリケート) | 角閃石 |
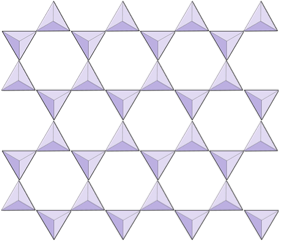 |
シート(フィロケイ酸塩) | 雲母、粘土鉱物、蛇紋石、緑簾石 |
| 3次元構造 | フレームワーク(テクトシリケート) | フェルドスパー、石英、ゼオライト |
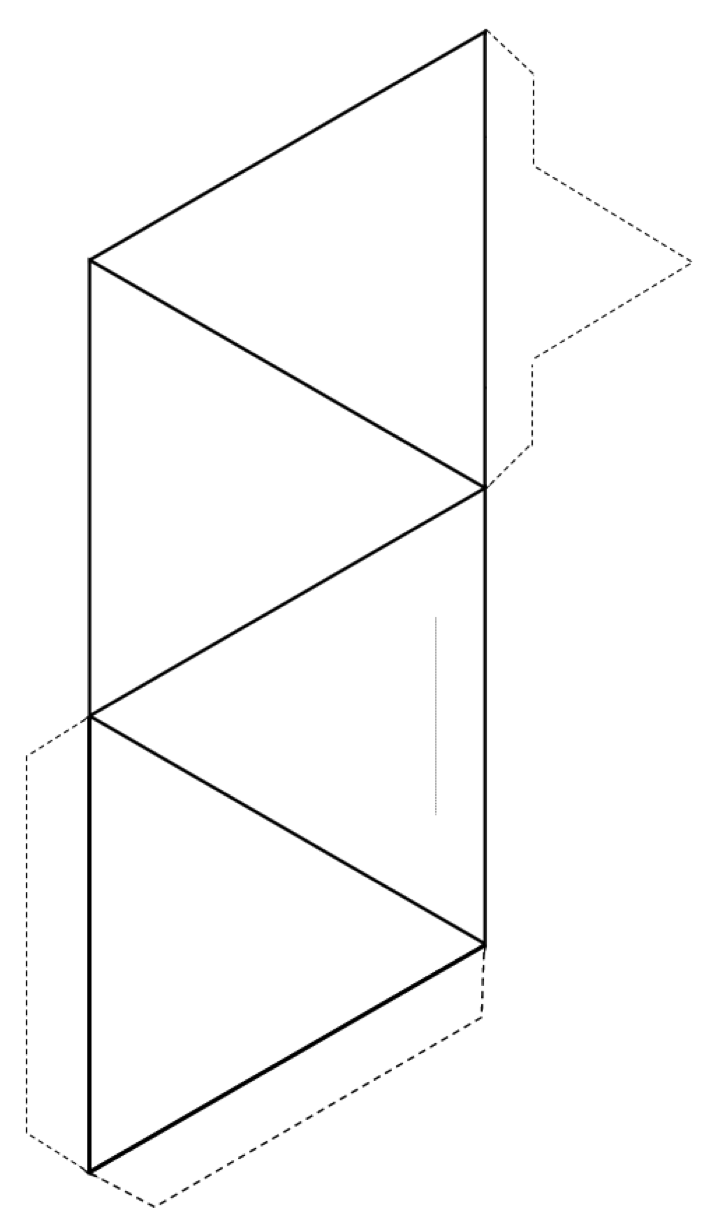
演習2.3四面体を作成する
形状の外側(実線と点線)を切り取り、実線に沿って折りたたんで四面体を形成します。
接着剤またはテープがある場合は、四面体にタブで固定します。接着剤やテープがない場合は、細い灰色の線に沿ってスライスを作成し、先のとがったタブをスリットに挿入します。
教室でこれを行う場合は、四面体を他の人と結合してみてください。ペア、リング、一本鎖および二本鎖、シート、さらには3次元フレームワーク。
他のほとんどのケイ酸塩鉱物とは異なり、かんらん石では、シリカ四面体はそれぞれに結合していません。その他。ただし、図2.10に示すように、鉄やマグネシウムに結合しています。
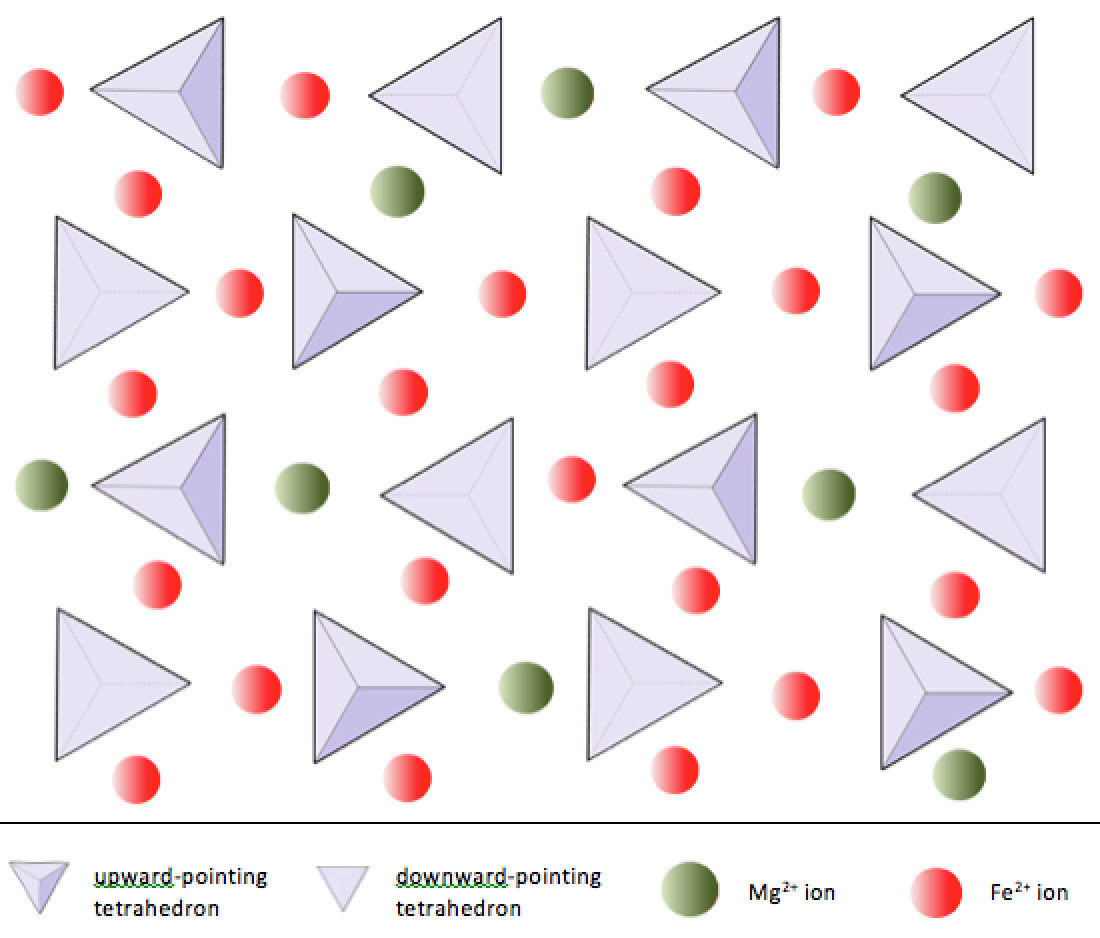
すでに述べたように、鉄とマグネシウムの+2イオンはサイズが似ています(完全に同じではありませんが)。これにより、一部のケイ酸塩鉱物で互いに代替することができます。実際、図2.11に示すように、ケイ酸塩鉱物の一般的なイオンのサイズはさまざまです。示されているイオンはすべて、酸素を除いて陽イオンです。鉄は、+ 2イオン(イオン化中に2つの電子を失う場合)または+3イオン(3つを失う場合)の両方として存在する可能性があることに注意してください。 Fe2 +は第一鉄として知られています。 Fe3 +は第二鉄として知られています。イオン半径はケイ酸塩鉱物の組成にとって重要であるため、この図を再度参照します。

単鎖の構造ケイ酸塩輝石を図2.12および2.13に示します。輝石では、シリカ四面体が1本の鎖で結合され、各四面体からの1つの酸素イオンが隣接する四面体と共有されるため、構造内の酸素が少なくなります。その結果、必要な陽イオンが少なくなるため、酸素とシリコンの比率がかんらん石よりも低くなり(4:1ではなく3:1)、シリコン原子あたりの正味電荷が少なくなります(–4ではなく–2)。その料金のバランスを取るために。輝石組成は、MgSiO3、FeSiO3、CaSiO3、またはこれらの組み合わせのタイプです。輝石は(Mg、Fe、Ca)SiO3と書くこともでき、括弧内の元素は任意の比率で存在できます。言い換えると、輝石はシリカ四面体(MgSiO3など)ごとに1つの陽イオンを持ち、かんらん石は2つ(Mg2SiO4など)を持ちます。各シリコンイオンは+4で、各酸素イオンは–2であるため、3つの酸素(–6)と1つのシリコン(+4)は、シリカ四面体の単鎖に対して–2の正味電荷を与えます。輝石では、四面体あたり1つの二価陽イオン(2+)がその–2電荷のバランスを取ります。かんらん石では、孤立した四面体の–4電荷のバランスをとるのに2価の陽イオンが必要です。
輝石の構造はかんらん石よりも「許容」的です。つまり、イオン半径の範囲が広い陽イオンです。輝石は鉄(半径0.63Å)またはマグネシウム(半径0.72Å)またはカルシウム(半径1.00Å)の陽イオンを持つことができるのはそのためです。
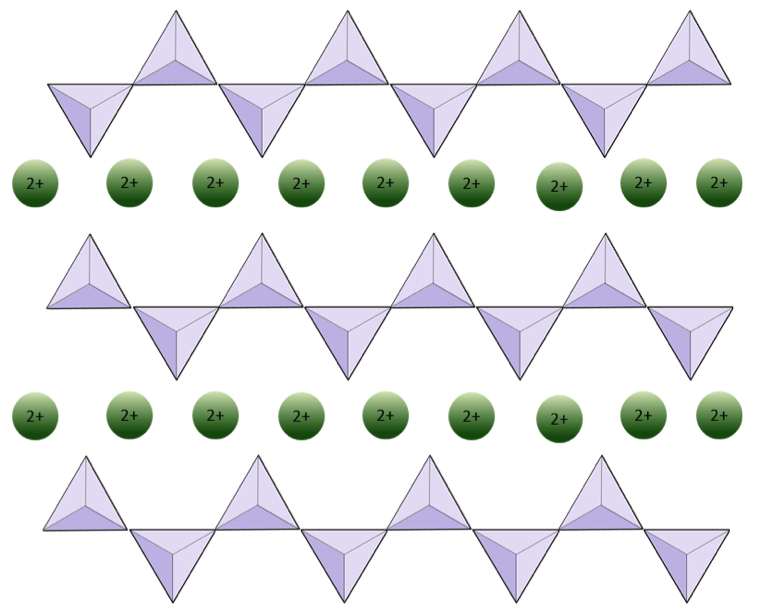
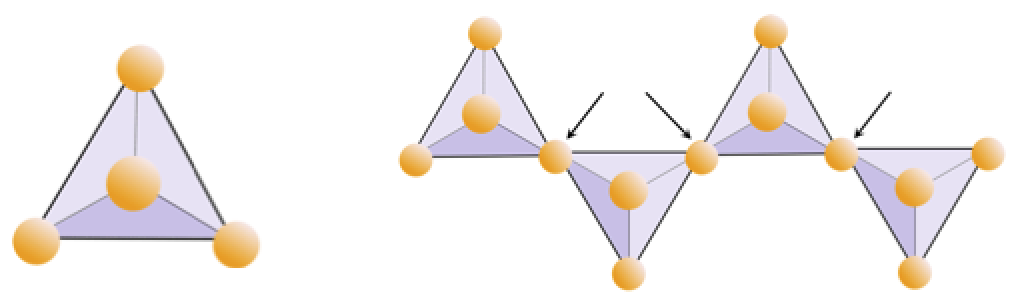
演習2.4酸素欠乏
下の図は、ケイ酸塩鉱物の単鎖を表しています。四面体の数と酸素イオン(黄色の球)の数を数えます。各四面体には1つのシリコンイオンがあるため、単鎖ケイ酸塩(輝石など)のSiとOの比率がわかります。
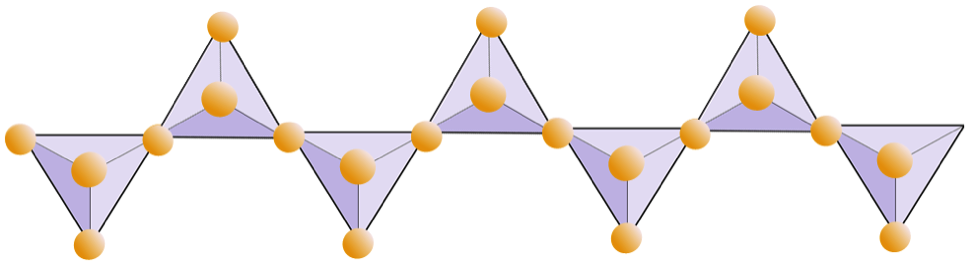
下の図は、ケイ酸塩鉱物の二本鎖を表しています。ここでも、四面体の数と酸素イオンの数を数えます。これにより、二本鎖ケイ酸塩(角閃石など)のSiとOの比率がわかります。
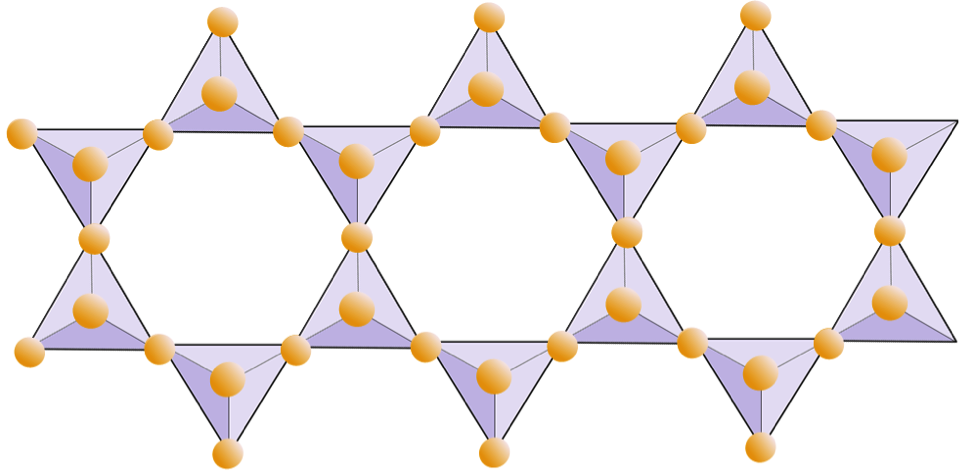
角閃石構造では、シリカ四面体は輝石よりも酸素とシリコンの比率が低い二本鎖で結合しているため、電荷のバランスを取るために必要なカチオンはさらに少なくなります。角閃石は輝石よりもさらに寛容であり、その組成は非常に複雑になる可能性があります。たとえば、角閃石には、ナトリウム、カリウム、カルシウム、マグネシウム、鉄、アルミニウム、シリコン、酸素、フッ素、およびヒドロキシルイオン(OH–)が含まれます。
雲母構造では、シリカ四面体は連続シートに配置され、各四面体は隣接する四面体と3つの酸素アニオンを共有します。隣接する四面体間での酸素の共有がさらに多くなるため、シート状ケイ酸塩鉱物に必要な電荷平衡カチオンが少なくなります。シート間の結合は比較的弱く、これはよく発達した一方向の劈開を説明します(図2.14)。黒雲母雲母には鉄やマグネシウムが含まれている可能性があり、それによって鉄マグネシアケイ酸塩鉱物(かんらん石、輝石、角閃石など)になります。緑泥石は、一般的にマグネシウムを含む別の同様の鉱物です。白雲母雲母では、存在する陽イオンはアルミニウムとカリウムだけです。したがって、それは非強磁性ケイ酸塩鉱物です。

白雲母、黒雲母、緑泥石以外にも、シート状ケイ酸塩(またはフィロケイ酸塩)がたくさんあります。通常、粘土サイズの破片(つまり、0.004 mm未満)として存在します。これらには、粘土鉱物のカオリナイト、イライト、スメクタイトが含まれ、サイズが非常に小さいため研究は困難ですが、岩石、特に土壌の非常に重要な成分です。
すべてのシートケイ酸塩鉱物の構造にも水が含まれています。
シリカ四面体は、長石と石英の両方で3次元のフレームワークに結合されています。これらは非強磁性鉱物であり、鉄やマグネシウムは含まれていません。長石には、シリカ四面体に加えて、陽イオンであるアルミニウム、カリウム、ナトリウム、カルシウムがさまざまな組み合わせで含まれています。石英にはシリカ四面体のみが含まれています。
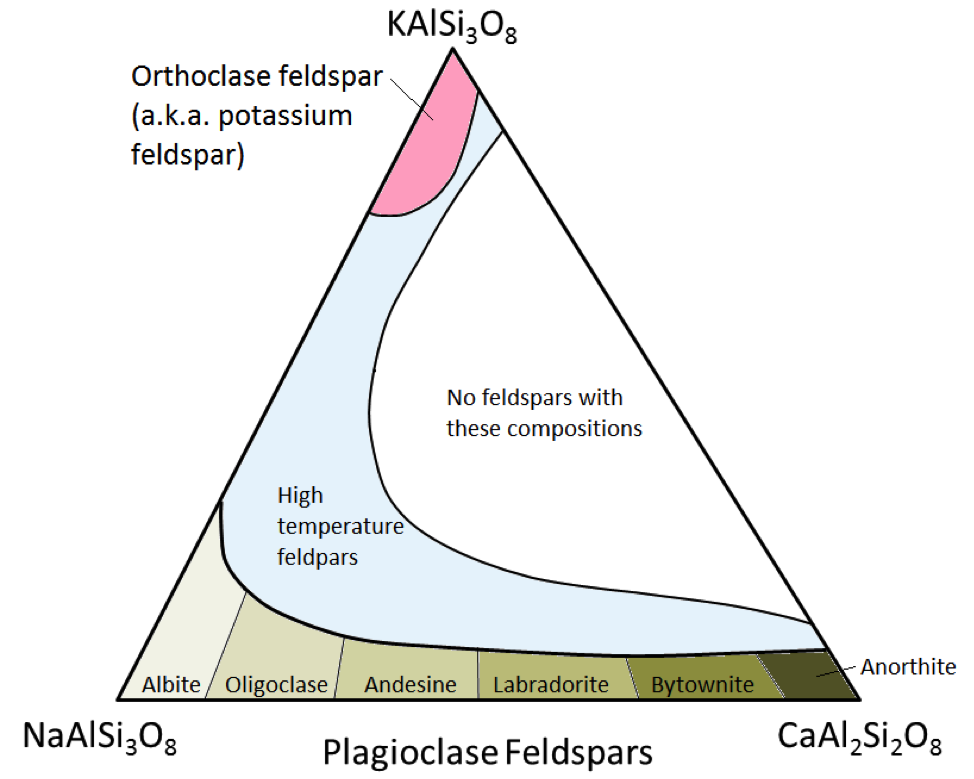
3つの主要な長石鉱物はカリウム長石(別名K長石またはK長石)と2種類の斜長石長石です:曹長石(ナトリウムのみ)と灰長石(カルシウムのみ) 。かんらん石中の鉄とマグネシウムの場合と同様に、斜長石中の曹長石と灰長石の間には連続した範囲の組成(固溶体系列)があります。これは、カルシウムイオンとナトリウムイオンのサイズがほぼ同じであるためです(1.00Åと0.99Å)。 CaAl2Si3O8とNaAlSi3O8の間の任意の中間組成が存在する可能性があります(図2.15)。サイズは非常に似ていますが、カルシウムイオンとナトリウムイオンの電荷は同じではないため(Ca2 +とNa +)、これは少し驚くべきことです。この問題は、Si4 +の代わりにAl3 +を使用することで説明されます。したがって、曹長石はNaAlSi3O8(1つのAlと3つのSi)であり、灰長石はCaAl2Si2O8(2つのAlと2つのSi)であり、中間組成の斜長石長石は中間の比率のAlとSiを持っています。これは「結合置換」と呼ばれます。
中性斜長石長石は、オリゴクレース(10%〜30%Ca)、アンデシン(30%〜50%Ca)、ラブラドライト(50%〜70)です。 %Ca)、およびバイタウンナイト(70%〜90%Ca)。K長石(KAlSi3O8)は、カリウムイオンのサイズが大きい(1.37Å)ため、またこのサイズが大きいため、斜長石とは構造がわずかに異なります。 、カルシウムとナトリウムは、高温を除いて、互いに容易に置き換わるものではありません。これらの高温の長石は、長石がいずれかに変化するのに十分なほどゆっくりと低温になるため、火山岩にのみ見られる可能性があります。低温フォーム。
カルシウム(SiO2)では、シリカ四面体が「完全な」3次元フレームワークで結合されています。各四面体は他の4つの四面体に結合され(各四面体の隅々で酸素が共有されます)、その結果、シリコンと酸素の比率は1:2になります。 1つのシリコンカチオンには+4の電荷があり、2つの酸素アニオンにはそれぞれ-2の電荷があるため、電荷のバランスが取れています。アルミニウムやナトリウムやカリウムなどの他の陽イオンは必要ありません。クォーツの硬度と劈開の欠如は、シリカ四面体に特徴的な強い共有結合/イオン結合に起因します。
演習2.5フェロマグネシアンシリケート?
ケイ酸塩鉱物は、化学式に鉄(Fe)やマグネシウム(Mg)が含まれているかどうかに応じて、フェロマグネシアンまたは非フェロマグネシアンに分類されます。いくつかのミネラルとその処方を以下に示します。それぞれについて、それが輝石ケイ酸塩であるかどうかを示します。
| ミネラル | 式 | フェロマグネシアンケイ酸塩? |
|---|---|---|
| オリビン | (Mg、Fe)2SiO4 | |
| パイライト | FeS2 | |
| 斜長石 | CaAl2Si2O8 | |
| 輝石 | MgSiO3 | |
| ヘマタイト | Fe2O3 | |
| 正長石 | KAlSi3O8 | |
| クォーツ | SiO2 |
| ミネラル | 式* | フェロマグネシアンケイ酸塩? |
|---|---|---|
| 両生類 | Fe7Si8O22(OH)2 | |
| ムスコバイト | K2Al4 Si6Al2O20(OH)4 | |
| マグネタイト | Fe3O4 | |
| biotite | K2Fe4Al2Si6Al4O20(OH)4 | |
| ドロマイト | (Ca、Mg)CO3 | |
| ガーネット | Fe2Al2Si3O12 | |
| 蛇紋岩 | Mg3Si2O5(OH)4 |
*一部の式、特により複雑な式は簡略化されています。
- オングストロームは、原子の表現に一般的に使用される単位です。 -スケール寸法。 1オングストロームは10〜10mまたは0.0000000001mです。オングストロームの記号はÅです。 ↵