Francium 요소 정보
화학 원소 프랑슘은 알칼리 금속으로 분류됩니다. 1939 년에 Marguerite Perey가 발견했습니다.

데이터 영역
| 분류 : | 프랑슘 알칼리 금속입니다. |
| 색상 : | 은회색-금속 (추정) |
| 원자 무게 : | (223), 안정 동위 원소 없음 |
| 상태 : | 고체 |
| 녹는 점 : | 27 oC, 300 K |
| 끓는점 : | 677 oC, 950 K |
| 전자 : | 87 |
| 양성자 : | 87 |
| 가장 풍부한 동위 원소의 중성자 : | 136 |
| 전자 껍질 : | 2, 8,18,32,18,8,1 |
| 전자 구성 : | 7s1 |
| 밀도 @ 20oC : | 1.873 g / cm3 |
다음을 포함하여 더보기 : 열, 에너지, 산화,
반응, 화합물, 반경, 전도도
| 원자 부피 : | 71.07 cm3 / mol |
| 구조 : | 숨은 참조로 간주 : 신체 중심 입방체 |
| 경도 : | – |
| 비열 용량 | – |
| 융해열 | 2 kJ mol-1 |
| 무화 열 | 73 kJ mol-1 |
| 기화열 | 64kJ mol-1 |
| 1 차 이온화 에너지 | 384kJ mol-1 |
| 2 차 이온화 에너지 | – |
| 3 차 이온화 에너지 | – |
| 전자 친 화성 | – |
| 최소 산화수 | 0 |
| 최소 일반적인 산화 번호 | 0 |
| 최대 산화 수 | 1 |
| 최대. 일반적인 산화 번호. | 1 |
| 전기 음성도 (폴링 스케일) | 0.7 |
| 분 극성 부피 | 48.7 Å3 |
| 공기와의 반응 | – |
| 반응 15M HNO3로 | – |
| 6M HCl과의 반응 | 격렬함, ⇒ H2, FrCl |
| 6M NaOH와의 반응 | 격렬함, ⇒ H2, FrOH |
| 산화물 | – |
| 수 소화물 | – |
| 염화물 | – |
| 원자 반경 | – |
| 이온 반경 (1+ 이온) | 194 pm |
| 이온 반경 (2+ 이온) | – |
| 이온 반경 (3+ 이온) | – |
| 이온 반경 (1- 이온) | – |
| 이온 반경 (2- 이온) | – |
| 이온 반경 (3- 이온) | – |
| 열전도율 | 3.61W m-1 K-1 |
| 전기 전도도 | – |
| 어는점 / 어는점 : | 27 oC, 300K |

이 우라늄 광석 샘플에는 약 100,000 개의 프랑슘 -223 원자 (3.3 x 10-20g)가 포함되어 있습니다. 프랑슘은 방사능입니다. 주어진 시간에 지구상에는 30g 미만이 존재합니다. 이미지 참조. (1)
프랜시 움 발견
Francium은 1939 년 Marguerite Perey가 악티늄 -227의 방사성 붕괴를 연구 할 때 발견했습니다.
이 발견은 파리의 퀴리 연구소에서 이루어졌습니다. 이 원소는 발견 된 국가 인 프랑스에서 이름을 따 왔습니다.
이 발견은 1935 년 Perey가 26 세의 나이에 미국 과학자들이 악티늄에 의해 방출되는 베타 입자를 발견했다고 주장하는 연구 논문을 읽었습니다. 평상시보다 더 많은 에너지를 가졌습니다.
Perey는이 발견에 대해 궁금해했고 이미 악티늄 관련 작업의 전문가로서 악티늄에 대한 자신의 실험을 수행하기로 결정했습니다. 그녀는 초순수 악티늄 샘플을 생산하고 그 방사선을 연구했습니다. Perey는 악티늄 방사능의 약 1 %가 베타 입자가 아닌 알파 입자를 방출하기 때문에 발생한다는 것을 발견했습니다.
Perey는 악티늄 -227이 헬륨 핵 (알파 입자라고도 함)을 방출하여 붕괴 될 수 있음을 발견했습니다. 자체 핵. 형성된 딸 핵은 이전에 발견되지 않은 원소로, 그녀가 고국 인 프랑스를 기념하기 위해 프랑슘이라고 부르기로 선택했습니다.
227Ac → 223Fr + 4He
87 개의 양성자를 가진 새로운 원소는 속했습니다. 다른 5 개의 알칼리 금속 인 리튬, 나트륨, 칼륨, 루비듐 및 세슘을 결합하는 주기율표의 그룹 1.
프랑슘의 발견은 자연적으로 발생하는 요소에 대한 인류의 발견을 완료했습니다.
그 이후 발견 된 모든 요소는 그 요소가 실험실에서 생산되었을 때 발견되었습니다.

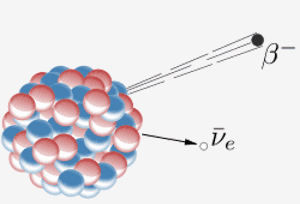
핵은 베타 입자 ( 전자) 및 항 중성미자. 그 결과 핵의 중성자가 양성자로 변합니다. 주기율표 (프란 슘)의 87 번 원소가이를 수행 할 때 여분의 양성자는 원소 88 (라듐)이된다는 것을 의미합니다.
Appearance 및 특성
유해 영향 :
프랑슘은 방사능이 매우 높습니다.
특성 :
프랑슘은 최대 반감기는 22 분입니다. 녹는 점이 낮고 (27oC, 81oF) 충분히 축적 될 수 있다면 따뜻한 방에서 액체가 될 것입니다.
프랑슘은 지각에서 두 번째로 희귀 한 원소입니다. 아스타틴 옆에. 주어진 시간에 지구상에 존재하는 프랑슘은 30g 미만입니다.
프랑슘은 모든 원소 중 전기 음성이 가장 적으므로 가장 화학적으로 반응성이 높은 알칼리 금속이어야합니다. 안타깝게도 물과 반응하는 것을 보여주기에는 충분한 양이 없습니다. 입자 가속기에서 소량으로 만들어집니다. 이론적으로 물과의 반응은 세슘보다 더 강력하고 나트륨보다 훨씬 더 폭력적입니다.
프랑슘은 가장 최근에 뉴욕의 스토니 브룩 대학교에서 연구되었습니다. 그곳의 과학자들은 특성을 측정하기 위해 자기장에서 레이저 빔을 사용하여 한 번에 최대 10,000 개의 프랑슘 원자를 가두 었습니다.
프랜 슘 사용
상업적으로 프랑슘은 희귀 성과 불안정성으로 인해 사용되지 않습니다. 연구 목적으로 만 사용됩니다.
Francium Decay
Francium의 동위 원소는 질량 수가 200에서 232까지이며 가장 일반적으로 알파 또는 베타 붕괴를 겪습니다.
다음은 프랑슘 붕괴 경로의 몇 가지 예입니다.
프랑슘 -223은 원소에서 가장 오래 살았던 동위 원소입니다. 반감기는 22 분입니다. 알파 입자 (헬륨 핵)를 방출하여 아스타틴 -219를 형성하거나 베타 입자를 방출하여 라듐 -223을 형성 할 수 있습니다. (베타 입자는 중성자가 양성자로 전환 될 때 핵에서 방출되는 전자입니다.)
Francium-221은 반감기가 5 분입니다. 알파 입자를 방출하여 아스타틴 -217을 형성하거나 베타 입자를 방출하여 라듐 -221이 될 수 있습니다.
Francium-216은 반감기가 0.7 마이크로 초입니다. 알파 입자를 방출하여 아스타틴 -212를 형성하거나 양전자를 방출하여 라돈 -216을 형성 할 수 있습니다.
Francium-212의 반감기는 19 분입니다. 알파 입자를 방출하여 아스타틴 -208을 형성하거나 궤도 전자를 포획하여 라돈 -212를 형성 할 수 있습니다. (2) (궤도 전자 포획 중에 핵은 원자 자체의 전자 중 하나를 포획하고 중성미자를 방출합니다.)
풍부와 동위 원소
풍부한 지각 : ~ 0ppm , ~ 0ppm
풍부한 태양계 : ~ 0ppm (중량 기준), ~ 0ppm (mol 기준)
비용, 순수 : 100g 당 $
비용, 부피 : 100g 당 $
출처 : 프랑슘은 악티늄의 알파 방사성 붕괴의 결과로 자연적으로 발생합니다.
동위 원소 : 프랑슘에는 33 개의 동위 원소가 있으며 반감기가 있습니다. 질량 번호는 200 ~ 232로 알려져 있습니다. 223Fr은 21.8 분으로 가장 긴 반감기를가집니다.

- Konrad Roeder의 사진
- EK 하이드, a. Ghiorso, G.T. Seaborg, Physical Review., 1950, 77, p765, Issue 6.
이 페이지 인용
온라인 링크의 경우 다음 중 하나를 복사하여 붙여 넣으십시오.
<a href="https://www.chemicool.com/elements/francium.html">Francium</a>
또는
<a href="https://www.chemicool.com/elements/francium.html">Francium Element Facts</a>
학술 문서에서이 페이지를 인용하려면 다음 MLA 준수 인용 :
"Francium." Chemicool Periodic Table. Chemicool.com. 11 Jan. 2015. Web. <https://www.chemicool.com/elements/francium.html>.