Kostengünstige Analyse der Verwendung von hochfrequenter Brustwandoszillation (HFCWO) bei Patienten mit nicht zystischer Fibrose-Bronchiektasie
Zusammenfassung
Bronchiektasie ist eine chronisch fortschreitende Krankheit, die durch eine irreversible pathologische Erweiterung der Lungenbronchien gekennzeichnet ist. Behandlungen für Bronchiektasen zielen darauf ab, Atemwegssekrete zu mobilisieren, Entzündungen zu reduzieren, Infektionen der Atemwege zu verhindern, die Beatmung zu verbessern, die Anzahl der Exazerbationen zu minimieren und die Lebensqualität einer Person zu verbessern. Die hochfrequente Brustwandoszillation (HFCWO) ist eine Behandlung zur Atemwegsfreigabe, die derzeit bei einer Reihe chronischer Atemwegserkrankungen angewendet wird, die die Bronchiektasie bei nicht zystischer Fibrose beeinträchtigen. In dieser Studie wurden die wirtschaftlichen Auswirkungen der HFCWO-Behandlung durch das SmartVest® Airway Clearance System auf die Inanspruchnahme und die Kosten der Gesundheitsversorgung im Zusammenhang mit Bronchiektasen bewertet.
Methoden
Die Ergebnisse eines zuvor veröffentlichten Fallüberprüfungsergebnisses Eine klinische Studie der Autoren bildete die Grundlage für diese Kosten-Nutzen-Analyse. Bronchiektasie-bedingte Exazerbationen, einschließlich der Anzahl der Krankenhausaufenthalte, Besuche in der Notaufnahme (ED) und der Häufigkeit von Antibiotika-Verschreibungen, wurden für jeden Patienten für einen Zeitraum von einem Jahr vor der Anwendung von SmartVest (Standard der Pflegekontrolle) und für einen Zeitraum von einem Jahr nach dem Start von SmartVest aufgezeichnet benutzen. Die Exazerbationsraten für ein Jahr vor SmartVest und ein Jahr nach SmartVest wurden verglichen. Exazerbationen wurden sowohl aus den Krankenakten des Patienten als auch per Telefoninterview überprüft. Die Antibiotikakosten wurden unter Verwendung der „Online-Preisgestaltung für Apothekenrabatte“ ermittelt, während die Kosten für Krankenhausaufenthalte und ED unter Verwendung des Statistical Brief # 146 des Healthcare Cost and Utilization Project (HCUP) und der NIS-Datenbank 2013 (HCUP National Inpatient Sample) ermittelt wurden
Ergebnisse
Die zuvor veröffentlichten klinischen Ergebnisse von neunundfünfzig SmartVest-Patienten mit nicht-zystischer Fibrose-Bronchiektasie dienten als Grundlage für diese Analyse. Bei der Analyse der Ergebnisdaten wurde SmartVest im Vergleich zum Standard verwendet der Pflegekontrolle war mit statistisch signifikanten Ergebnissen verbunden: einem Rückgang der Antibiotika-Kosten um 58%, einem Rückgang der ED-Besuchskosten um 63% und einem Rückgang der Krankenhauskosten um 60%. Insgesamt ergab die Kostenanalyse eine jährliche Einsparung von 3.045 USD pro Jahr Patienten pro Jahr der SmartVest-Anwendung.
Schlussfolgerungen
Die klinische Wirksamkeit der Verwendung von SmartVest zur Behandlung von Patienten mit nicht-zystischer Fibrose-Bronchiektasie wurde zuvor durch eine signifikante Reduktion verifiziert n bei bronchiektasiebedingten Exazerbationen, was sich direkt in einer signifikanten Reduzierung der Inanspruchnahme und der Kosten der Gesundheitsversorgung in dieser Population um insgesamt 60% niederschlägt. Darüber hinaus können sekundäre Vorteile wie das Potenzial zur Reduzierung von Krankenhausrückübernahmen und das Potenzial zur Beeinflussung der Antibiotikaresistenz noch größere Vorteile haben als die Senkung der Kosten.
Schlüsselwörter
SmartVest, Hochfrequenz-Brustkorb Wandoszillation, HFCWO, Bronchiektasie, Kosten
Einleitung
Bronchiektasie ist eine chronische und ätiologisch heterogene Erkrankung. Gemeinsame Merkmale der Bronchiektasie sind Atemnot, häufige Exazerbationen, chronischer Husten, Hämoptyse und übermäßige Sputumproduktion. Die Krankheit ist in der Regel durch Zyklen mit beeinträchtigter mukoziliärer Clearance, Bronchialinfektion und Entzündung gekennzeichnet, die zu strukturellen Schäden der Atemwege mit permanenter und abnormaler Dilatation führen.1 Bronchiektasen können das Ergebnis einer Vielzahl von Erkrankungen der Atemwege und des Systems sein, einschließlich Mukoviszidose. Dyskinetische Ziliarsyndrome, Inhalations- / Aspirationsverletzungen, primäre und erworbene Immundefizienzzustände sowie eine Reihe von rheumatischen und entzündlichen Erkrankungen.2 Bronchiektasen werden bei 7 bis 52% der Patienten mit Asthma oder chronisch obstruktiver Lungenerkrankung (COPD) beobachtet .3,4 , 37
Seitz et al. Analysierten eine 5% -Stichprobe der Medicare-Datenbank für ambulante Ansprüche auf Bronchiektasen bei Leistungsempfängern im Alter von ≥ 65 Jahren von 2000 bis 2007.6 Die Datenbank enthält Informationen auf Anspruchsebene aus der nicht-institutionellen ambulanten Gesundheitsversorgung Anbieter. Die Bronchiektasie wurde von der Datenbank unter Verwendung der Codes der Internationalen Klassifikation von Krankheiten, Neunte Revision, Codes für klinische Modifikationen (ICD-9-CM) identifiziert. Die Studienpopulation umfasste > 2 Millionen Einzelpersonen, die von 2000 bis 2007 mindestens einen Monat lang in Medicare Teil B eingeschrieben waren. Die Studie ergab eine Prävalenz der Bronchiektasie in der Gesamtbevölkerung von 1.106 Fällen pro 100.000 Menschen im achtjährigen Berichtszeitraum. Die Studie ergab auch, dass die Prävalenz der Bronchiektasie bei Medicare-Begünstigten zwischen 2000 und 2007 um 8,7% anstieg und die Hospitalisierungsrate für Bronchiektasie jährlich um 2 stieg.4% bei Männern und 3,0% bei Frauen.
Die Gesamtbelastung durch fortgeschrittene Lungenerkrankungen steigt, und wenn Daten vorliegen, scheinen die Kosten im Zusammenhang mit der Morbidität und Mortalität dieser Krankheiten erheblich zu sein.2 Dies könnte, zum Teil ein Spiegelbild der zunehmenden Alterung der Bevölkerung mit chronischen Lungenerkrankungen, die einen überproportionalen Anstieg der Gesundheitskosten zur Folge hat; Die Rate der Krankenhausaufenthalte aufgrund chronischer Lungenerkrankungen steigt deutlich über das Alter von 50 Jahren und insbesondere bei älteren Frauen.2,7 Unter Verwendung der Entlassungsaufzeichnungen zwischen 1997 und 2010 wurden die durchschnittlichen Krankenhauskosten für die stationäre Versorgung bei Patienten mit a geschätzt Die Exazerbation der Lungenentzündung betrug 9.300,28 USD. Im Jahr 2001 wurden die jährlichen medizinischen Kosten für die Versorgung von Personen mit Bronchiektasie in den USA auf 13.244 USD geschätzt, was höher ist als die jährlichen Kosten für viele andere chronische Krankheiten wie Herzerkrankungen (12.000 USD) und COPD (11.000 USD) .38 Eine Studie aus dem Jahr 2005 ergab, dass Patienten mit nicht-zystischer Fibrose-Bronchiektasie durchschnittlich 2,0 zusätzliche Tage pro Jahr im Krankenhaus hatten, 6,1 zusätzliche ambulante Begegnungen und 27,2 weitere Tage Antibiotikatherapie im Vergleich zu Patienten ohne Krankheit.9 Im Jahr 2005 Die Behandlungskosten für Bronchiektasen ohne Mukoviszidose betrugen jährlich 630 Millionen US-Dollar.5
Patienten mit Bronchiektasen ohne Mukoviszidose können Schwierigkeiten haben, die Luft zu reinigen ay Sekrete und können erheblich von der Atemwegsfreigabe-Therapie profitieren.2 Ziel der Behandlung der Bronchiektasie ist es, Atemwegssekrete zu mobilisieren, um Entzündungen zu reduzieren, Infektionen der Atemwege zu verhindern, die Beatmung zu verbessern, die Anzahl der Exazerbationen zu minimieren und die Lebensqualität eines Patienten zu verbessern. 10-12 Derzeit wird eine Reihe von therapeutischen Methoden angewendet, um Atemwegssekrete bei Patienten mit Lungenerkrankungen, Beeinträchtigung der Clearance der Atemschleimhaut oder bei Patienten, bei denen das Risiko besteht, eine dieser Erkrankungen zu entwickeln, zu beseitigen.8 Diese Methoden zielen im Allgemeinen darauf ab, die Clearance der Sekretion durch Reduktion zu fördern Schleimviskosität und Verwendung von Scherkräften, um den Schleim von der Lungenwand zu lösen und die Mobilisierung zu erleichtern, um das Auswerfen zu erleichtern. Der Standard der Behandlung umfasst eine Kombinationstherapie mit mukolytischen und mukokinetischen Mitteln, Bronchodilatatoren, einer entzündungshemmenden Therapie und einer Form der physischen / mechanischen Atemwegstherapie.2 Die Atemwegstherapie spielt eine entscheidende Rolle, da sie dazu beiträgt, das Zurückhalten von mit Krankheitserregern beladenem Schleim zu vermeiden ist der zugrunde liegende Ursprung einer wiederkehrenden Infektion, die zu einer fortschreitenden Verschlechterung der Lunge führt.2,13,14 Atemwegsfreigabemethoden spielen eine entscheidende Rolle bei der Aufrechterhaltung der Gesundheit der Atemwege während der gesamten Lebenszeit des Patienten.
Eine Reihe von Atemwegsfreigaben Es stehen Methoden zur Verfügung, einschließlich Brustphysiotherapie, Masken für positiven endexspiratorischen Druck, orale Hochfrequenzgeräte und hochfrequente Brustwandoszillation (HFCWO) .2 Positive endexspiratorische Druckmasken und orale Hochfrequenzgeräte erfordern aktive Anstrengung, Beherrschung der Technik und / oder körperliche Beweglichkeit, die ihre Verwendung einschränken können.2
HFCWO wird zur Atemwegsfreigabe bei Patienten mit einem breiten Spektrum von Atemwegskompromissen verwendet ng Krankheiten und Zustände, einschließlich genetischer und immunologischer Störungen, neuromuskulärer Erkrankungen und obstruktiver Lungenerkrankungen wie Asthma und COPD.15-18 Im Gegensatz zu einigen anderen Methoden erfordert HFCWO vom Benutzer nur minimale Aktivität und ist nicht von einem Gesundheitsdienstleister abhängig Technik ist wirksam.2 Klinische Studien, vor allem bei Patienten mit Mukoviszidose, haben gezeigt, dass HFCWO sicher und wirksam ist.2,15,19-22 HFCWO liefert Kompressionsimpulse an die Brustwand über eine aufblasbare Weste, die an einen Luftimpulsgenerator angeschlossen ist .2 Der Generator erzeugt einen abwechselnden Luftstrom in und aus der Weste, der die Brustwand innerhalb eines Bereichs wählbarer Frequenzen und Drücke schnell komprimiert und freigibt. Es wurde berichtet, dass die auf die Brustwand ausgeübte oszillatorische Kompression den viskosen Schleim verdünnt, den Schleim von der Lungenwand trennt und den Schleim von den kleinen Atemwegen der Lunge zu den großen Atemwegen befördert, wo er ausgeworfen oder abgesaugt werden kann.2,23, 24 HFCWO kann zu einer signifikanten Verbesserung des Lungenvolumens von 15 bis 57 ml und des Durchflusses von bis zu 1,6 l / s führen.22
In einer früheren Fallstudie wurden die klinischen Ergebnisse der SmartVest® Airway Clearance System-Therapie bei Exazerbation bewertet -bezogene Gesundheitsversorgung und Medikamenteneinnahme bei Patienten mit nicht-zystischer Fibrose-Bronchiektasie.25 Die Studie ergab, dass die Verwendung von SmartVest zu einer statistisch signifikanten Reduzierung der Bronchiektasie-bedingten Exazerbationen um 60% führte, einschließlich des Einsatzes von Antibiotika, Notaufnahmen und Krankenhausaufenthalten . Die aktuelle Studie soll die wirtschaftlichen Auswirkungen der SmartVest-Therapie auf die Kosten für Gesundheitsversorgung und Antibiotika im Zusammenhang mit Bronchiektasen bewerten.
Methoden
Eine kürzlich durchgeführte SmartVest (Electromed, Inc., New Prague, MN) Als Grundlage für diese Analyse diente die ergebnisbasierte klinische Studie zur Fallprüfung.25 In der Studie wurden alle mit Bronchiektasen verbundenen Exazerbationen erfasst, einschließlich der Anzahl der Krankenhausaufenthalte, ED-Besuche und des Einsatzes von Antibiotika für einen Zeitraum von einem Jahr vor dem Einsatz von SmartVest (Standard der Pflegekontrolle) und zum Vergleich für einen Zeitraum von einem Jahr nach Beginn von SmartVest Verwendung (Behandlung). Die Studie umfasste nur diejenigen Probanden mit der Diagnose einer nicht-zystischen Fibrose-Bronchiektasie, die SmartVest seit mindestens einem Jahr anwenden und deren medizinische Unterlagen vor Beginn der SmartVest-Therapie ein Jahr lang verfügbar waren. Patienten wurden ausgeschlossen, wenn sie ihr vorgeschriebenes SmartVest-Therapieschema nicht eingehalten hatten, nicht telefonisch kontaktiert werden konnten oder abgelaufen waren. Alle vor der Verwendung von SmartVest gesammelten Daten wurden über die Krankenakten des Patienten erfasst.
Die Krankenakten des Patienten wurden auf alle Bronchiektasie-bedingten Exazerbationen überprüft, die während eines Zeitraums von einem Jahr vor Beginn der SmartVest-Therapie auftraten. Die Probanden wurden telefonisch kontaktiert und befragt, um für einen Zeitraum nach Beginn der SmartVest-Therapie Exazerbationen im Zusammenhang mit Bronchiektasen zu sammeln. Der Fragebogen für die Telefonumfrage wurde ausschließlich für die Studie entwickelt. Während des Telefoninterviews wurden dem Probanden spezifische Fragen zum Einsatz von Antibiotika im Zusammenhang mit den Atemwegen, zu ED-Besuchen und zu Krankenhausaufenthalten gestellt. In dem Interview wurde auch gefragt, ob der Patient SmartVest gemäß dem Verschreibungsschema des Arztes verwendet.
Die Antibiotikakosten wurden unter Verwendung der „Online-Rabatt-Apothekenpreise“ ermittelt, die Kosten für Arztbesuche und Arztgebühren wurden jedoch nicht berücksichtigt Die Kosten für Krankenhausaufenthalte und ED wurden anhand der gewichteten nationalen Schätzungen aus der Nationalen Stichprobe für stationäre Patienten (NIS) des Gesundheitskosten- und -nutzungsprojekts (HCUP), 2013, Agentur für Forschung und Qualität im Gesundheitswesen (AHRQ) ermittelt, die auf Daten basiert, die von einzelnen Staaten gesammelt und bereitgestellt wurden AHRQ durch die Staaten.26 Die NIS-Datenbank enthält eine geschichtete Wahrscheinlichkeitsstichprobe von Krankenhäusern aus staatlichen stationären Datenbanken, die Krankenhausaufenthalte von Patienten mit Medicare, Medicaid, privaten Versicherungen und Nichtversicherten umfasst.27 Die NIS enthält Daten von 5 bis 8 Millionen Krankenhausaufenthalten von etwa 1000 Krankenhäuser. Es ist vorgesehen, eine Stichprobe von ungefähr 20% der US-amerikanischen Nicht-Bundes-Kurzzeitkrankenhäuser gemäß der Definition des American Medical Associ zu erstellen ation. Die NIS stammen aus Staaten, die am Projekt für Kosten und Nutzung im Gesundheitswesen teilnehmen. Die NIS enthalten einheitliche Daten zum stationären Aufenthalt aus Krankenhausentlassungsdatenbanken, die von staatlichen Stellen, Krankenhausverbänden und anderen privaten Organisationen verwaltet werden. Die Gesamtzahl der gewichteten Entladungen in den USA basierend auf HCUP-NIS betrug 35.597.792,28 450 USD (2012) für einen ED-Besuch und 9.300 USD (2010) für einen Krankenhausaufenthalt mit Lungenentzündung. Verlängerte Krankenhausaufenthalte aufgrund von Komplikationen oder Komorbiditäten wurden nicht berechnet. Unter Verwendung der Preisberechnungen für Online-Rabattapotheken betrugen die Kosten für ein Standard-Antibiotika-Regime gegen Lungenentzündung 290 USD (2016). Die Arztgebühren für einen Arztbesuch und die anschließende Verschreibung standen nicht zur Berechnung zur Verfügung.
Von den 104 identifizierten Bronchiektasie-SmartVest-Patienten erfüllten 59 Patienten die Einschluss- / Ausschlusskriterien.25 In der Studienpopulation betrug die durchschnittliche Anzahl Die Anzahl der Antibiotika-Verschreibungen pro Jahr war bei SmartVest (0,6 / Jahr) um 58% niedriger als bei der Standardkontrolle (1,4 / Jahr) (siehe Tabelle 1). Durch die Verwendung von SmartVest konnten die ED-Besuche um 63% (0,08 / Jahr gegenüber 0,03 / Jahr) und die Krankenhauseinweisungen um 60% (0,5 / Jahr gegenüber 0,2 / Jahr) signifikant reduziert werden. Die jährlichen Kosten pro Patient für Antibiotika bei Patienten, die mit SmartVest behandelt wurden, waren im Vergleich zu Patienten, die mit Standardbehandlungen behandelt wurden, um 233 USD niedriger (siehe Tabelle 1). Die Krankenhausaufenthalte nach einjähriger SmartVest-Nutzung konnten ebenfalls um 2.790 USD pro Patient und Jahr erheblich reduziert werden. Insgesamt ergab das Gesamtergebnis eine jährliche Einsparung von 3.045 USD pro Patient und Jahr bei der Verwendung von SmartVest.
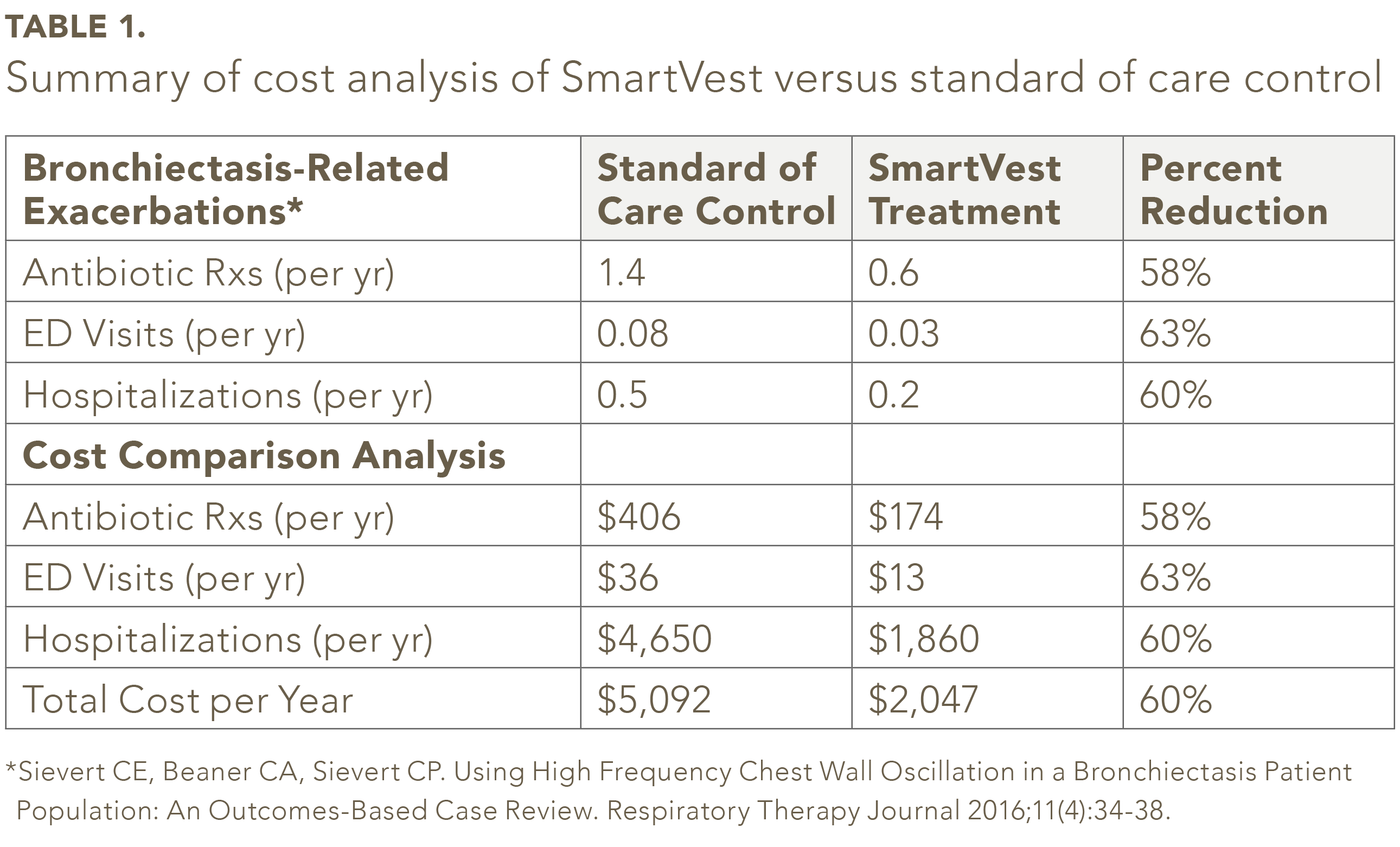
Die Analyse ergab keine Einsparungen Berücksichtigen Sie alle Arzt- / Bürogebühren, die anfallen, um ein Antibiotika-Rezept ohne Krankenhausaufenthalt zu erhalten. Die Analyse berücksichtigte auch keinen Bürobesuch wegen einer möglichen Exazerbation, die nicht zu einer Verschreibung oder einem Krankenhausaufenthalt führte. Darüber hinaus berücksichtigte die Analyse keine zusätzlichen Kosten, wenn es sich bei der Exazerbation um eine antibiotikaresistente Lungenentzündung des Bakterienstamms handelte, die Berichten zufolge mehr als 15.000 US-Dollar pro Episode kosten kann.
Diskussion
Der Zweck von Die Analyse bestand darin, die wirtschaftlichen Auswirkungen der Verwendung von SmartVest auf die mit Bronchiektasen verbundenen medizinischen Kosten im Vergleich zu einem Standard der Pflegekontrolle zu bewerten. Nach unserem Kenntnisstand ist dies die erste Studie, die die Gesundheitskosten für die Behandlung von Patienten mit nicht-zystischer Fibrose-Bronchiektasie mit HFCWO bewertet.Die Gesamtkosten umfassten die Kosten für Antibiotika, ED-Besuche und Krankenhausaufenthalte im Zusammenhang mit Exazerbationen im Zusammenhang mit Bronchiektasen ohne Mukoviszidose. Die Studie zeigte eine signifikante Verringerung der Inanspruchnahme des Gesundheitswesens und der damit verbundenen Kosten, wenn Bronchiektasiepatienten ein Jahr lang mit SmartVest behandelt wurden. Die Gesamtkosten wurden um 60% gesenkt, was einer Einsparung von 3.045 USD pro Patient und Jahr entspricht.
Eine kürzlich durchgeführte Studie, in der Krankenhausentlassungen, Rückübernahmen und ED-Besuche bei COPD oder Bronchiektasen bei Erwachsenen in den USA bewertet wurden Von 2001 bis 2012 stieg die Zahl der Krankenhausentlassungen um 88.000.31 Die Studie ergab außerdem, dass etwa 7% der Patienten mit COPD oder Bronchiektasie innerhalb von 30 Tagen mit COPD oder Bronchiektasie als Hauptdiagnose wieder aufgenommen wurden.31 Im Gegensatz dazu verringerte sich die Entlassungsrate für andere Krankheiten.31 Der Grund für den signifikanten Anstieg der COPD- und Bronchiektasie-Krankenhaus- und ED-Besuche ist nicht klar, da ein signifikanter Rückgang der Raucherquoten beobachtet wurde. Es könnte jedoch das unter Diagnose der Krankheit liegende Potenzial und die Langzeitwirkung von COPD und Bronchiektasie in einer alternden Bevölkerung widerspiegeln.31
Eine frühere ergebnisbasierte Studie zur Fallstudie ergab, dass SmartVest weniger Krankenhausaufenthalte durch verwendet 1,5-fach, 25 zeigt den Kostenvorteil von HFCWO bei der Reduzierung der Belastung durch die Inanspruchnahme des Gesundheitswesens. Andere Studien haben auch Faktoren (sowohl System als auch Patient) bewertet, die die Rückübernahme bei Patienten mit COPD senken können und zumindest teilweise für Patienten mit Bronchiektasie relevant sind. Zu diesen Faktoren gehören die Kontinuität mit der Grundversorgung des Patienten oder des Lungenarztes, die Intervention des Entlassungskoordinators sowie das Ausmaß oder die Art der Atemtherapie.32-34
Eine Verringerung der Anzahl von Exazerbationen im Zusammenhang mit Bronchiektasen kann sich ebenfalls auf a auswirken Lebensqualität des Patienten.35,36 Bei einer Population von Patienten mit COPD war die Verwendung von SmartVest mit einer signifikanten Verbesserung des Fünf-Symptome-Scores P = 0,002 (Bewertung von Sputum, Keuchen, Husten, Atemnot und Belastungstoleranz) verbunden ) .36 Die SmartVest-Behandlung zeigte auch eine signifikante Verbesserung des St. George’s Respiratory Questionnaire (SGRQ) P = 0,02, während bei Patienten, die mit konventioneller Behandlung behandelt wurden, keine Verbesserung beobachtet wurde.36 In ähnlicher Weise ergab unsere ergebnisbasierte Studie zur vorherigen Fallüberprüfung, dass 68 % der Probanden gaben während des Telefoninterviews an, dass die Verwendung von SmartVest ihre Lebensqualität erheblich verbessert hat.25
Einige Einschränkungen des Studiendesigns sollten berücksichtigt werden rot bei der Interpretation der Ergebnisse. Die Patientengröße der Studie war gering, und die Daten zu Krankenhausaufenthalten, ED-Besuchen und Antibiotika-Konsum nach Beginn der SmartVest-Therapie wurden hauptsächlich durch Patienteninterviews ermittelt. Die Studie kann als konservativ angesehen werden, da keine Kosten für Arztgebühren im Zusammenhang mit einem Bürobesuch, der zu einer Verschreibung von Antibiotika führt, oder keine Kosten für einen Besuch in der Praxis, der nicht zu einer Verschreibung von Antibiotika führte, hinzugefügt wurden. Darüber hinaus kann die Abhängigkeit von HCUP-, NIS- und AHRQ-Datenbanken, die von den in Ansprüchen eingegebenen Diagnosen abhängen, falsch oder gar nicht codiert sein, wodurch möglicherweise Messfehler in Bezug auf ICD-9-CM-basierte Variablen eingeführt werden / p>
Die Reduzierung der Kosten für die Inanspruchnahme des Gesundheitswesens wie Antibiotikaeinsatz, ED-Besuche und Krankenhausaufenthalte sind vorrangige Ziele der jüngsten Gesundheitsrichtlinien wie dem Affordable Care Act (ACA). Zum Beispiel hat der ACA das Hospital Readmissions Reduction Program (HRRP) eingerichtet, das CMS angewiesen hat, Krankenhäuser zu bestrafen, indem die Erstattungszahlungen für überschüssige Patientenrückübernahmen für denselben Zustand reduziert werden. HRRP identifizierte ursprünglich die drei wichtigsten „anwendbaren Bedingungen“ für die gezielte Rückübernahmemessung, einschließlich akutem Myokardinfarkt, Herzinsuffizienz und Lungenentzündung. Darüber hinaus hat CMS kürzlich die Ausweitung zusätzlicher anwendbarer Bedingungen ab dem Programm des Geschäftsjahres 2015 auf Patienten abgeschlossen, die für eine wieder aufgenommen wurden Akute Verschlechterung der COPD Die in dieser und anderen Studien gezeigte signifikante Verringerung der Inanspruchnahme des Gesundheitswesens und der Krankenhauseinweisungen für Patienten mit nicht-zystischer Bronchiektasie unter Verwendung von SmartVest kann eine entscheidende Rolle bei der Reduzierung von Rückübernahmen durch Krankenhäuser spielen und daher nicht bestraft werden.
Bei Patienten mit Atemwegsinfektionen, die gegen orale Antibiotika resistent sind, ist die Belastung viel größer und schwerwiegender. Intravenöse Antibiotika erschweren die Versorgung erheblich, da ein Krankenhausaufenthalt oder eine Überwachung zu Hause erforderlich ist. Die Behandlung dieser Patienten umfasst die Platzierung eines zentralen Venenkatheters sowie die Koordination von die Dosen von Medikamenten, die oft Multi gegeben werden müssen ple Zeiten pro Tag, regelmäßige Blutuntersuchungen zur Überwachung auf Nebenwirkungen und Messung der Blutspiegel des Antibiotikums über viele Tage, Schritte, die teuer werden und das Leben der Patienten stören.
Die Weltgesundheitsorganisation (WHO) hat erklärt, dass die mikrobielle Resistenz gegen Antibiotika eine „große globale Bedrohung mit verheerenden Auswirkungen auf die öffentliche Gesundheit“ darstellt. Antimikrobielle Resistenz bedroht die wirksame Prävention und Behandlung einer immer größeren Anzahl von Infektionen, die nicht nur durch Bakterien, sondern auch durch Viren und Pilze verursacht werden. Die US-amerikanischen Zentren für die Kontrolle und Prävention von Krankheiten (CDC) betrachten die Antibiotikaresistenz als eines ihrer Hauptanliegen und Prioritäten. Allein in den USA infizieren sich mindestens 2 Millionen Menschen mit antibiotikaresistenten Bakterien, und jedes Jahr sterben mindestens 23.000 Menschen als direkte Folge dieser Infektionen.39 Als Reaktion auf die weltweite Besorgnis haben die US-amerikanischen Centers for Medicare & Medicaid Services (CMS) hat kürzlich eine vorgeschlagene Regeländerung seiner Teilnahmebedingungen veröffentlicht, nach der Krankenhäuser unter anderem Antibiotika-Stewardship-Programme implementieren müssen, um an Medicare- und Medicaid-Programmen teilnehmen zu können. Antibiotika-Stewardship umfasst die Verbesserung der Patientenergebnisse durch die Einführung von Prozessen und Verfahren, die das Auftreten von Infektionen mit pa reduzieren Besondere Aufmerksamkeit auf Lungenentzündung wie vorbeugende Behandlung. Als sekundärer Vorteil zu den Kosten-Nutzen-Ergebnissen dieser Studie kann eine signifikante Reduzierung des Antibiotika-Bedarfs bei Bronchiektasie-Patienten durch die Verwendung von SmartVest noch größere Vorteile haben als die Kosten zu senken. Eine verfügbare Behandlung, die Infektionen der Atemwege und damit den Bedarf an Antibiotika erheblich reduzieren könnte, passt gut in die Infektionskontrollprogramme des Krankenhauses.
Zusammenfassend zeigt SmartVest die klinische Wirksamkeit der HFCWO-Atemwegsfreigabe bei Patienten mit COPD36 und bei Patienten mit COPD36 Bronchiektasie 25 und die in dieser Studie beobachtete signifikante Reduzierung der Kosten für Antibiotika, ED und Krankenhausaufenthalte unterstützen den Kostenvorteil der Verwendung von SmartVest und sprechen sich für den Versicherungsschutz von SmartVest durch die Zahler aus. Darüber hinaus können sekundäre Vorteile wie das Potenzial zur Reduzierung von Krankenhausrückübernahmen und das Potenzial zur Beeinflussung der Antibiotikaresistenz noch größere Vorteile haben als die Senkung der Kosten.
Laden Sie den Studientext herunter
Danksagungen
Die Autoren möchten sich bei Elizabeth Goodwin PhD für die redaktionelle Unterstützung bedanken.
- King P. Pathogenese der Bronchiektasie. Paediatr Respir Rev. 2011; 12 (2): 104–110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Hochfrequente Brustkompression: eine praktische Therapie für Patienten mit Bronchiektasie. Respiratory Therapy 2008; 3 (1): 22-26.
- Patel IS, Vlahos I., Wilkinson TM, et al. Bronchiektasie, Exazerbationsindizes und Entzündungen bei chronisch obstruktiven Lungenerkrankungen. Am J Respir Crit Care Med 2004; 170 (4): 400 & ndash; 407. 10.1164 / rccm.200305-648OC
- Gono H., Fujimoto K., Kawakami S. et al. Bewertung der Wandstärke der Atemwege und des Lufteinschlusses durch HRCT bei asymptomatischem Asthma. Eur Respir J 2003; 22 (6): 965-971. Weycker D., Edelsberg J., Oster G. et al. Prävalenz und wirtschaftliche Belastung durch Bronchiektasen. Clinical Pulmonary Medicine 2005; 12 (4): 205–209. Seitz AE, Olivier KN, Adjemian J. et al. Trends in der Bronchiektasie bei Begünstigten von Arzneimitteln in den USA, 2000 bis 2007. CHEST Journal 2012; 142 (2): 432-439. Seitz AE, Olivier KN, Steiner CA, et al. Trends und Belastung durch Krankenhausaufenthalte im Zusammenhang mit Bronchiektasen in den USA, 1993-2006. Chest 2010; 138 (4): 944 & ndash; 949. 10.1378 / Brust 10-0099
- Seitz AE, Olivier KN, Steiner CA, et al. Trends und Belastung durch Krankenhausaufenthalte im Zusammenhang mit Bronchiektasen in den USA, 1993-2006. CHEST Journal 2010; 138 (4): 944-949. Weycker D., Edelsberg J., Oster G. et al. Prävalenz und wirtschaftliche Belastung durch Bronchiektasen. Clinical Pulmonary Medicine 2005; 12: 205–209.
- Fibrosis. AoCPiC. Pflegestandards und gute klinische Praxis für das Physiotherapie-Management bei Mukoviszidose 2011. Verfügbar ab: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio Jun 11.pdf.
- O’Donnell AE. Bronchiektasie. Chest 2008; 134 (4): 815 & ndash; 823. 10.1378 / Brust.08-0776
- Barker AF. Bronchiektasie. N Engl J Med 2002; 346 (18): 1383 & ndash; 1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Nichtpharmakologische Atemwegstherapien: ACCP-Richtlinien für evidenzbasierte klinische Praxis. Chest 2006; 129 (1 Suppl): 250S-259S. 10.1378 / Brust.129.1 Suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Behandlung der mukoziliären Dysfunktion. Chest 1996; 110 (4): 1048–1057. Arens R., Gozal D., Omlin KJ, et al. Vergleich der hochfrequenten Brustkompression und der konventionellen Brustphysiotherapie bei Krankenhauspatienten mit Mukoviszidose. Am J Respir Crit Care Med 1994; 150 (4): 1154 & ndash; 1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Hochfrequente Schwingung der Atemwege und der Brustwand. Respir Care 2002; 47 (7): 797 & ndash; 807. Hansen LG, Warwick WJ.Hochfrequentes Brustkompressionssystem zur Unterstützung der Entfernung von Schleim aus der Lunge. Biomed Instrum Technol 1990; 24 (4): 289 & ndash; 294. Lange DJ, Lechtzin N., Davey C. et al. Hochfrequente Brustwandoszillation bei ALS: eine explorative randomisierte, kontrollierte Studie. Neurology 2006; 67 (6): 991 & ndash; 997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. Die Langzeitwirkung der hochfrequenten Brustkompressionstherapie auf Lungenkomplikationen bei Mukoviszidose. Pediatr Pulmonol 1991; 11 (3): 265 & ndash; 271. Kluft J., Beker L., Castagnino M. et al. Ein Vergleich der Bronchialdrainage-Behandlungen bei Mukoviszidose. Pediatr Pulmonol 1996; 22 (4): 271 & ndash; 274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P Scherer TA, Barandun J., Martinez E. et al. Einfluss hochfrequenter oraler Atemwegs- und Brustwandschwingungen und konventioneller physikalischer Brusttherapie auf den Auswurf bei Patienten mit stabiler Mukoviszidose. Chest 1998; 113 (4): 1019–1027. Nicolini A., Cardini F., Landucci N. et al. Wirksamkeit der Behandlung mit hochfrequenter Brustwandschwingung bei Patienten mit Bronchiektasie. BMC Pulm Med 2013; 13: 21. 10.1186 / 1471-2466-13-21 Osman LP, Roughton M., Hodson ME, et al. Kurzzeit-Vergleichsstudie zu hochfrequenten Brustwandoszillationen und europäischen Atemwegsfreigabetechniken bei Patienten mit Mukoviszidose. Thorax 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Hochfrequenzunterstützte Atemwegsfreigabe. Respir Care 2007; 52 (9): 1224 & ndash; 1235; Diskussion 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Verwendung der hochfrequenten Brustwandoszillation bei einer Bronchiektasie-Patientenpopulation: Eine ergebnisbasierte Fallübersicht. Respiratory Therapy Journal 2016; 11 (4): 34-38.
- HCUP. Überblick über die landesweite Stichprobe der Notaufnahme (NEDS) 2016. Verfügbar ab: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Übersicht über die nationalen (landesweiten) stationären Proben. Verfügbar ab: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C. Kosten für Krankenhausaufenthalte in der USA, 2010: Statistical Brief # 146. Statistische Kurzberichte zum Gesundheitskosten- und Nutzungsprojekt (HCUP). Rockville (MD): Agentur für Gesundheitsforschung und Qualität (USA); 2006.
- Stein PD, Matta F. Kosten für Besuche in der Notaufnahme und Krankenhausaufenthalte wegen pulmonaler arterieller Hypertonie.
J Epidemiol Public Health Rev. 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Erstattung des Übergangspflege-Managements zur Reduzierung der COPD-Rückübernahme. Chest
2014; 145 (1): 149–155. 10.1378 / Brust.13-0787 - Ford ES. Krankenhausentlassungen, Rückübernahmen und ED-Besuche wegen COPD oder Bronchiektasie bei Erwachsenen in den USA: Ergebnisse
aus der landesweiten Stichprobe stationärer Patienten 2001-2012 und der landesweiten Stichprobe der Notaufnahme 2006-2011. Chest 2015; 147 (4): 989 & ndash; 998. 10.1378 / Brust.14-2146 - Sharma G, Kuo YF, Freeman JL, et al. Ambulanter Kontrollbesuch und 30-tägiger Besuch in der Notaufnahme sowie Rückübernahme bei Patienten, die wegen einer chronisch obstruktiven Lungenerkrankung ins Krankenhaus eingeliefert wurden. Arch Intern Med 2010; 170 (18): 1664 & ndash; 1670. 10.1001 / archinternmed.2010.345
- Lainscak M., Kadivec S., Kosnik M., et al. Die Intervention des Entlassungskoordinators verhindert Krankenhausaufenthalte bei Patienten mit COPD: eine randomisierte kontrollierte Studie. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O., Sewell L., Morgan MD, et al. Ein kurzes ambulantes Lungenrehabilitationsprogramm reduziert die Rückübernahme nach einem Krankenhausaufenthalt wegen einer Verschlimmerung einer chronisch obstruktiven Lungenerkrankung. Respirology 2013; 18 (7): 1063 & ndash; 1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. Eine langfristige Luftbefeuchtungstherapie ist bei Patienten mit mittelschwerer oder schwerer chronisch obstruktiver Lungenerkrankung oder Bronchiektasie kostengünstig. Value Health 2014; 17 (4): 320–327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. Eine Pilotstudie zum Einfluss hochfrequenter Brustwandoszillationen bei Patienten mit chronisch obstruktiver Lungenerkrankung mit Schleimhypersekretion. Int J Chron Obstruct Pulmon Dis 2011; 6: 693–699. 10.2147 / COPD. S22896.
- Martınez-Garcıa MA, et al. Prognostischer Wert der Bronchiektasie bei Patienten mit mittelschwerer bis schwerer chronisch obstruktiver Lungenerkrankung. Am J Respir Crit Care Med 2013; Vol 187, Iss. 8, S. 823–831.
- O’Donnell AE. Bronchiektasie. Chest 2008; 134: 815–82.
- Zentren für die Kontrolle und Prävention von Krankheiten – Website zur Antibiotikaresistenz / Antibiotikaresistenz https://www .cdc.gov / drugresistance /