Aortadilatasjon ved bicuspid aortaklaffesykdom | Revista Española de Cardiología (engelsk utgave)
Innledning
Bicuspid aorta valve (BAV) er den vanligste medfødte hjerteavviket, forekommer hos 0,5% -1,4% av befolkningen ; denne anomalien overføres sporadisk genetisk av en autosomal-dominerende vei, med en 3: 1 mannlig overvekt. 1 BAV er klinisk viktig, ikke bare på grunn av ventilrelaterte komplikasjoner (ventil dysfunksjon, infektiøs endokarditt), men også på grunn av dens tilknytning til mange vaskulære abnormiteter, inkludert aortadilatasjon2 (figur 1).
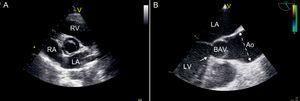
Figur 1. Ekkokardiografiske bilder som vurderer bicuspid aortaklaff. A: Transthoracic parasternal kort akse visning som viser bicuspid aortaklaff med antero-posterior konfigurasjon. B: Transesofageal langaksevisning som viser unormal systolisk åpning («kuppel») av en bicuspid aortaklaff. Aortadilatasjon er tydelig, begynnende over sinotubulær kryss og er maksimal i midten av stigende del av den tubulære aorta (stiplet linje). stenose er tilstede, med en fibrøs rygg som oppstår fra septaldelen av venstre ventrikkelutstrømningskanal (pil). Ao, aorta; BAV, bicuspid aortaklaff; LA, venstre atrium; LV, venstre ventrikkel; RA, høyre atrium; RV, høyre ventrikkel.
Den rapporterte prevalensen av BAV-relatert aortadilatasjon varierer fra 33% -80%. Denne variasjonen er basert på terskler som brukes til å definere dilatasjon, normale verdier for alder og kroppsoverflate og region av Forskjellige typer aortaaneurismer er beskrevet avhengig av hvilken region som er involvert, 3 er utvidelse av midtstigende kanal (utvidelse ved den rørformede stigende delen alene), det hyppigste mønsteret som er observert.4 Alder og BAV-morfologi har også vært assosiert ed med stigende aorta (AscAo) dimensjon, selv om morfologiens rolle ikke er klart definert.5, 6
Patofysiologi
Det er fortsatt kontrovers mellom to teorier om patogenesen av aortadilatasjon hos pasienter med BAV. En teori hevder at AscAo-utvidelse kan være en konsekvens av turbulens i blodstrømmen, med en primær hemodynamisk effekt som virker fra fosterets liv og resulterer i forskjellige grader av stressindusert aortadegenerasjon. Selv om denne hypotesen har fordelen av relativ enkelhet, antyder noen studier at hemodynamiske endringer alene ikke kan være eneansvarlige for aortadilatasjon hos disse pasientene.7 Den andre teorien reiser hypotesen om tilstedeværelsen av en medfødt medfødt defekt i aortastrukturen. Sammenhengen mellom cusp-arrangement og AscAo-sykdom kan forklares med unormale utviklingsmønstre for nevrale kamceller, og strukturelle abnormiteter vil forekomme på cellenivå uavhengig av den hemodynamiske lesjonen.8 Denne teorien har blitt stadig mer populær det siste tiåret, og har ført til mer aggressive anbefalinger for behandling av proksimal aorta hos disse pasientene. Det er noen bevislinjer som støtter den dominerende medfødte veggabnormiteten:
-
• Hos BAV-pasienter (inkludert barn) med normalt fungerende aortaklaff er det observert signifikant proksimal aortaforstørrelse sammenlignet med aldersmatchte normale kontroller. Imidlertid er en ‘normalt’ fungerende BAV iboende stenotisk, med ikke-aksial og turbulent strøm selv om det ikke er noen transvalvulær trykkgradient. Denne strømmen er svært eksentrisk og forårsaker unormale spiralformede strømningsmønstre i den proksimale aorta.9 Disse unormale hemodynamiske mønstrene virker over lange perioder og kan føre til asymmetriske stressinduserte aortavegglesjoner med påfølgende utvidelse av spesifikke aortasegmenter.
-
• Pasienter med BAV har vist seg å ha større aortarot og AscAo-diametre enn pasienter med tricuspid aortaklaff (TAV), selv etter matching for hemodynamisk alvorlighetsgrad av klaffeskader.5 Imidlertid jeteksentrisitet som skjer gjennom BAV har ikke blitt analysert.
-
• AscAo-utvidelse kan forekomme selv etter utskifting av aortaklaffen.10
-
• En indre veggabnormalitet vil bli støttet av demonstrasjonen av en histopatologisk abnormitet som ligger til grunn for AscAo-komplikasjoner i BAV, nemlig cystisk medial degenerasjon. Dette patologiske funnet er observert i aortaene til pasienter med BAV før aneurismedannelse oppstår, og består av en redusert ekstracellulær matrikskomponent og økte matriseredbrytningsenzymer i aorta. 11, 12, 13 Interessant, selv om lignende histologiske og biomolekylære endringer forekommer i BAV og Marfan aortas, fordelingen av disse endringene er forskjellig i begge forhold, og til og med i TAV-aneurismer (tabell 1), som tar til orde for en primær rolle for hemodynamikk i utviklingen av reaktiv aortaveggombygging.
Tabell 1 .Histopatologi av cystisk medial degenerasjon
Karakteristisk BAV-aneurisme Marfan-aneurisme TAV-aneurisme Reduksjon av ECM-komponenter Øk VSMC-apoptose: redusert produksjon av ECM-proteiner Elastinfragmentering: tap av strukturell støtte og elastisitet FB-1-mangel: løsrivelse av VSMC fra elastin og kollagenmatrise (matriseforstyrrelse) Mindre grad av endringer Øk matrixnedbrytningsenzymer Øk MMP -2Øk MMP-9 Øk MMP2 / TIMP-1 Øk MMP-12 Øk MMP-13 Romlig CMD-fordeling Asymmetrisk Omkrets Begrenset til aneurysmal region BAV , bicuspid aortaklaff; CMD, cystisk medial degenerasjon; ECM, ekstracellulær matrise; FB, fibrillin; MMP, matriksmetalloproteinase; TAV, tricuspid aortaklaff; TIMP, vevsinhibitor av metalloproteinase; VSMC, vaskulære glatte muskelceller.
-
• Endelig har det blitt antydet at BAV-sykdom har høy arvelighet, med vilje som nesten er genetisk. I store familiestudier er det rapportert at BAV hos førstegrads slektninger (FDR) til en person med BAV er 9%. I tillegg har noen studier rapportert aortarotdilatasjon, thorax aorta-aneurisme eller aortadisseksjon hos opptil en tredjedel av FDR av BAV-pasienter, uansett om det var en BAV. 14, 15 Selv om flere potensielle gensteder for BAV og AscAo-aneurismer har vært antydet, er det ikke fastslått noe bestemt sted som ansvarlig for aortadilatasjon i BAV.
Dilatasjonens naturhistoriehastighet
Aortadilatasjon er dokumentert i barndommen, noe som antyder at dette prosessen begynner tidlig i livet. Informasjon om progresjonen av aortasykdom assosiert med BAV varierer mye, med studier som rapporterer ≈0,3-1,1 mm per år (mm / år). 7 I Olmsted County-studien var prevalensen av AscAo-utvidelse (> 40mm) var 15%, og i en undergruppe av pasienter med gjentatte målinger steg prevalensen til 39% .16 Selv om mange risikofaktorer er assosiert med utvidelse av aorta (høyt blodtrykk, mannlig kjønn, signifikant ventil sykdom), er den viktigste variabelen sannsynligvis alder. Både pediatriske og voksne studier har rapportert at, sammenlignet med TAV-assosierte aneurismer, blir BAV-relatert aneurisme raskere forstørret og presenterer i en betydelig yngre alder. 6, 7 I tillegg er progressiv utvidelse av aorta vanligere hos pasienter med større aortas ved baseline.
Aortadisseksjon og brudd
Selv om den mest fryktede aortakomplikasjonen hos BAV-pasienter er aortadisseksjon, forblir den faktiske forekomsten av denne komplikasjonen under debatt. Prevalensen varierer avhengig av den studerte kohorten, med et samlet estimat av tilfeller på 4% .17, 18 Noen rapporter fra henvisningssentre antydet en risiko for aortadisseksjon 5-9 ganger høyere i BAV enn i TAV, mens andre observerte ingen slik sammenheng .7, 19 Nyere studier har gitt en lavere risiko. I Toronto-serien var 20 forekomsten av disseksjon 0,1% per pasientår av oppfølging, og i Olmsted County-studien var den 25-årige kohortrisikoen for aortadisseksjon etter ekkokardiografisk diagnose 0,5% .21
Faktisk dissekeres og sprekker BAV-assosierte AscAo-aneurismer med et størrelsesområde som er sammenlignbart med det for aneurismer fra andre etiologier (gjennomsnitt: 60 ± 12 mm; område: 30-108 mm) .22 Den økte risikoen for disseksjon og brudd assosiert med BAV skyldes den høyere prevalensen og frekvensen av aortadilatasjon, som forekommer i en betydelig yngre alder enn idiopatiske AscAo-aneurismer. 7, 19 En sammenligning mellom BAV- og TAV-pasienter viste at, selv om BAV-pasienter hadde en høyere hastighet på aorta-vekst ( 1,9 vs 1,3 mm / år), var forekomsten av brudd og disseksjon lik.7 Derfor til tross for raskere vekstrater, oppstår negative hendelser i lignende hastigheter og i lignende aortadiametre.
Pasienter med Marfan syndrom har en mye høyere levetidssannsynlighet for aortadissektio n (40%) enn pasienter med BAV. Siden BAV-sykdom er ~ 100 ganger mer vanlig enn Marfan-syndromet, er BAV-sykdommen ansvarlig for et like stort eller større antall aortadisseksjoner enn Marfan-syndromet. 22
Diagnose og overvåkning
Transthoracic echocardiogram (TTE) er vanligvis den primære avbildningsteknikken for diagnostisering av BAV (figur 1), siden den identifiserer pasienter der aortaroten eller AscAo forstørres og vurderer progresjonen deres over tid. Normalområdet (AscAo og aortarotdiameter2) må korrigeres for alder og kjønn.Disse TTE-målingene korrelerer tett med målinger ved multidetektor computertomografi (CT) scan23 og magnetisk resonanstomografi (MRI), 24 som antyder at TTE er en nøyaktig bildemodalitet. Ikke desto mindre kan standard TTE ikke visualisere hele AscAo og kan ikke oppdage den største diameteren, vanligvis mest uttalt i den proksimale til midten av AscAo. Det anbefales at en MR- eller CT-skanning utføres for å evaluere hele AscAo når den ikke blir tilstrekkelig visualisert av ekkokardiogram. Det er også rimelig å utføre en MR eller CT-skanning ved utgangspunktet når aortadilatasjon (≥45 mm) først diagnostiseres, noe som vil tjene som et referansetiltak under oppfølgingen hvis det oppdages avvik mellom serielle ekkokardiogrammer. En MR-skanning kan nøyaktig oppdage og måle aortaaneurismer og bekrefte ventilanatomi, og unngå kontrast og stråleeksponering. Nylig har unormal systolisk spiralstrøm blitt demonstrert av 4-dimensjonal MR, og graden og retningen av strømningsstråleeksentrisitet kan være avgjørende for å bestemme risikoen for segmentell aneurismedannelse.9 Den spesifikke aortaanatomien kan diktere hvilken bildebehandling som er optimal. For eksempel, når aneurismer involverer aortaroten, er MR å foretrekke fremfor CT, fordi CT avbilder roten mindre godt og er mindre nøyaktig i størrelsen på diameteren. Hvis det er en kontraindikasjon mot CT og MR, er TEE et rimelig alternativ som er klart bedre enn TTE for å vurdere aneurismer som ligger i aortaroten (figur 1), aortabuen og synkende aorta. Kombinasjonen av TTE og multi-slice CT angiogram kan gi all nødvendig informasjon hvis det er planlagt kirurgi.
Når en thorax aorta-aneurisme først oppdages, er det ikke mulig å bestemme veksthastigheten, og det er derfor hensiktsmessig å oppnå en gjentatt bildestudie 6 måneder etter den første studien. Hvis størrelsen på aneurismen forblir uendret, er det i de fleste tilfeller rimelig å få en bildebehandling på årlig basis.25 Dette gjelder også etter utskifting av aortaklaffen, ettersom progressiv aortadilatasjon kan forekomme. Oppfølgingsevaluering bør vurderes med kortere intervaller, avhengig av aortadimensjoner, ekspansjonshastighet og fysisk aktivitet. Hos BAV-pasienter uten signifikante ventillesjoner og normal aortadiameter kan et ekkokardiogram hvert annet år være tilstrekkelig.
Til slutt bør screening av FDR av BAV-pasienter vurderes for å oppdage misdannelse i aortaklaffen og utvidet AscAo. TTE kan pålitelig identifisere FDR med strukturelle hjerteavvik14, 26 (figur 2). Imidlertid er den naturlige historien til FDR med en mildt utvidet aortarot og en TAV-fenotype ukjent. Derfor er det nødvendig med langsiktige oppfølgingsstudier av denne populasjonen, både for å bestemme utvidelsesgraden, og for å fastslå frekvensen av seriell TTE-screening, som med rimelighet vil oppdage utvidelse av aorta før komplikasjoner oppstår. 14
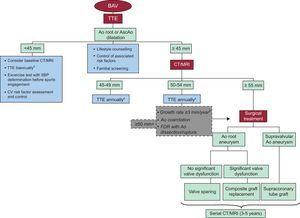
Figur 2. Algoritme som viser generell tilnærming til aorta dilatasjon ledelse og overvåking. Ao, aorta; AscAo, stigende aorta; BAV, bicuspid aortaklaff; CT, computertomografi; CV, kardiovaskulær; FDR, førstegrads slektninger; MR, magnetisk resonansavbildning; SBP, systolisk blodtrykk; TTE, transthoracic echocardiogram.aVurdere tidligere oppfølging hvis valvulær dysfunksjon er til stede. BSerie sammenligninger av bilder gjort med samme bildebehandlingsteknikk, side om side, på samme aortanivå.
Management Medical Management
I tillegg til rutinemessig bildebehandling, bør pasienter med BAV motta informasjon om risikoen for disseksjon og dannelse av aneurisme, samt de typiske symptomene på akutt aortadisseksjon (Figur 2).
Aktiviteter eller livsstil bør modifiseres siden høy intensitet , konkurranse- og kollisjonsidretter er potensielt farlige og kan utløse aortadisseksjon eller brudd i mer enn milde utvidede aortaer (45 mm) .27
Tilknyttede kardiovaskulære risikofaktorer som høyt blodtrykk bør kontrolleres aggressivt hos disse pasientene. β-blokkere kan administreres for å forsinke eller forhindre aortarotdilatasjon eller progresjon hos BAV-pasienter (i fravær av alvorlig aortaoppstøt) .25, 26 Begrunnelsen for denne anbefalingen er imidlertid basert på effekten av β-blokkeringsbehandling i Marfan , 28 og bør derfor bekreftes av videre forskning. Selv om noen studier ga en fordel med angiotensinreseptorblokker og angiotensinkonverterende enzyminhibitorbehandling hos personer med Marfan syndrom, 29, 30, er det foreløpig ingen data som viser en lignende fordel fra disse terapiene ved BAV-aneurisme.
Den medisinske behandlingen av BAV-sykdom inkluderer for øyeblikket ikke statiner, noe som potensielt kan begrense aortadilatasjon ved å redusere matrisemetalloproteinaseekspresjon og forbedre endotelfunksjonen via økt endotel nitrogenoksidsyntase.31 En nylig randomisert, placebokontrollert studie som involverte deltakere med mild eller moderat aortastenose viste at statiner ikke endret aortaklaffrelaterte hendelser eller progresjon av aortaklaffstenose.31 Imidlertid hadde bare ~ 5% av deltakerne BAV. Videre forskning fokusert på effekten av statiner på AscAo-utvidelse, disseksjon og brudd hos pasienter med BAV-sykdom er berettiget.
Kirurgi
Den optimale timingen for aortakirurgi hos pasienter med BAV uten indikasjon for ventiloperasjon er fortsatt usikker pga. de begrensede dataene som er tilgjengelige om den naturlige historien til asymptomatisk aortadilatasjon (figur 2). AscAo-diameter er den dimensjonen som oftest brukes til å bestemme størrelsen på den forstørrede aorta, og er et viktig kriterium for å anbefale valgfri kirurgi hos asymptomatiske pasienter med aortaaneurisme. Nåværende retningslinjer sier at kirurgi for å reparere aortaroten eller erstatte AscAo er indikert hos pasienter med TAV hvis diameteren på aortaroten eller AscAo er ≥55 mm, og at formler som inkluderer høyde og aorta tverrsnittsareal for pasienter med liten vekst bør brukes. 25, 32, 33 Nedre terskel (≥50 mm) anbefales hos Marfan- og BAV-pasienter. Basert på nylige langsiktige oppfølgingsstudier er imidlertid forskjellene mellom begge enhetene betydelige. Pasienter med BAV faller sannsynligvis mellom de to ytterpunktene i et spekter av tilstander representert av Marfan syndrom og degenerativ AscAo-aneurisme, og størrelseskriterier for kirurgisk inngrep kan være midt mellom de som er etablert for begge tilstandene (henholdsvis 50 og 55 mm). Hos BAV-pasienter med risikofaktorer som aortakoarktasjon, alvorlig aortastenose eller FDR med en historie med aortaruptur eller disseksjon, er det tilrådelig å operere når AscAo er ≥50 mm, og hos de som gjennomgår utskiftning av valgfri aortaklaff når er ≥ 45 mm. Ekspansjonshastigheten har vist seg å være en annen viktig prediktor for brudd. En vekstrate over 10 mm / år har tradisjonelt blitt ansett som en indikasjon for kirurgi.34 Nylige fremskritt innen kardiovaskulær bildebehandling har forbedret reproduserbarheten til seriemålinger. Derfor er det generell enighet om å akseptere en utvidelseshastighet på mer enn 3 mm / år som avskjæringsverdi for å indikere kirurgi, forutsatt at sammenligninger har blitt gjort nøyaktig side om side, med samme bildebehandlingsteknikk og på samme nivå av aorta. Til slutt må intervensjonskriterier veies nøye mot kirurgisk risiko, både for pasienten (alder, comorbiditeter osv.) Og for senteret. På de beste sentrene er den nåværende sykehusdødeligheten for valgfri kirurgi av AscAo hos unge pasienter uten komorbiditeter rundt 2%. 34, 35 Pasientkarakteristikker, aortaklaffedysfunksjon, plassering av aortadilatasjon og type operasjon bør vurderes i beslutningsprosessen .
Det er flere mulige kirurgiske alternativer, og valget avhenger av aneurysmens beliggenhet, distale omfang av aortainnblanding og ønsket antikoagulasjonsstatus (Tabell 2) .36, 37 Hvis ventilreparasjon eller en ventilsparende intervensjon vurderes, TEE kan utføres pre- eller intraoperativt for å definere anatomi av cusps og AscAo.38
Tabell 2. Kirurgiske alternativer for Bicuspid Aorta Valve Disease
| Kirurgisk teknikk | Betraktninger |
| Reduksjon av aortoplastikk med / uten ekstern syntetisk innpakning | • Generelt ikke anbefalt (risiko for tilbakevendende utvidelse) • Alternativ for pasienter med høyt s akutt risiko (spesielt hvis bihulene ikke er betydelig utvidet) |
| Erstatning av aortarot og AscAo med reimplantasjon av koronar ostia (Bentall-prosedyre) | Standardteknikk i pasienter med betydelig ventilsykdom og utvidelse av AscAo |
| Utskifting av aortaklaff og separat suprakoronar aorta reparasjon | • Generelt ikke anbefalt (risiko for progressiv sinus dilatasjon) • Alternativ for eldre pasienter med BAV-stenose, bihuler i normal størrelse og utvidelse av supracoronar AscAo |
| Ventilsparende aortautskiftning | Akseptabelt alternativ for unge pasienter med normalt- fungerende BAV |
| Lungeautograft | • Generelt ikke anbefalt (fare for utvidelse av autograft) • Alternativ for barn, ungdommer eller unge kvinner som ønsker å bli gravid |
| Reparasjon av aortaklaff | Akseptabelt alternativ hvis nøye pasientvalg er gjort |