Kostnadseffektiv analyse av bruk av høyfrekvent brystveggoscillasjon (HFCWO) hos pasienter med ikke-cystisk Fibrose Bronchiectasis
Abstrakt
Bronchiectasis er en kronisk progressiv sykdom preget av irreversibel patologisk utvidelse av lungebronker. Behandlinger for bronkiektasi er rettet mot å mobilisere luftveisekresjoner, redusere betennelse, forhindre luftveisinfeksjoner, forbedre ventilasjon, minimere antall forverringer og forbedre en persons livskvalitet. Høyfrekvent svingning i brystveggen (HFCWO) er en luftveisklareringsbehandling som for tiden brukes for en rekke kroniske luftveiskompromitterende sykdommer, inkludert ikke-cystisk fibrose bronkiektase. Denne studien evaluerte den økonomiske effekten av HFCWO-behandling levert av SmartVest® Airway Clearance System på bronkiektaserelatert helseutnyttelse og kostnad.
Metoder
Resultatene av et tidligere publisert utfall av saksgjennomgang -basert klinisk studie av forfatterne ga grunnlaget for denne kostnadseffektivitetsanalysen. Bronkiektaserelaterte forverringer inkludert antall sykehusinnleggelser, akuttmottak (ED) og hyppigheten av antibiotikaresepter ble registrert for hver pasient i ett år før SmartVest-bruk (standard omsorgskontroll) og i ett års periode etter start av SmartVest bruk. Forverringsratene for ett år før SmartVest og ett år etter SmartVest ble sammenlignet. Forverringer ble verifisert fra både pasientens journal og via telefonintervju. Antibiotikakostnader ble bestemt ved bruk av «on-line rabatt apotekpriser», mens sykehusinnleggelse og ED-kostnader ble bestemt ved hjelp av Healthcare Cost and Utilization Project (HCUP) Statistical Brief # 146 og HCUP National Inpatient Sample (NIS) 2013 database.
Resultater
De tidligere publiserte kliniske utfallene fra femtito SmartVest pasienter med ikke-cystisk fibrose bronkiektasi tjente som grunnlag for denne analysen. Når resultatdata ble analysert, brukte SmartVest sammenlignet med standard av omsorgskontroll, var assosiert med statistisk signifikante resultater; 58% reduksjon i antibiotikakostnad, 63% reduksjon i ED-besøkskostnader og 60% reduksjon i sykehusinnleggelseskostnader. Totalt resulterte kostnadsanalysen i en årlig besparelse på $ 3,045 per pasient per år med SmartVest-bruk.
Konklusjoner
Den kliniske effekten av å bruke SmartVest som behandling for pasienter med ikke-cystisk fibrose bronkiektase ble tidligere verifisert med en signifikant reduktio n ved bronkiektaserelaterte forverringer, noe som direkte betyr en betydelig reduksjon på 60% i helseutnyttelse og -kostnader i denne befolkningen. Videre kan sekundære fordeler som potensialet for å redusere sykehusinnleggelser og potensialet for innvirkning på å avskrekke antibiotikaresistens ha enda større fordeler enn å redusere kostnadene.
Nøkkelord
SmartVest, høyfrekvent brystkasse veggsvingning, HFCWO, bronkiektase, kostnad
Innledning
Bronkiektase er en kronisk og etiologisk heterogen sykdom. Vanlige kjennetegn ved bronkiektasi er kortpustethet, hyppige forverringer, kronisk hoste, hemoptyse og overdreven sputumproduksjon. Sykdommen er typisk preget av sykluser med nedsatt slimhinneavklaring, bronkial infeksjon og betennelse som resulterer i strukturell skade på luftveiene med permanent og unormal utvidelse.1 Bronkiektase kan være resultatet av et mangfoldig utvalg av luftveissykdommer, inkludert cystisk fibrose, dyskinetiske ciliære syndromer, inhalasjons- / aspirasjonsskader, primære og ervervede immundefekttilstander, og en rekke revmatiske og inflammatoriske tilstander.2 Bronkiektase er observert hos 7% til 52% av pasienter med astma eller kronisk obstruktiv lungesykdom (KOLS) , 37
Seitz, et al., Analyserte en 5% prøve av Medicare poliklinisk skadedatabase for bronkiektase blant mottakere i alderen ≥ 65 år fra 2000 til 2007.6 Databasen inneholder informasjon på kravnivå fra ikke-institusjonell poliklinisk helse leverandører. Bronkiektase ble identifisert av databasen ved hjelp av International Classification of Diseases, Ninth Revision, Clinical Modification codes (ICD-9-CM) koder. Studiepopulasjonen inkluderte > 2 millioner unike individer registrert i Medicare del B i minst en måned fra 2000 til 2007. Studien bestemte forekomsten av bronkiektasi i den totale befolkningen til 1 106 tilfeller per 100 000 mennesker over den åtte år lange gjennomgangsperioden. Studien fant også at forekomsten av bronkiektasi hos Medicare-mottakere økte med 8,7% mellom 2000 og 2007, og sykehusinnleggelsen for bronkiektase økte årlig med en hastighet på 2.4% blant menn og 3,0% blant kvinner.
Den samlede byrden av avansert lungesykdom øker, og der data foreligger, ser kostnadene knyttet til sykdommen og dødeligheten av disse sykdommene til å være betydelig.2 Dette kan, delvis være en refleksjon av den økende aldrende befolkningen med kronisk lungesykdom som har en uforholdsmessig økning i helsekostnadene; sykehusinnleggelsesfrekvensen på grunn av kronisk lungesykdom øker markant over 50 år, og særlig hos eldre kvinner.2,7 Ved bruk av utskrivingsjournaler fra 1997-2010 ble det beregnet den gjennomsnittlige sykehuskostnaden for innleggelse hos pasienter med Forverring av lungebetennelse var $ 9 300,28 I 2001 ble det også anslått at den årlige medisinske kostnaden for omsorg for personer i USA med bronkiektasi var $ 13 244, noe som er større enn den årlige kostnaden for mange andre kroniske sykdommer, for eksempel hjertesykdom ($ 12 000) og KOLS ($ 11000) .38 En studie fra 2005 fant at pasienter med ikke-cystisk fibrose bronkiektasi i gjennomsnitt hadde 2,0 ekstra dager per år på sykehuset, hadde 6,1 polikliniske møter og 27,2 flere dager med antibiotikabehandling sammenlignet med pasienter uten sykdommen.9 I 2005 var behandlingskostnadene for ikke-cystisk fibrose bronkiektase $ 630 millioner årlig.5
Pasienter med ikke-cystisk fibrose bronkiektase kan ha problemer med å rydde luft ay sekresjoner og kan ha betydelig nytte av luftveisklareringsterapi.2 Målet med behandling for bronkiektasi er å mobilisere luftveisekresjoner for å redusere betennelse, forhindre luftveisinfeksjoner, forbedre ventilasjon, minimere antall forverringer og forbedre pasientens livskvalitet. 10-12 En rekke terapeutiske metoder brukes for tiden for å fjerne luftveisekresjoner hos pasienter med lungesykdom, nedsatt luftveisslimhemming, eller som har risiko for å utvikle en av disse tilstandene.8 Disse metodene tar generelt sikte på å fremme sekresjonsklarering ved å redusere slimviskositet og bruk av skjærkrefter for å frigjøre slim fra lungeveggen for å lette mobilisering for å lette oppspytt. Omsorgsstandard innebærer kombinasjonsbehandling med mucolytiske og mucokinetiske midler, bronkodilatatorer, betennelsesdempende terapi og en eller annen form for fysisk / mekanisk clearance av luftveisbehandling.2 Luftveisklareringsterapi spiller en kritisk rolle da det hjelper til å unngå oppbevaring av patogenbelagt slim som er den underliggende opprinnelsen til tilbakevendende infeksjon som forårsaker progressiv lungeforverring.2,13,14 Luftveisklaringsmetoder spiller en kritisk rolle for å opprettholde respiratorisk helse gjennom hele pasientens levetid.
Et antall luftveisklarering metoder er tilgjengelige, inkludert fysioterapi på brystet, masker med positivt endepiratorisk trykk, orale høyfrekvente enheter og høyfrekvente brystveggsvingninger (HFCWO) .2 Positive endepiratoriske trykkmasker og orale høyfrekvente enheter krever aktiv innsats, mestring av teknikk og / eller fysisk smidighet som kan begrense bruken av dem.2
HFCWO brukes til luftveisklarering hos pasienter med et bredt spekter av luftveiskompromittering ng sykdommer og tilstander, inkludert genetiske og immunologiske forstyrrelser, nevromuskulære sykdommer og obstruktive lungesykdommer, slik som astma og KOLS. teknikk for å være effektiv.2 Kliniske studier, primært hos pasienter med cystisk fibrose, har vist HFCWO å være trygg og effektiv.2,15,19-22 HFCWO leverer kompresjonsimpulser til brystveggen gjennom en oppblåsbar vest koblet til en luftpulsgenerator .2 Generatoren produserer en vekslende luftstrøm inn i og ut av vesten som raskt komprimerer og frigjør brystveggen innenfor et utvalg av valgbare frekvenser og trykk. Den oscillerende kompresjon som er gitt til brystveggen har blitt rapportert å tynn tyktflytende slim, koble slim fra lungeveggen og drive slim fra de mindre luftveiene i lungene mot de store luftveiene der det kan ekspektoreres eller suges bort.2,23, 24 HFCWO kan føre til signifikant forbedring i lungevolumet på 15 til 57 ml og i strømning opp til 1,6 liter / sek. 22
En tidligere case review-studie evaluerte de kliniske resultatene av SmartVest® Airway Clearance System-terapi ved forverring -relatert helseutnyttelse og medisinering hos pasienter med ikke-cystisk fibrose bronkiektasi.25 Studien fant at bruken av SmartVest resulterte i en statistisk signifikant 60% reduksjon i bronkiektaserelaterte forverringer inkludert bruk av antibiotika, akuttmottak (ED) og sykehusinnleggelser . Den nåværende studien er designet for å vurdere den økonomiske effekten av SmartVest-terapi på bronkiektaserelaterte helsetjenester og antibiotikakostnader.
Metoder
En nylig SmartVest (Electromed, Inc., New Prague, MN , USA) case review resultatbasert klinisk studie tjente som grunnlag for denne analysen.25 Studien registrerte alle bronkiektaserelaterte forverringer for å inkludere antall sykehusinnleggelser, ED-besøk og antibiotikabruk i ett år før SmartVest-bruk (standard omsorgskontroll) og til sammenligning i ett år etter starten av SmartVest-bruk (behandling). Studien inkluderte bare de forsøkspersonene med en diagnose av ikke-cystisk fibrose bronkiektase som hadde brukt SmartVest i minst ett år, og hvis medisinske journaler var tilgjengelige i ett år før oppstart av SmartVest-behandling. Pasienter ble ekskludert hvis de ikke hadde fulgt det foreskrevne SmartVest-terapiregimet, ikke kunne bli kontaktet via telefon eller hadde utløpt. Alle data som ble samlet inn før SmartVest-bruk, ble registrert via pasientens medisinske journaler.
Pasientens medisinske journaler ble gjennomgått for alle bronkiektaserelaterte forverringer som skjedde i løpet av ett års periode før SmartVest-behandlingen startet. Emner ble kontaktet og intervjuet per telefon for å samle bronkiektaserelaterte forverringer i ettårsperioden etter at SmartVest-behandlingen startet. Spørreskjemaet for telefonundersøkelsen ble utviklet for det eksklusive formålet med studien. Under telefonintervjuet ble emnet stilt spesifikke spørsmål angående respiratorisk relatert antibiotikabruk, ED-besøk og sykehusinnleggelser. Intervjuet spurte også om pasienten brukte SmartVest i henhold til legens reseptregime.
Antibiotikakostnadene ble bestemt ved hjelp av «on-line rabatt apotekpriser», men kostnadene for kontorbesøk og legeavgifter var ikke inkludert. Innleggelser på sykehus og ED ble bestemt ved hjelp av de vektede nasjonale estimatene fra Healthcare Cost and Utilization Project (HCUP) National Inpatient Sample (NIS), 2013, Agency for Healthcare Research and Quality (AHRQ), basert på data samlet inn av de enkelte stater og gitt til AHRQ av statene. 26 NIS-databasen inkluderer et lagdelt sannsynlighetsutvalg av sykehus fra statlige sykehusdatabaser som inkluderer sykehusinnleggelser av pasienter med Medicare, Medicaid, privat forsikring og uforsikrede.27 NIS inneholder data fra 5 til 8 millioner sykehusopphold fra ca. 1000 sykehus. Det er beregnet til å tilnærme et utvalg på 20% av amerikanske ikke-føderale, kortvarige sykehus som definert av American Medical Associ ation. NIS er hentet fra stater som deltar i Healthcare Cost and Utilization Project. NIS inneholder enhetlige innleggelsesdata fra sykehusutslippsdatabaser vedlikeholdt av statlige etater, sykehusforeninger og andre private organisasjoner. Totalt antall vektede utslipp i USA basert på HCUP NIS var 35 597 792,28
Resultater
Gjennomgang av HCUP- og Medicare-databaser avslørte tilknyttede helsekostnader for en bronkiektaserelatert forverring
å være $ 450 (2012) for et ED-besøk og $ 9 300 (2010) for en sykehusinnleggelse med lungebetennelse. Utvidet sykehusopphold basert på komplikasjoner eller komorbiditeter ble ikke beregnet. Ved å bruke online beregningspriser for apotekpriser var kostnaden for et standard antibiotikakur for lungebetennelse $ 290 (2016). Legeavgift for et kontorbesøk og etterfølgende resept var ikke tilgjengelig for beregning.
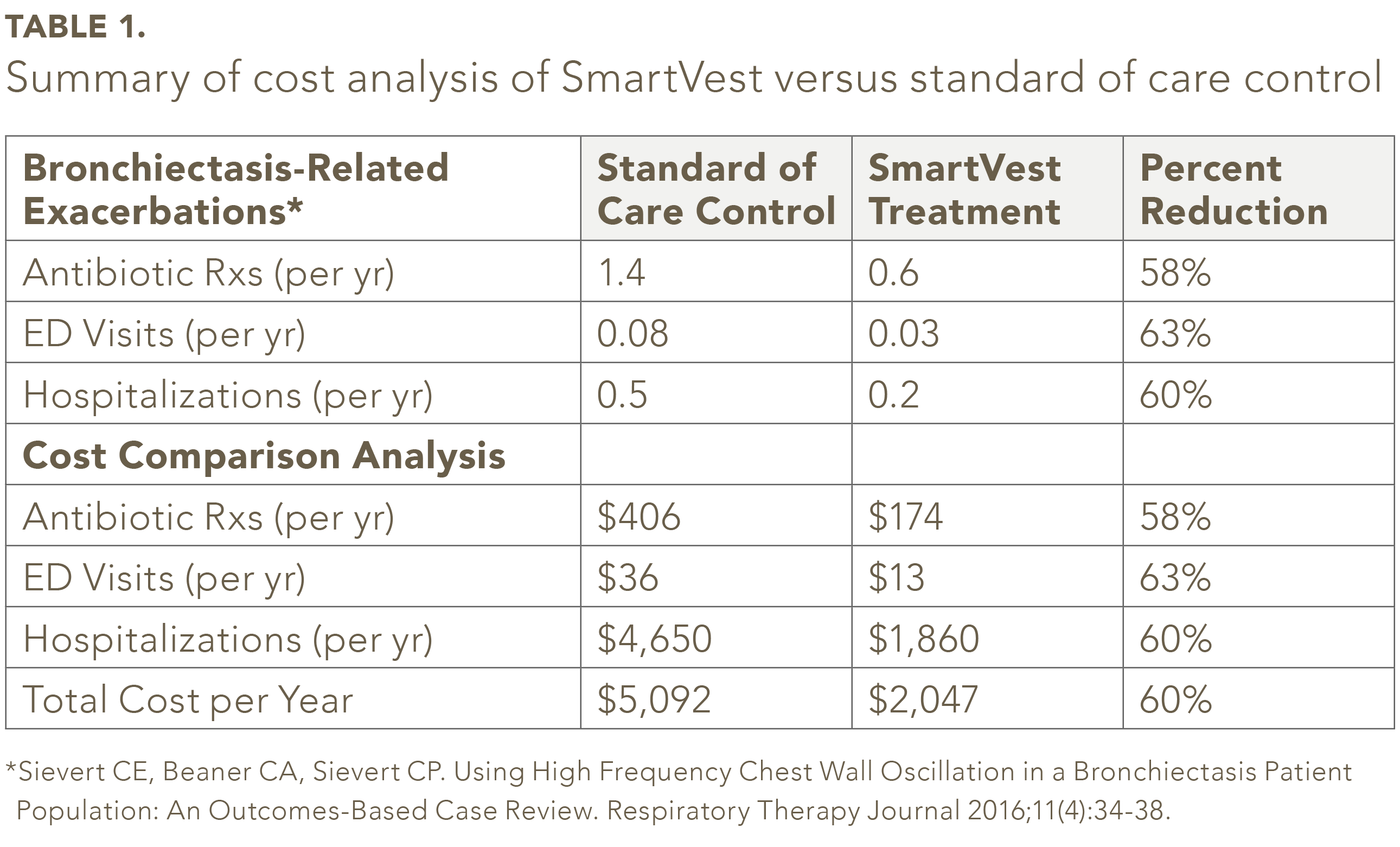
Av de 104 identifiserte SmartVest-pasientene med bronkie, oppfylte 59 pasienter kriteriene for inklusjon / eksklusjon.25 I studiepopulasjonen var det gjennomsnittlige antallet av antibiotikaresepter per år var 58% mindre for SmartVest (0,6 / år) sammenlignet med standard omsorgskontroll (1,4 / år) (se tabell 1). SmartVest-bruk reduserte også ED-besøk betydelig med 63% (0,08 / år vers 0,03 / år) og sykehusinnleggelser med 60% (0,5 / år vers 0,2 / år). De årlige kostnadene per pasient for antibiotika for pasienter behandlet med SmartVest var rundt $ 233 lavere sammenlignet med de som ble behandlet med standardomsorg (se tabell 1). Sykehusinnleggelser, etter ett års bruk av SmartVest, ble også redusert betydelig med $ 2 790 per pasient per år. Totalt viste de samlede resultatene en årlig besparelse på 3 045 dollar per pasient per år med SmartVest-bruk.
Analysen gjorde ikke redegjøre for eventuelle lege- / kontoravgifter som er pådratt for å få resept på antibiotika uten sykehusinnleggelse. Analysen tok heller ikke hensyn til et kontorbesøk for en potensiell forverring som ikke resulterte i resept eller sykehusinnleggelse. I tillegg redegjorde ikke analysen for ekstra utgifter hvis forverringen var en antibiotikaresistent bakteriestamme lungebetennelse som angivelig kan koste mer enn $ 15 000 for hver episode.
Diskusjon
Formålet med analysen var å evaluere den økonomiske effekten av SmartVest-bruk på medisinske kostnader forbundet med bronkiektase sammenlignet med en standard for pleiekontroll. Så vidt vi vet er dette den første studien som vurderer helsekostnadene ved behandling av ikke-cystisk fibrose bronkiektasepasienter med HFCWO.Samlet kostnad inkluderte kostnadene ved antibiotika, ED-besøk og sykehusinnleggelser relatert til forverringer assosiert med ikke-cystisk fibrose bronkiektase. Studien viste en signifikant reduksjon i helseutnyttelsen og de tilhørende kostnadene da pasienter med bronkiektasi ble behandlet med SmartVest i ett år. Den totale kostnaden ble redusert med 60%, noe som tilsvarer en besparelse på $ 3,045 per pasient per år.
En nylig studie som evaluerte sykehusutskrivninger, reinnleggelser og ED-besøk for KOLS eller bronkiektase hos voksne i USA funnet fra 2001 til 2012 økte antall sykehusutslipp med 88 000,31 Studien fant også at omtrent 7% av pasientene med KOLS eller bronkieektase ble reinnlagt innen 30 dager med KOLS eller bronkiektase som hoveddiagnosen.31 I motsetning til dette reduserte utslippshastigheten for andre sykdommer.31 Årsaken til den betydelige økningen i KOLS- og bronkiektasis sykehus- og ED-besøk er ikke klar ettersom det er observert en signifikant nedgang i røyking. Det kan imidlertid gjenspeile potensialet under diagnosen av sykdommen og den langsiktige karakteren av KOLS og bronkiektase i en aldrende befolkning.31
En tidligere case review resultatbasert studie rapporterte at SmartVest brukte reduserte sykehusinnleggelser 1,5 ganger, 25 som indikerer kostnadsfordelen med HFCWO ved å redusere belastningen på helsevesenet. Andre studier har også evaluert faktorer (både system og pasient) som kan redusere reinnleggelse hos pasienter med KOLS, og er, i det minste delvis, relevante for pasienter med bronkiektase. Disse faktorene inkluderer kontinuitet med pasientens primærhelsetjeneste eller pulmonolog, utskrivningskoordinatorintervensjon og omfanget eller typen respiratorisk terapi.32-34
Reduksjon i antall bronkiektaserelaterte forverringer kan også påvirke en pasientens livskvalitet.35,36 I en populasjon av pasienter med KOLS var bruk av SmartVest assosiert med signifikant forbedring i fem-symptom-poenget P = 0,002 (vurdering av sputum, hvesing, hoste, kortpustethet og treningstoleranse ) .36 SmartVest-behandling viste også en signifikant forbedring i St. George’s Respiratory Questionnaire (SGRQ) P = 0,02, mens det ikke ble observert noen forbedring hos pasienter som ble behandlet med konvensjonell behandling.36 Tilsvarende fant vår tidligere saksomtale resultatbasert studie at 68 % av fagene indikerte under telefonsamtalen at bruken av SmartVest hadde forbedret livskvaliteten betydelig.25
Flere begrensninger i studiedesignet bør vurderes rød når du tolker resultatene. Pasientstørrelsen på studien var liten, og sykehusinnleggelsene, ED-besøk og antibiotikabruk etter initiering av SmartVest-terapi ble først og fremst innhentet gjennom pasientintervju. Studien kan betraktes som konservativ på grunn av at det ikke er lagt til noen kostnad for legegebyr som er knyttet til et kontorbesøk, noe som resulterer i en antibiotikaresept, eller at det ikke er lagt til noen kostnad for et kontorbesøk som ikke resulterte i et antibiotikaresept. I tillegg kan avhengighet av HCUP-, NIS- og AHRQ-databaser, som avhenger av diagnosene som er angitt på krav, være kodet feil eller ikke kodet i det hele tatt, og derved potensielt innføre målefeil med hensyn til ICD-9-CM-baserte variabler. / p>
Å redusere helseutnyttelseskostnadene som antibiotikabruk, ED-besøk og sykehusinnleggelser er prioriterte mål i nylige helsedirektiv som Affordable Care Act (ACA). For eksempel har ACA etablert sykehusreinnleggelsesreduksjonsprogrammet (HRRP), som har pålagt CMS å straffe sykehus ved å redusere refusjonsbetalinger for overflødig pasientinnleggelser for samme tilstand. HRRP identifiserte opprinnelig de tre beste «gjeldende forholdene» for fokusert gjenopptaksmåling for å inkludere akutt hjerteinfarkt, hjertesvikt og lungebetennelse. I tillegg avsluttet CMS nylig utvidelsen av ytterligere gjeldende forhold som begynte med regnskapsåret 2015 for å inkludere pasienter som ble tatt opp for en akutt forverring av KOLS. Den signifikante reduksjonen i helsetjenester og sykehusinnleggelser for ikke-cystisk bronkiektasepasienter som bruker SmartVest, som vist i denne studien og andre, kan spille en kritisk rolle for å hjelpe sykehus med å redusere reinnleggelser og dermed ikke bli straffet.
For pasienter som har luftveisinfeksjoner som er motstandsdyktige mot orale antibiotika, er belastningen mye større og mer alvorlig. Intravenøs antibiotika kompliserer omsorg sterkt fordi sykehusinnleggelse eller hjemmeovervåkning er nødvendig. Behandling for disse pasientene inkluderer plassering av et sentralt venekateter, koordinering av dosene medikamenter som ofte må gis flere flere ganger per dag, regelmessige blodprøver for å overvåke bivirkninger og måling av blodnivået av antibiotika i mange dager, trinn som blir dyre og forstyrrer pasientenes liv.
Verdens helseorganisasjon (WHO) har erklært at mikrobiell resistens mot antibiotika utgjør en «stor global trussel med ødeleggende implikasjoner for folkehelsen.» Antimikrobiell resistens truer effektiv forebygging og behandling av et stadig økende utvalg av infeksjoner forårsaket av ikke bare bakterier, men også virus og sopp. De amerikanske sentrene for sykdomsbekjempelse og forebygging (CDC) anser antimikrobiell resistens som en av deres største bekymringer og prioriteringer. Bare i USA blir minst 2 millioner mennesker smittet med bakterier som er resistente mot antibiotika, og minst 23.000 mennesker dør hvert år som et direkte resultat av disse infeksjonene.39 Som svar på den verdensomspennende bekymringen, US Centers for Medicare & Medicaid Services (CMS) ga nylig ut en foreslått regelendring av sine vilkår for deltakelse, som blant annet vil kreve at sykehus gjennomfører antibiotikastyringsprogrammer for å delta i Medicare- og Medicaid-programmene. Antibiotikastyring inkluderer forbedring av pasientens resultater ved å vedta prosesser og prosedyrer som reduserer forekomsten av infeksjoner med pa særlig oppmerksomhet mot lungebetennelse som forebyggende behandling. Som en sekundær fordel for resultatene av denne studien, kan en betydelig reduksjon i behovet for antibiotika hos bronkiektasipasienter ved bruk av SmartVest ha enda større fordeler enn å redusere kostnadene. En tilgjengelig behandling som kunne redusere luftveisinfeksjoner betydelig og dermed behovet for antibiotika, passer godt inn i sykehusets infeksjonskontrollprogrammer. bronkiektasi, 25 og den signifikante reduksjonen i antibiotikakostnader, ED og sykehusinnleggelse observert i denne studien støtter kostnadsfordelen ved bruk av SmartVest og argumenterer for forsikringsdekning av SmartVest av betalere. Videre kan sekundære fordeler som potensialet for å redusere sykehusinnleggelser og potensialet for innvirkning på å avskrekke antibiotikaresistens ha enda større fordeler enn å redusere kostnadene.
Last ned studieteksten
Anerkjennelser
Forfatterne vil takke Elizabeth Goodwin PhD for redaksjonell støtte.
- King P. Pathogenesis of bronchiectasis. Paediatr Respir Rev 2011; 12 (2): 104-110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Høyfrekvent brystkompresjon: en praktisk terapi for pasienter med bronkiektase. Respiratory Therapy 2008; 3 (1): 22-26.
- Patel IS, Vlahos I, Wilkinson TM, et al. Bronkiektase, forverringsindekser og betennelse ved kronisk obstruktiv lungesykdom. Am J Respir Crit Care Med 2004; 170 (4): 400-407. 10.1164 / rccm.200305-648OC
- Gono H, Fujimoto K, Kawakami S, et al. Evaluering av tykkelse på luftveiene og luftfangst ved HRCT ved asymptomatisk astma. Eur Respir J 2003; 22 (6): 965-971.
- Weycker D, Edelsberg J, Oster G, et al. Utbredelse og økonomisk byrde ved bronkiektase. Klinisk lungemedisin 2005; 12 (4): 205-209.
- Seitz AE, Olivier KN, Adjemian J, et al. Trender innen bronkiektasi blant medisinmottakere i USA, 2000 til 2007. CHEST Journal 2012; 142 (2): 432-439.
- Seitz AE, Olivier KN, Steiner CA, et al. Trender og byrder ved bronkiektaseassosierte sykehusinnleggelser i USA, 1993-2006. Bryst 2010; 138 (4): 944-949. 10.1378 / chest.10-0099
- Seitz AE, Olivier KN, Steiner CA, et al. Trender og byrder ved bronkiektaseassosierte sykehusinnleggelser i USA, 1993-2006. CHEST Journal 2010; 138 (4): 944-949.
- Weycker D, Edelsberg J, Oster G, et al. Utbredelse og økonomisk byrde ved bronkiektase. Klinisk lungemedisin 2005; 12: 205-209.
- Fibrose. AoCPiC. Omsorgsstandarder og god klinisk praksis for behandling av fysioterapi ff cystisk fibrose 2011. Tilgjengelig fra: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio 11. juni. pdf.
- O’Donnell AE. Bronkiektase. Bryst 2008; 134 (4): 815-823. 10.1378 / chest.08-0776
- Barker AF. Bronkiektase. N Engl J Med 2002; 346 (18): 1383-1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Ikke-farmakologiske clearance luftveier: ACCP evidensbaserte retningslinjer for klinisk praksis. Bryst 2006; 129 (1 Suppl): 250S-259S. 10.1378 / chest.129.1 suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Behandling av slimhinnedysfunksjon. Bryst 1996; 110 (4): 1048-1057.
- Arens R, Gozal D, Omlin KJ, et al. Sammenligning av høyfrekvent brystkompresjon og vanlig brystfysioterapi hos sykehuspasienter med cystisk fibrose. Am J Respir Crit Care Med 1994; 150 (4): 1154-1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Høyfrekvent svingning i luftveiene og brystveggen. Respir Care 2002; 47 (7): 797-807.
- Hansen LG, Warwick WJ.Høyfrekvent brystkompresjonssystem som hjelper til med å fjerne slim fra lungene. Biomed Instrum Technol 1990; 24 (4): 289-294.
- Lange DJ, Lechtzin N, Davey C, et al. Høyfrekvent svingning i brystveggen i ALS: en undersøkende randomisert, kontrollert studie. Nevrologi 2006; 67 (6): 991-997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. Den langsiktige effekten av høyfrekvent brystkompresjonsterapi på lungekomplikasjoner av cystisk fibrose. Pediatr Pulmonol 1991; 11 (3): 265-271.
- Kluft J, Beker L, Castagnino M, et al. En sammenligning av bronkial dreneringsbehandling ved cystisk fibrose. Pediatr Pulmonol 1996; 22 (4): 271-274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P
- Scherer TA, Barandun J, Martinez E, et al. Effekt av høyfrekvent oral svingning av luftveiene og brystveggen og konvensjonell fysioterapi på brystet på slimløsningen hos pasienter med stabil cystisk fibrose. Bryst 1998; 113 (4): 1019-1027.
- Nicolini A, Cardini F, Landucci N, et al. Effektivitet av behandling med høyfrekvent svingning i brystveggen hos pasienter med bronkiektase. BMC Pulm Med 2013; 13: 21. 10.1186 / 1471-2466-13-21
- Osman LP, Roughton M, Hodson ME, et al. Kortsiktig komparativ studie av høyfrekvente svingninger i brystveggen og europeiske luftveisklareringsteknikker hos pasienter med cystisk fibrose. Thorax 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Høyfrekvent assistert luftveisklarering. Respir Care 2007; 52 (9): 1224-1235; diskusjon 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Bruke høyfrekvent oscillasjon av brystveggen i en pasientpopulasjon med bronkiektase: En resultatbasert saksgjennomgang. Respiratory Therapy Journal 2016; 11 (4): 34-38.
- HCUP. Oversikt over Nationwide Emergency Department Sample (NEDS) 2016. Tilgjengelig fra: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Oversikt over nasjonale (landsdekkende) inneprøver. Tilgjengelig fra: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C. Kostnader for sykehusopphold i USA, 2010: Statistical Brief # 146. Helsekostkostnad og utnyttelsesprosjekt (HCUP) Statistiske briefinger. Rockville (MD): Agency for Healthcare Research and Quality (US); 2006.
- Stein PD, Matta F. Kostnader ved akuttmottaksbesøk og sykehusinnleggelser for pulmonal arteriell hypertensjon.
J Epidemiol Public Health Rev 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Refusjon for overgangsomsorgsledelse for å redusere KOLS-reinnleggelse. Brystet 2014, 145 (1): 149-155. 10.1378 / chest.13-0787
- Ford ES. Sykehusutslipp, reinnleggelser og ED-besøk for KOLS eller bronkiektasi blant amerikanske voksne: funn
fra det landsdekkende døgnprøven 2001-2012 og Nationwide Emergency Department Sample 2006-2011. Bryst 2015; 147 (4): 989-998. 10.1378 / chest.14-2146 - Sharma G, Kuo YF, Freeman JL, et al. Poliklinisk oppfølgingsbesøk og 30-dagers akuttmottaksbesøk og reinnleggelse hos pasienter innlagt på grunn av kronisk obstruktiv lungesykdom. Arch Intern Med 2010; 170 (18): 1664-1670. 10.1001 / archinternmed.2010.345
- Lainscak M, Kadivec S, Kosnik M, et al. Utslippskoordinatorintervensjon forhindrer sykehusinnleggelser hos pasienter med KOLS: en randomisert kontrollert studie. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O, Sewell L, Morgan MD, et al. Kort poliklinisk lungerehabiliteringsprogram reduserer reinnleggelse etter sykehusinnleggelse for en forverring av kronisk obstruktiv lungesykdom. Respirologi 2013; 18 (7): 1063-1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. Langvarig luftfuktningsterapi er kostnadseffektiv for pasienter med moderat eller alvorlig kronisk obstruktiv lungesykdom eller bronkiektase. Verdihelse 2014; 17 (4): 320-327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. En pilotstudie av virkningen av høyfrekvent svingning i brystveggen hos pasienter med kronisk obstruktiv lungesykdom med slimhypersekresjon. Int J Chron Obstruct Pulmon Dis 2011; 6: 693-699. 10.2147 / KOLS. S22896.
- Martınez-Garcıa MA, et al. Prognostisk verdi av bronkiektase hos pasienter med moderat til alvorlig kronisk obstruktiv lungesykdom. Am J Respir Crit Care Med 2013; Vol. 187, utg. 8, s 823–831.
- O’Donnell AE. Bronkiektase. Bryst 2008; 134: 815–82.
- Senter for sykdomsbekjempelse og forebygging – Antibiotisk / antimikrobiell motstandsside https://www .cdc.gov / drugresistance /