Tidsskrifter | Retningslinjer | Tillatelse Gastroenterology Research
Forutsigbarhet av gastrisk tarmmetaplasi av Mottled Patchy Erythema Sett ved endoskopi
Naoyoshi Nagataa, g, Takuro Shimbob, Junichi Akiyamaa, Ryo Nakashimaa, Hyung Hun Kimc, Takeichi Yoshidad, Kazufusa Hoshimotoe, Naomi Uemuraf
aDepartment of Gastroenterology and Hepatology, National Center for Global Health and Medicine (NCGM), Tokyo, Japan
bDepartment of Clinical Research and Informatics International Clinical Research Center Research Institute, NCGM, Tokyo, Japan
cDivision of Internal Medicine, Kosin University College of Medicine, Busan, Korea
dDepartment of Gastroenterology and Hepatology, Wakayama Medical University, Wakayama, Japan
eDepartment of Clinical Laboratory Pathological Division, NCGM, Tokyo, Japan
fDepartment of Gastroenterology and Hepatology, NCGM, Kohnodai Hospital, Chiba, Japan
gTilsvarende forfatter: Naoyoshi Nagata, Institutt for G astroenterology and Hepatology, National Center for Global Health and Medicine, 1-21-1 Toyama, Shinjuku-ku, Tokyo 162-8655, Japan
Manuskript akseptert for publisering 26. september 2011
Kort tittel: Endoskopisk diagnose av tarmmetaplasi
doi: https://doi.org/10.4021/gr357w
- Abstrakt
- Innledning
- Metoder
- Resultater
- Diskusjon
| Abstrakt | ▴Topp |
Bakgrunn: Tarmmetaplasi (IM) betraktes som en premalignant lesjon. Imidlertid har endoskopisk diagnose av IM blitt ansett som vanskelig. Ved hjelp av endoskopi fant vi et unikt mønster av erytem, «Mottled Patchy Erythema (MPE)», som inkluderer alvorlig IM. Helicobacter pylori (Hp) -infeksjon i seg selv kan forårsake erytem, som gjenspeiler histologiske endringer i mageslimhinnen. Derfor registrerte vi Hp-utryddelse pasienter for å validere forholdet mellom MPE og patologiske funn.
Metoder: Vi registrerte pasienter med kronisk gastritt som gjennomgikk vellykket Hp-utrydding minst 6 måneder før studien. Vi definerte MPE som flere flate eller deprimerte erytematøse lesjoner. Når vi møtte MPE ved endoskopi, utførte vi biopsi på både MPE-stedet og ikke-MPE-stedet. Non-MPE-stedet ble definert som et tilstøtende slimhinne som ligger innen 3 cm fra MPE-stedet. Alle biopsiprøver ble evaluert immunhistokjemisk for IM-undertype ved bruk av MUC2, MUC5AC, MUC6, CD10 og CDX2 flekker. Graden av IM ble definert i henhold til det oppdaterte Sydney-systemet. Diagnostisk nøyaktighet av MPE-funn for patologisk IM ble beregnet. forholdet mellom MPE og IM-undertype ble også vurdert.
Resultater: Totalt 102 pasienter ble valgt til studien. Av disse hadde 55 (54%) pasienter MPE. Biopsiprøver ble tatt fra MPE-stedene og ikke-MPE-steder fra disse 55 pasientene. IM-prosenter og medianpoeng for IM var begge signifikant høyere på MPE-stedene (P < 0,001) enn på ikke-MPE-stedene. Følsomheten og spesifisiteten for MPE ved påvisning av histologisk IM var henholdsvis 72,7% og 84,1%. Ingen signifikante assosiasjoner ble observert i ekspresjonen av MUC2, MUC5AC, MUC6, CD10 og CDX2 mellom MPE-stedene og ikke-MPE-stedene. Det var ingen signifikante forskjeller i forholdstallene (fullstendig / ufullstendig) av IM-undertyper mellom de to gruppene.
Konklusjoner: MPE er et nyttig endoskopisk funn for å oppdage histologisk IM uten bruk av kromendoskopi og forstørrende endoskopi. Imidlertid er IM-undertypen vanskelig å identifisere. I epoken med Hp-utryddelse har MPE potensialet til å bli et prediktivt funn for risikoen for magekreft.
Nøkkelord: Tarmmetaplasi; Premalignant lesjon; Endoskopisk funn; Erytem; Endoskopi med hvitt lys; Undertype, utryddelse; Helicobacter pylori
| Innledning | ▴Topp |
Det antas at utvikling av magekreft involverer en flertrinnsprosess, inkludert Helicobacter pylori (Hp) -infeksjon, kronisk gastritt, kjertelatrofi, intestinal metaplasi (IM) og til slutt dysplasi. IM og gastrisk atrofi anses sammen for å være risikofaktorer for utvikling av magekreft av tarmtypen og betraktes som premalignante lesjoner.Gastrisk atrofi kan gjenkjennes ved endoskopi og korrelerer med histologisk evaluering. Imidlertid har diagnosen IM ved bruk av endoskopi med hvitt lys blitt ansett å være vanskelig på grunn av at IM mangler forskjell i farge og dens tilstedeværelse som flere flate lesjoner.
Nylig , fant vi at et unikt erytematøst funn ved endoskopi kunne observeres selv etter Hp-utryddelse. Vi beskriver dette funnet som «Mottled Patchy Erythema (MPE).» MPE kan gjenkjennes som flere flate eller lett deprimerte erytematøse lesjoner under standard endoskopi med hvitt lys; patologisk inkluderer den alvorlig IM. Hp-infeksjon i seg selv kan forårsake erytem, sett ved endoskopi, som gjenspeiler histologiske endringer som infiltrasjon av inflammatoriske celler og ødem. , vi registrerte pasienter som gjennomgikk Hp-utryddelse for å validere forholdet mellom MPE og patologiske funn.
| Metoder | ▴Topp |
Pasientvalg
Pasienter med kronisk gastritt som gjennomgikk vellykket Hp-utrydding minst 6 måneder før studien, ble prospektivt registrert for studien ved National Center for Global Health and Medicine (NCGM) mellom januar 2008 og desember 2008. Eksklusjonskriterier i utelukket bruken av ikke-steroide antiinflammatoriske legemidler (NSAIDs), antacida og antitrombotiske medikamenter i løpet av de fire ukene før endoskopi. Vi ekskluderte også pasienter med en historie med gastrisk kirurgi, hemorragisk sykdom, levercirrhose, nyresvikt, hjertesvikt og tidlig eller avansert magekreft. Skriftlig informert samtykke ble innhentet fra deltakerne i samsvar med Helsinki-erklæringen og den etterfølgende revisjonen. Studieprotokollen ble godkjent av NCGMs etiske komité.
Helicobacter pylori-utryddelse
Pasienter med kronisk gastritt og magesårssykdom indusert av Hp-infeksjon gjennomgikk utryddingsterapi. Pasientene ble behandlet med et 7-dagers regime bestående av amoxicillin, klaritromycin og en protonpumpehemmere (PPI) to ganger daglig, som var standard førstelinjeregime godkjent i Japan. Hvis utryddelse ikke lyktes, ble det gitt et annet regime bestående av amoksicillin, metronidazol og PPI. Utryddelse ble bekreftet ved negativ histologisk undersøkelse av gastriske biopsier, sammen med en negativ 13C-urea-pustetest (13C-UBT) 2 til 3 måneder etter fullført utryddingsterapi. Når alle testene var negative, ble en pasient definert som negativ for Hp-infeksjon.
Endoskopisk vurdering
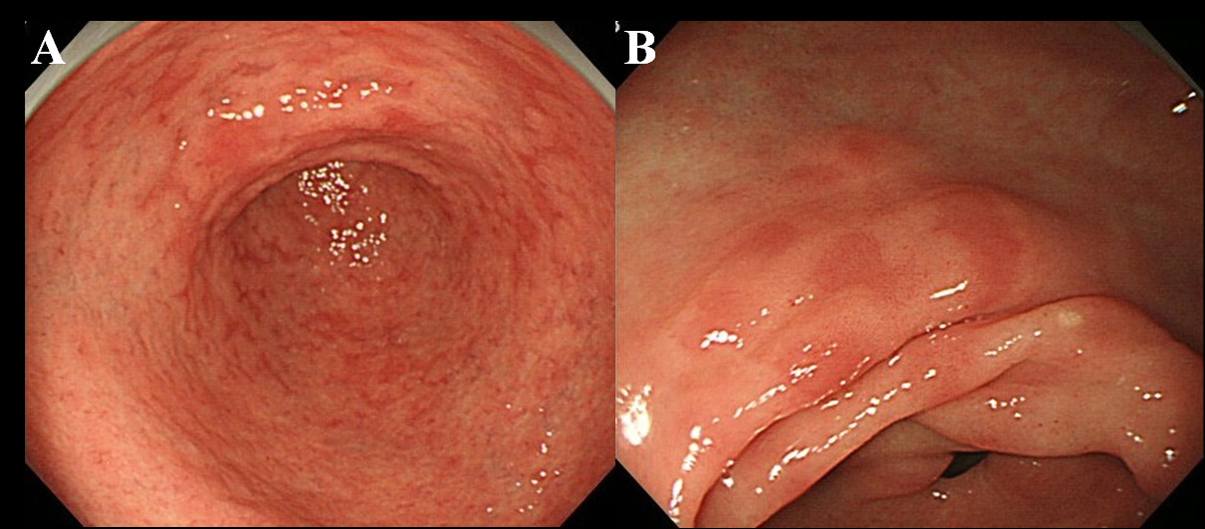
Minst 6 måneder etter utryddelsen av Hp, gjennomgikk pasienter endoskopisk undersøkelse. Vi brukte et høyoppløselig endoskop uten forstørrelse (Olympus videoscope, modell GIF-H260) for å observere tilstedeværelsen av MPE i mageslimhinnen. Vi definerte MPE som flere flate eller lett deprimerte erytematøse lesjoner som kunne skilles fra overbelastet slimhinne, blødning, angioektasi, flekkaktig erytem og lineær erytem (figur 1A, B). Vi skilte også mellom MPE og rødaktig slimhinne med et regenererende epitel ledsaget av sår eller sår arr.
 Klikk for stort bilde |
Figur 1. Endoskopisk funn av MPE. (A) Flere og flate erytemer i antrumet; (B) Flat og deprimert erytem i mindre krumning i antrummet. |
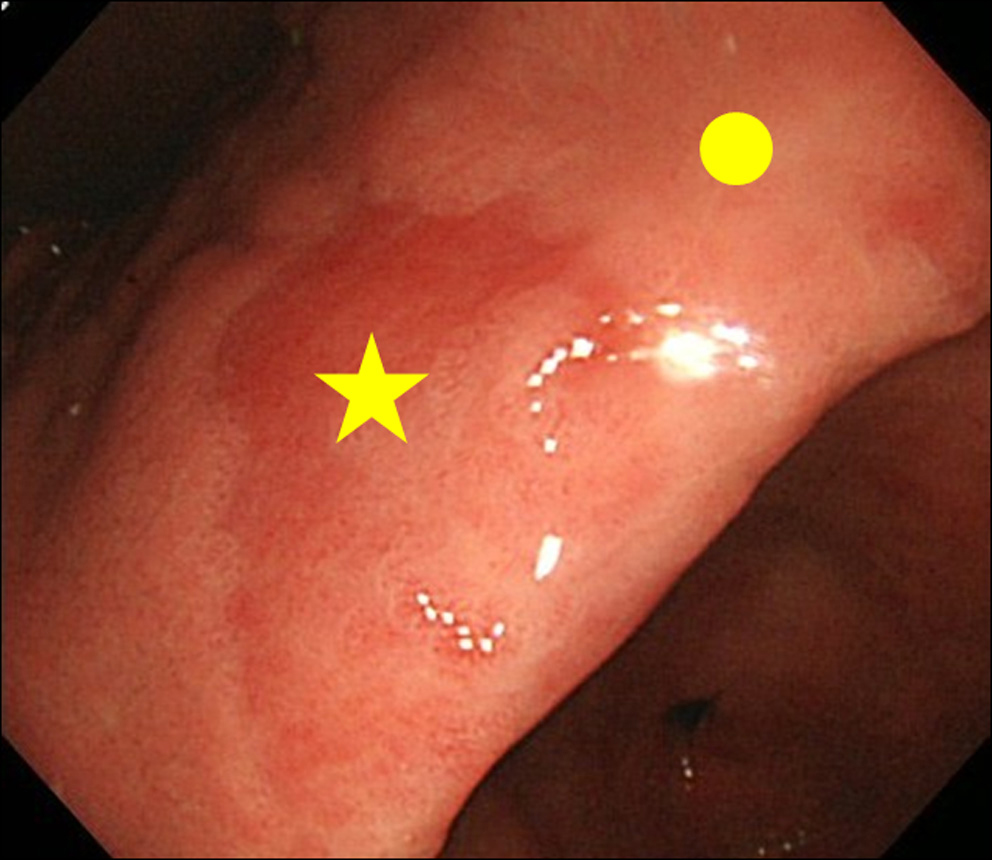
Når vi støter på et funn av MPE-funn ved endoskopi, utførte vi biopsi av både MPE-stedet og ikke-MPE-stedet. Ikke-MPE-stedet ble definert som et tilstøtende slimhinne lokalisert innen 3 cm fra MPE-stedet (fig. 2).
 Klikk for stort bilde |
Figur 2. Biopsiside. (★) Biopsiside for MPE; (•) Biopsiside for ikke-MPE. Ikke-MPE-sted ble definert som et tilstøtende slimhinne som ligger innen 3 cm fra MPE-stedet. |
Omfanget av den atrofiske grensen ble klassifisert i 3 trinn: mild, moderat og alvorlig, som definert av Kimura og Takemoto.
Histologisk vurdering
Biopsiprøver ble sendt til laboratoriet vårt, fiksert i 10% bufret formalin. Prøvene ble bearbeidet, innebygd i parafin og kuttet i 4 um seksjoner. Objektglass fra hvert eksemplar ble farget med hematoksylin-eosin (HE) (fig.3A) og immunhistokjemisk farging. De immunhistokjemiske flekkene inkluderte følgende: (1) MUC2, en markør for tarmslim som er nyttig for å oppdage begerceller (figur 3B), (2) MUC5AC, en markør for gastrisk mucin, som uttrykkes i slimete nakkeceller og foveolar epitel (fig. 3C), (3) MUC6, en markør for gastrisk mucin, som uttrykkes i slimete celler i kroppens nakkesone og pyloriske kjertler i antrum (fig. 3D), (4) CD10, en nyttig markør for å oppdage børstegrensen til tynntarmen (fig. 3E), og (5) CDX2, en markør for tilstedeværelse av IM (fig. 3F). Vi brukte CDX2 fordi nylige studier har vist at CDX2-uttrykk kunne observeres mye i IM-kjertler, og forsvant ikke etter utryddelse av Hp. Tilstedeværelsen av IM ble bekreftet av både HE og immunhistokjemisk farging.
Subtyper av IM ble klassifisert som komplette eller ufullstendige typer. Den komplette typen ble definert som redusert ekspresjon av gastrisk mucin (MUC5AC eller MUC6) og co-ekspresjon av intestinal mucin (MUC2) og CD10 (Fig. 3A-F). Den ufullstendige typen ble definert som uttrykk for gastrisk mucin (MUC5AC eller MUC6) og MUC2. Fordi det ikke finnes etablerte kriterier for å kategorisere en sak som både de komplette og ufullstendige typene i en seksjon, tildelte vi IM-undertypene som den vanligste typen.
Graden av IM ble scoret basert på det oppdaterte Sydney-systemet (0: ingen, 1: mild, 2: moderat, 3: merket).
Statistisk analyse
Vi delte pasientene i to grupper basert på om pasientene var positive eller negative for MPE. Vi brukte Student’s t-test for å sammenligne alder og periode med utryddelse. Chi-kvadrat-testen eller Fishers eksakte sannsynlighetstest ble brukt for kjønnsforhold og graden av endoskopisk atrofi i de to gruppene.
Vi sammenlignet også de histologiske funnene mellom MPE-stedene og ikke-MPE-stedene. For å sammenligne forskjellene mellom de to biopsisidene, brukte vi Wilcoxon Matched-Pairs Signed-Ranks Test for IM median score, og Fishers eksakte test for utbredelsen av IM, IM subtyper og IM fenotyper. Sensitivitet, spesifisitet, positive og negative prediktive verdier, og positive og negative sannsynlighetsforhold for MPE sett ved endoskopi for påvisning av patologisk IM ble beregnet. P-verdier < 0,05 ble ansett som signifikante. Alle statistiske analyser ble utført med Stata-programvare, versjon 10 (StataCorp LP, College Station, TX, USA).
| Resultater | ▴Topp |
Pasientkarakteristikker
I løpet av studietiden var 157 pasienter som gjennomgikk øvre endoskopi og fikk Hp-utryddelse ble gjennomgått. Vi ekskluderte 52 av de 157 pasientene fra analyse for et av følgende kriterier: bruk av syrenøytraliserende midler (31), antitrombotiske legemidler (17) eller NSAIDs (3); eller tidligere levercirrhose (5), hjertesvikt (1) eller tidlig magekreft (2). Mer enn ett utelukkelseskriterium gjaldt noen pasienter.
Totalt ble 102 pasienter valgt for analyse etter eksklusjon. Av disse var det 55 (54%) pasienter med MPE. Ingen signifikante forskjeller ble observert i gjennomsnittsalder og kjønn mellom MPE-positive og -negative pasienter (tabell 1). Det var ingen signifikante forskjeller mellom de to gruppene etter Hp-utryddelsesperioden. Imidlertid oppstod gastrisk atrofi med høyere alvorlighetsgrad (moderat til alvorlig) signifikant oftere i MPE-positiv gruppe sammenlignet med MPE-negativ gruppe (positiv 65,6% versus negativ 45,0%, P = 0,035).
 Klikk for å se |
Tabell 1. Demografiske egenskaper hos pasienter (n = 102) |
Endoskopiske funn og patologiske trekk
 Klikk for å se |
Tabell 2. Sammenligning av IM-poengsum mellom MPE og ikke-MPE-nettsted (n = 55) |
Ingen signifikante assosiasjoner ble observert i uttrykket av MUC2, MUC5AC, MUC6, C D10 og CDX2 mellom MPE-stedene og ikke-MPE-stedene (Tabell 3). Det var ingen signifikant forskjell i forholdstallene (fullstendig / ufullstendig) av IM-undertyper mellom de to gruppene (MPE: 18/30 versus ikke-MPE: 8/10, P = 0,778).
 Klikk for å se |
Tabell 3. Fenotyper og undertyper av tarmmetaplasi |
| Diskusjon | ▴Top |
I denne studien fokuserte vi på et unikt erytematøst utseende sett på endoskopi etter Hp-utryddelse. Vi kalte dette funnet «MPE», og vi fant at tilstedeværelsen av MPE sett ved endoskopi typisk var karakteristisk for patologisk IM.
Diagnosen IM med konvensjonell endoskopi har blitt ansett som vanskelig fordi IM vanligvis vises i flat slimhinne og har få morfologiske endringer. Kaminishi et al rapporterte «askefarget nodular endring» som en indikator for IM; nøyaktigheten av disse etterforskernes funn var høy, med en spesifisitet på 98-99%, men følsomheten var lav (6-12%). Kaminishi et al bemerket at konvensjonell endoskopi er mindre nyttig for å bekrefte diagnosen IM. Nyere studier har dukket opp om endoskopisk funn av IM ved å bruke forstørrende endoskopi. Det har blitt rapportert at de karakteristiske funnene fra gastriske groper sett med metylenblå kromendoskopi og det «villuslignende utseendet» sett med konfokal endoskopi har vært nyttige for diagnostisering av IM. Uedo et al rapporterte at utseendet til «en lyseblå topp» ( LBC) er et nøyaktig tegn for tilstedeværelse av IM, sett med smalbåndsbildende (NBI) forstørrende endoskopi. På grunn av de høye utstyrskostnadene og ytterligere ferdigheter og tid som kreves for nærmere undersøkelse ved bruk av spesialverktøy som NBI eller forstørrende endoskopi, er screening med dette utstyret ikke praktisk i daglig klinisk praksis. I tillegg er det en økt risiko for skade på DNA i mage-tarmslimhinnen når du bruker kromoendoskopi med metylenblått etterfulgt av hvitt lys, og krever forsiktighet ved bruk. Derfor er det mer fordelaktig å diagnostisere IM ved å finne MPE uten bruk av kromendoskopi og forstørrende endoskopi. Våre studieresultater antyder at tilstedeværelsen av IM kan diagnostiseres med standard endoskopi uten biopsi.
Hvorfor kan MPE observeres selv etter utryddelse av Hp? Dette kan tilskrives histologiske endringer i mageslimhinnen. De bemerkelsesverdige histologiske endringene etter utryddelse inkluderer forbedringer i infiltrasjonen av inflammatoriske celler, epitelial hyperplasi og ødem. De endoskopiske bildene av erytematøs og ødematøs slimhinne som ser ut til å bli forbedret gjenspeiler disse histologiske endringene. Derfor spekulerer vi i at MPE består av et gjenværende område med vedvarende erytematøs IM og et raskt gjenopprettet ikke-IM-område som følge av vellykket Hp-utryddelse. Utryddelsen av Hp førte til at kontrasten mellom MPE-området og ikke-MPE-områdene ble tydeligere. Det er imidlertid ukjent hvorfor bare MPE-stedet observeres som en erytematøs slimhinne. Det kan sannsynligvis utledes at et svært tett område av mikrokar omgir metaplastiske kjertler; dette er ikke belyst i denne studien. I tillegg var IM-poengsummen på MPE-området betydelig høyere enn poengsummen på ikke-MPE-siden. Vi spekulerer i at utseendet på erytematøs slimhinne er assosiert med tilstedeværelsen av mange metaplastiske kjertler. . Undertypene til IM er klassifisert i enten den komplette eller ufullstendige typen; dette er de mest brukte undertypene. Flere studier har vist at den komplette typen ikke utviser noen økt risiko for å utvikle karsinom, mens den ufullstendige typen er assosiert med en økt risiko for ondartet transformasjon. Imidlertid er sammenhengen mellom undertyper og risikoen for magekreft ikke allment akseptert. For tiden er det vanskelig å identifisere noen av undertypene ved hjelp av standard endoskopi.
Det er rapportert at Hp-utryddingsterapi er effektiv for å forhindre både gastrointestinalt sår og utvikling av magekreft. Denne bruken av Hp-utryddingsterapi vil sannsynligvis dukke opp i klinisk praksis i nær fremtid. Imidlertid bør det utvises forsiktighet mot risikoen for utvikling av magekreft etter Hp-utryddelse. Karakteristikkene av magekreft etter utryddelse er rapportert å inkludere patologisk alvorlig IM ved corpus og alvorlig gastrisk atrofi som oppdaget ved endoskopi. Derfor er det nødvendig å nøye observere tilstedeværelsen av IM selv etter Hp-utryddelse.
Til slutt er tilstedeværelsen av MPE ved endoskopisk undersøkelse karakteristisk for patologisk IM.Det vil være gunstig i klinisk praksis å kunne diagnostisere patologisk IM uten kromendoskopi eller forstørrende endoskopi. OED har potensial til å bli et prediktivt funn for risikoen for magekreft i epoken med Hp-utryddelse.
Anerkjennelser
Vi anerkjenner Dr. Hidenobu Watanabe og Dr. Hiroyoshi Ota for deres konsulenttjenester til denne studien angående patologiske evalueringer. Vi ønsker å uttrykke takknemlighet til Hisae Kawashiro, klinisk forskningskoordinator, for hjelp med datainnsamling.
Støtte for støtte
Dette arbeidet ble støttet av Grant of National Center for Global Health and Medicine (21-108).
Interessekonflikter
Forfatterne erklærer at de ikke har noen interessekonflikter.
| ▴Topp |
- Correa P. Human gastrisk karsinogenese: en multistap og multifaktoriell prosess — First American Cancer Society Award Lecture on Cancer Epidemiologi og forebygging. Cancer Res. 1992; 52 (24): 6735-6740.
publisert - Leung WK, Sung JJ. Gjennomgangsartikkel: intestinal metaplasia og gastrisk karsinogenese. Aliment Pharmacol Ther. 2002; 16 (7): 1209-1216.
publisert doi - Uemura N, Okamoto S, Yamamoto S, Matsumura N, Yamaguchi S, Yamakido M, Taniyama K, et al. Helicobacter pylori-infeksjon og utvikling av magekreft. N Engl J Med. 2001; 345 (11): 784-789.
pubmed doi - Kimura K, Takemoto T. En endoskopisk anerkjennelse av den atrofiske grensen og dens betydning i kronisk gastritt. Endoskopi. 1969; 1: 1-3.
- Satoh K, Kimura K, Taniguchi Y, Kihira K, Takimoto T, Saifuku K, Kawata H, et al. Biopsisteder egnet for diagnostisering av Helicobacter pylori-infeksjon og vurdering av omfanget av atrofisk gastritt. Am J Gastroenterol. 1998; 93 (4): 569-573.
publisert doi - Kaminishi M, Yamaguchi H, Nomura S, Oohara T, Sakai S, Fukutomi H, Nakahara A, et al. Endoskopisk klassifisering av kronisk gastritt basert på en pilotstudie fra Research Society for Gastritis. Fordøy Endosc. 2002; 14: 138-151.
- Rugge M, Leandro G, Farinati F, Di Mario F, Sonego F, Cassaro M, Guido M, et al. Gastrisk epitel dysplasi. Hvordan klinisk patologisk bakgrunn forholder seg til ledelse. Kreft. 1995; 76 (3): 376-382.
pubmed doi - Nagata N, Akiyama J, Uemura N. Endoskopisk diagnose av gastrisk tarmmetaplasi etter Helicobacter pylori-utryddelse. Endoskopi. 2009; 41 (suppl I): A212.
- Dixon MF, Genta RM, Yardley JH, Correa P. Klassifisering og gradering av gastritt. Det oppdaterte Sydney-systemet. International Workshop on the Histopathology of Gastritis, Houston 1994. Am J Surg Pathol. 1996; 20 (10): 1161-1181.
pubmed doi - Ho SB, Shekels LL, Toribara NW, Kim YS, Lyftogt C, Cherwitz DL, Niehans GA. Mucin-genuttrykk i normalt, preneoplastisk og neoplastisk humant gastrisk epitel. Cancer Res. 1995; 55 (12): 2681-2690.
publisert - Silva E, Teixeira A, David L, Carneiro F, Reis CA, Sobrinho-Simoes J, Serpa J, et al. Slimhinner som nøkkelmolekyler for klassifisering av tarmmetaplasi i magen. Virchows Arch. 2002; 440 (3): 311-317.
pubmed doi - Reis CA, David L, Correa P, Carneiro F, de Bolos C, Garcia E, Mandel U, et al. Tarmmetaplasi i menneskelig mage viser tydelige mønstre av mucin (MUC1, MUC2, MUC5AC og MUC6) uttrykk. Cancer Res. 1999; 59 (5): 1003-1007.
publisert - Groisman GM, Amar M, Livne E. CD10: et verdifullt verktøy for lysmikroskopisk diagnose av mikrovilløs inklusjonssykdom (familiær mikrovilløs atrofi). Am J Surg Pathol. 2002; 26 (7): 902-907.
pubmed doi - Carl-McGrath S, Lendeckel U, Ebert M, Wolter AB, Roessner A, Rocken C. Ektopeptidases CD10, CD13, CD26 og CD143 er oppregulert i magekreft. Int J Oncol. 2004; 25 (5): 1223-1232.
publisert - Bai YQ, Yamamoto H, Akiyama Y, Tanaka H, Takizawa T, Koike M, Kenji Yagi O, et al. Ektopisk uttrykk for homeodomain-protein CDX2 i tarmmetaplasi og karsinomer i magen. Kreft Lett. 2002; 176 (1): 47-55.
publisert doi - Satoh K, Mutoh H, Eda A, Yanaka I, Osawa H, Honda S, Kawata H, et al. Avvikende uttrykk for CDX2 i mageslimhinnen med og uten tarmmetaplasi: effekt av utryddelse av Helicobacter pylori. Helicobacter. 2002; 7 (3): 192-198.
pubmed doi - Dinis-Ribeiro M, da Costa-Pereira A, Lopes C, Lara-Santos L, Guilherme M, Moreira-Dias L, Lomba- Viana H, et al. Forstørrelseskromoendoskopi for diagnose av gastrisk tarmmetaplasi og dysplasi. Gastrointest Endosc. 2003; 57 (4): 498-504.
publisert doi - Areia M, Amaro P, Dinis-Ribeiro M, Cipriano MA, Marinho C, Costa-Pereira A, Lopes C, et al. Ekstern validering av en klassifisering for metylenblå forstørrelseskromoendoskopi i premaligne magesår. Gastrointest Endosc. 2008; 67 (7): 1011-1018.
publisert doi - Yang JM, Chen L, Fan YL, Li XH, Yu X, Fang DC. Endoskopiske mønstre av mageslimhinne og dens klinisk-patologiske betydning. Verden J Gastroenterol. 2003; 9 (11): 2552-2556.
publisert - Uedo N, Ishihara R, Iishi H, Yamamoto S, Yamada T, Imanaka K, Takeuchi Y, et al. En ny metode for diagnostisering av mage-tarmmetaplasi: smalbåndsavbildning med forstørrende endoskopi. Endoskopi. 2006; 38 (8): 819-824.
publisert doi - Kiesslich R, Jung M. Forstørrelse endoskopi: forbedrer det analyse av slimhinneoverflaten for diagnostisering av gastrointestinale neoplasier ?. Endoskopi. 2002; 34 (10): 819-822.
pubmed doi - Olliver JR, Wild CP, Sahay P, Dexter S, Hardie LJ. Kromendoskopi med metylenblått og tilhørende DNA-skader i Barretts spiserør. Lancet. 2003; 362 (9381): 373-374.
pubmed doi - Oda Y , Miwa J, Kaise M, Matsubara Y, Hatahara T, Ohta Y. Fem års oppfølgingsstudie på histologiske og endoskopiske endringer i mageslimhinnen etter Helicobacter pylori-utryddelse. Dig Endosc. 2004; 16: 213-18.
- Tepes B, Kavcic B, Zaletel LK, Gubina M, Ihan A, Poljak M, Krizman I. To til fire år histologisk oppfølging av mageslimhinnen etter Helicobacter pylori-utryddelse. J Pathol. 1999; 188 (1): 24-29.
pubmed doi - Jass JR, Filipe MI. Mukinprofilene til normal mage slimhinne, tarmmetaplasi og dets varianter og gastrisk karsinom. Histochem J. 1981; 13 (6): 931-939.
pubmed doi - Filipe MI, Munoz N, Matko I, Kato I, Pompe-Kirn V, Jutersek A, Teuchmann S, et al. Tarmmetaplasi typer og risikoen for mage kreft: en kohortestudie i Slovenia. Int J kreft. 1994; 57 (3): 324-329.
pubmed doi - Rokkas T, Filipe MI, Sladen GE. Påvisning av økt forekomst av tidlig magekreft hos pasienter med tarmmetaplasi type III som følges nøye opp. Mage. 1991; 32 (10): 1110-1113.
publisert doi - Genta RM, Rugge M. Gjennomgangsartikkel: pre-neoplastiske tilstander i mageslimhinnen – en praktisk tilnærming for den forvirrede klinikeren. Aliment Pharmacol Ther. 2001; 15 (Suppl 1): 43-50.
publisert - Fukase K, Kato M, Kikuchi S, Inoue K, Uemura N, Okamoto S, Terao S, et al. Effekt av utryddelse av Helicobacter pylori på forekomst av metakront gastrisk karsinom etter endoskopisk reseksjon av tidlig gastrisk kreft: en åpen, randomisert kontrollert studie. Lancet. 2008; 372 (9636): 392-397.
publisert doi - Tashiro J, Miwa J, Tomita T; Matsubara Y, Oota Y. Magekreft oppdaget etter Helicobacter pylori-utryddelse. Fordøyelsesendoskopi. 2007; 19: 167-173.
Dette er en artikkel med åpen tilgang distribuert under vilkårene i Creative Commons Attribution License, som tillater ubegrenset bruk, distribusjon og reproduksjon i hvilket som helst medium, forutsatt at originalverket er sitert riktig.
Gastroenterology Research er utgitt av Elmer Press Inc.