Mesomeer effect
Het mesomere effect in de chemie is een eigenschap van substituenten of functionele groepen in een chemische verbinding. Het wordt gedefinieerd als de polariteit die in het molecuul wordt geproduceerd door de interactie van twee pi-bindingen of tussen een pi-binding en een eenzaam paar elektronen aanwezig op een aangrenzend atoom.

+ M-effect van een methoxygroep in een ether
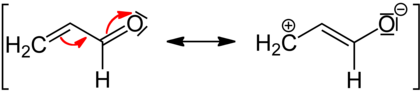
–M effect van een carbonylgroep in acroleïne
Het effect wordt op een kwalitatieve manier gebruikt en beschrijft de elektronen onttrekkende of vrijgevende eigenschappen van substituenten op basis van relevante resonantiestructuren en wordt gesymboliseerd door de letter M. Het mesomere effect is negatief (-M) wanneer de substituent is een elektronenonttrekkende groep en het effect is positief (+ M) wanneer de substituent een elektronenafgevende groep is.
+ M EFFECTORDER:
–O- > –NH2 > –OF > –NHCOR > –OCOR > –Ph > CH3 > –F > –Cl > –Br > –I
-M EFFECT ORDER:
–NO2 > –CN > –S (= O) 2 − OH > –CHO > –C = O > –COOCOR > –COOR > –COOH > –CONH2 > –COO-
De netto elektronenstroom van of naar de substituent wordt mede bepaald door het inductieve effect. Het mesomere effect als gevolg van p-orbitale overlap (resonantie) heeft absoluut geen effect op dit inductieve effect, aangezien het inductieve effect puur te maken heeft met de elektronegativiteit van de atomen en hun topologie in het molecuul (waaraan atomen zijn verbonden ).
De begrippen mesomerisch effect, mesomerie en mesomeer werden in 1938 door Ingold geïntroduceerd als een alternatief voor Paulings synoniem concept van resonantie. ‘Mesomerie’ wordt in deze context vaak aangetroffen in de Duitse en Franse literatuur , maar in de Engelse literatuur domineert de term “resonantie”.