Geologia fizyczna
Ogromna większość minerałów tworzących skały skorupy ziemskiej to minerały krzemianowe. Należą do nich minerały, takie jak kwarc, skaleń, mika, amfibol, piroksen, oliwin i wiele różnych minerałów ilastych. Budulcem wszystkich tych minerałów jest czworościan krzemionki, będący połączeniem czterech atomów tlenu i jednego atomu krzemu. Są one ułożone w taki sposób, że płaszczyzny przeciągane przez atomy tlenu tworzą czworościan (rysunek 2.6). Ponieważ jon krzemu ma ładunek +4, a każdy z czterech jonów tlenu ma ładunek –2, tetraedr krzemionki ma ładunek netto –4.
W minerałach krzemianowych te czworościany są ułożone i połączone ze sobą na różne sposoby, od pojedynczych jednostek po złożone struktury (rysunek 2.9). Najprostsza struktura krzemianowa, czyli mineralnego oliwinu, składa się z izolowanych czworościanów związanych z jonami żelaza i / lub magnezu. W oliwinie ładunek –4 każdego czworościanu krzemionki jest równoważony dwoma dwuwartościowymi (tj. +2) kationami żelaza lub magnezu. Oliwin może być Mg2SiO4 lub Fe2SiO4 lub pewną kombinacją tych dwóch (Mg, Fe) 2SiO4. Dwuwartościowe kationy magnezu i żelaza mają dość mały promień (0,73 w porównaniu z 0,62 angstremów). Ze względu na to podobieństwo wielkości i ponieważ oba są dwuwartościowymi kationami (oba mają ładunek +2), żelazo i magnez mogą łatwo zastąpić się nawzajem w oliwinie i wielu innych minerałach.
| Konfiguracja czworościanu | Przykładowe minerały | |
|---|---|---|
 |
Izolowane (nesosilicates) | Oliwin, granat, cyrkonia, cyjanit |
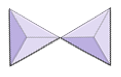 |
Pary (sorokrzemiany) | Epidot, zoisyt |
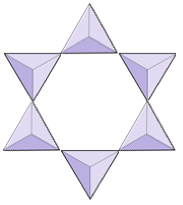 |
Pierścienie (cyklokrzemiany) | Turmalin |
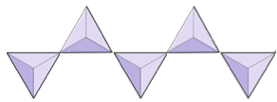 |
Pojedyncze łańcuchy (niekrzemiany) | Pirokseny, wollastonit |
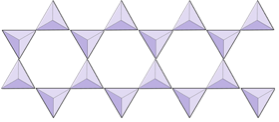 |
Podwójne łańcuchy (niekrzemiany) | Płazy |
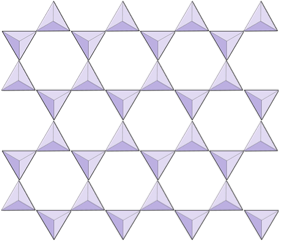 |
Arkusze (krzemiany warstwowe) | Miki, minerały ilaste, serpentyna, chloryt |
| 3-wymiarowe struktura | Framework (tectosilicates) | Skaleń, kwarc, zeolit |
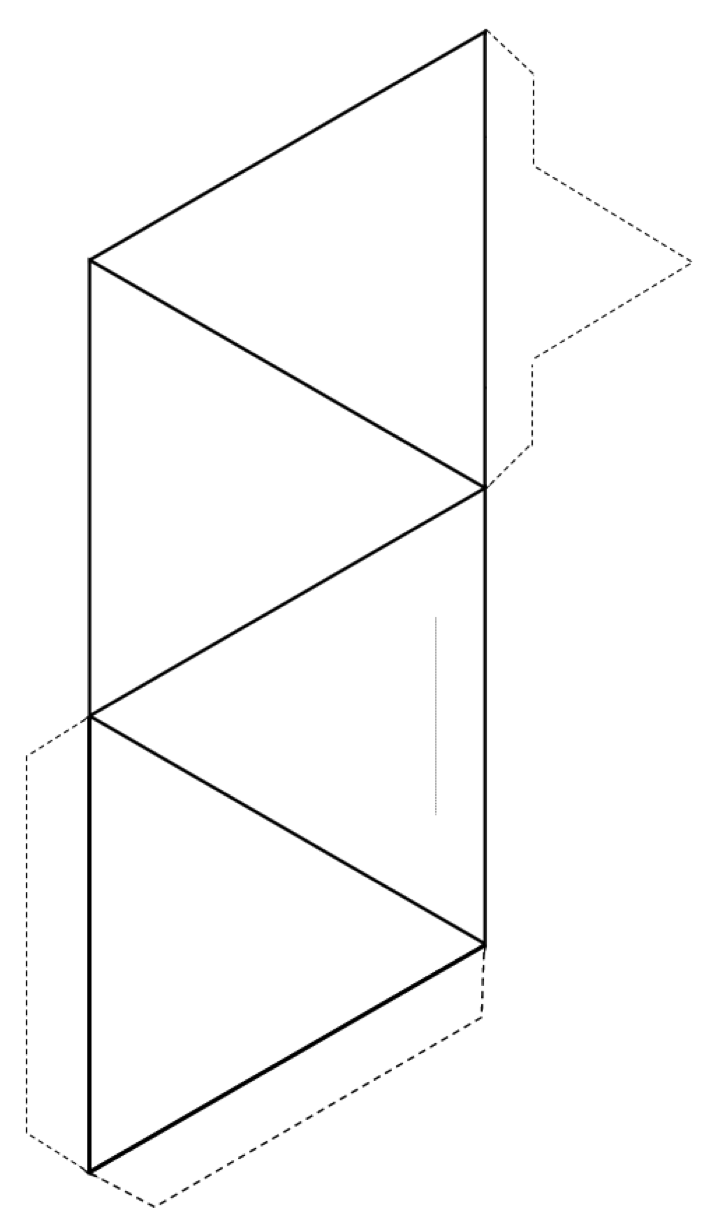
Ćwiczenie 2.3 Tworzenie czworościanu
Wytnij zewnętrzną stronę kształtu (linie ciągłe i przerywane), a następnie złóż wzdłuż linii ciągłych, aby utworzyć czworościan.
Jeśli masz klej lub taśmę, zabezpiecz zakładki do czworościanu, aby utrzymać go razem. Jeśli nie masz kleju ani taśmy, zrób plasterek wzdłuż cienkiej szarej linii i włóż ostro zakończony języczek w szczelinę.
Jeśli robisz to w klasie, spróbuj połączyć swój czworościan z innymi w pary, pierścienie, pojedyncze i podwójne łańcuchy, arkusze, a nawet trójwymiarowe struktury.
W oliwinie, w przeciwieństwie do większości innych minerałów krzemianowych, tetraedry krzemionkowe nie są połączone ze sobą inny. Są one jednak związane z żelazem i / lub magnezem, jak pokazano na rysunku 2.10.
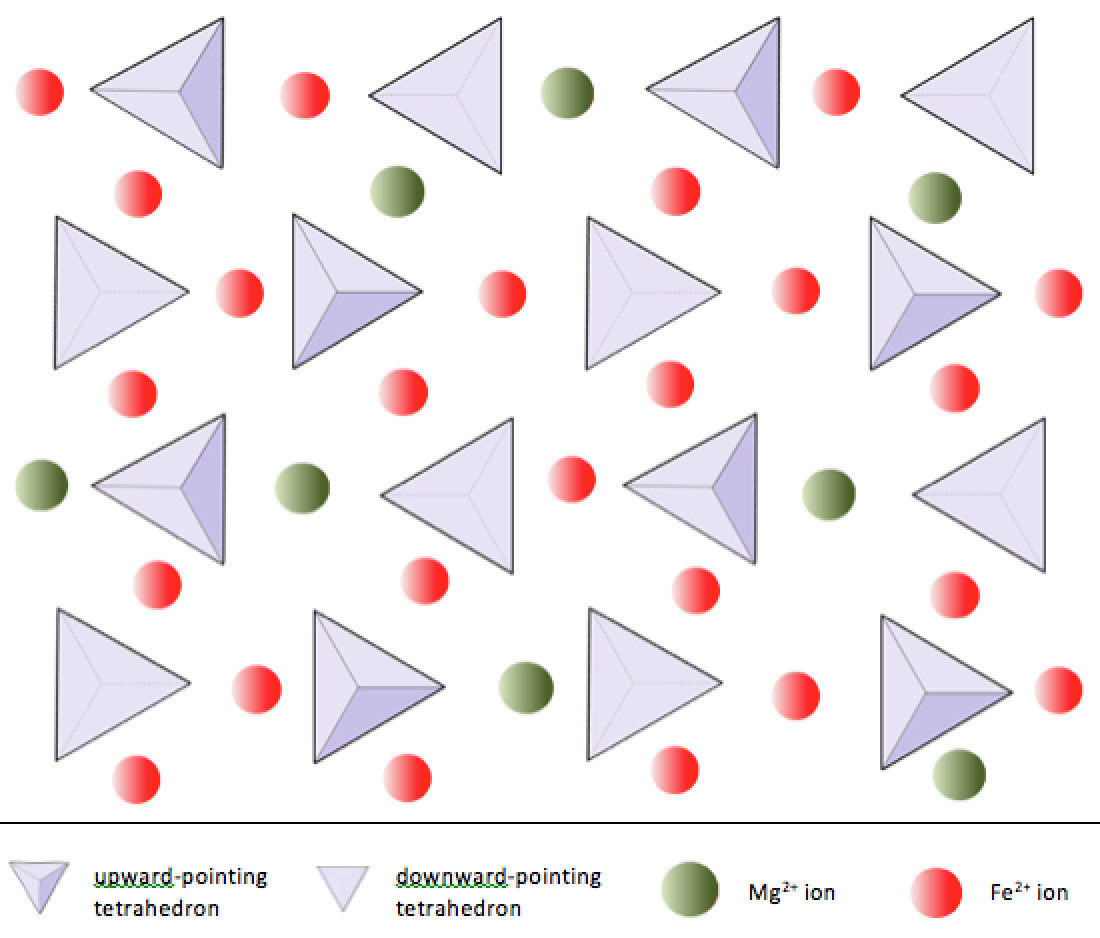
Jak już wspomniano, jony +2 żelaza i magnezu mają podobną wielkość (chociaż nie są takie same). To pozwala im zastępować się nawzajem w niektórych minerałach krzemianowych. W rzeczywistości zwykłe jony w minerałach krzemianowych mają szeroki zakres rozmiarów, jak pokazano na rysunku 2.11. Wszystkie przedstawione jony są kationami, z wyjątkiem tlenu. Zauważ, że żelazo może istnieć zarówno jako jon +2 (jeśli straci dwa elektrony podczas jonizacji), jak i jako jon +3 (jeśli straci trzy). Fe2 + jest znane jako żelazo żelazne. Fe3 + jest znane jako żelazo żelazowe. Promienie jonowe mają krytyczne znaczenie dla składu minerałów krzemianowych, więc będziemy ponownie odwoływać się do tego diagramu.

Struktura pojedynczego łańcucha piroksen krzemianowy przedstawiono na rysunkach 2.12 i 2.13. W piroksenie tetraedry krzemionki są połączone ze sobą w jeden łańcuch, w którym jeden jon tlenu z każdego czworościanu jest współdzielony z sąsiednim czworościanem, stąd w strukturze jest mniej tlenu.W rezultacie stosunek tlenu do krzemu jest niższy niż w oliwinie (3: 1 zamiast 4: 1), a ładunek netto na atom krzemu jest mniejszy (–2 zamiast –4), ponieważ potrzeba mniej kationów aby zrównoważyć tę opłatę. Kompozycje piroksenu należą do typu MgSiO3, FeSiO3 i CaSiO3 lub ich kombinacji. Piroksen można również zapisać jako (Mg, Fe, Ca) SiO3, gdzie pierwiastki w nawiasach mogą występować w dowolnej proporcji. Innymi słowy, piroksen ma jeden kation na każdy tetraedr krzemionki (np. MgSiO3), podczas gdy oliwin ma dwa (np. Mg2SiO4). Ponieważ każdy jon krzemu ma wartość +4, a każdy jon tlenu –2, trzy tlenki (–6) i jeden krzem (+4) dają ładunek netto równy –2 dla pojedynczego łańcucha tetraedrów krzemionki. W piroksenie, jeden dwuwartościowy kation (2+) na czworościan równoważy ten –2 ładunek. W oliwinie potrzebne są dwa dwuwartościowe kationy, aby zrównoważyć ładunek –4 izolowanego czworościanu.
Struktura piroksenu jest bardziej „permisywna” niż struktura oliwinu – co oznacza, że kationy o szerszym zakresie promieni jonowych może do niego pasować. Dlatego pirokseny mogą zawierać kationy żelaza (promień 0,63 A), magnezu (promień 0,72 A) lub wapnia (promień 1,00 A).
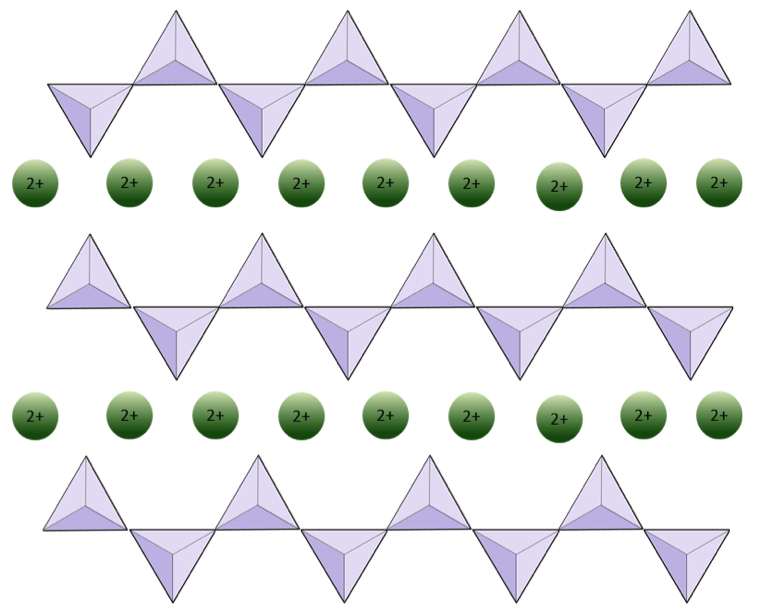
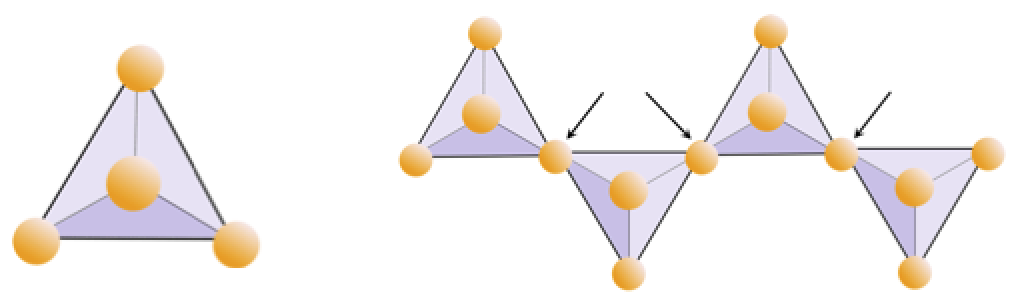
Ćwiczenie 2.4 Pozbawienie tlenu
Poniższy diagram przedstawia pojedynczy łańcuch w minerale krzemianowym. Policz liczbę czworościanów w stosunku do liczby jonów tlenu (żółte kulki). Każdy czworościan ma jeden jon krzemu, więc powinno to dać stosunek Si do O w jednołańcuchowych krzemianach (np. Piroksenie).
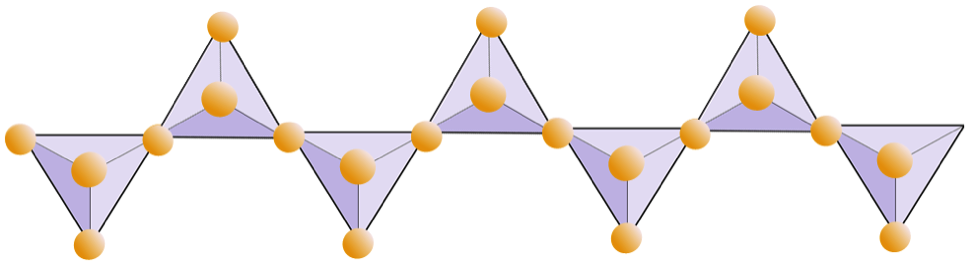
Poniższy diagram przedstawia podwójny łańcuch w minerale krzemianowym. Ponownie policz liczbę czworościanów w stosunku do liczby jonów tlenu. To powinno dać ci stosunek Si do O w dwułańcuchowych krzemianach (np. Amfibole).
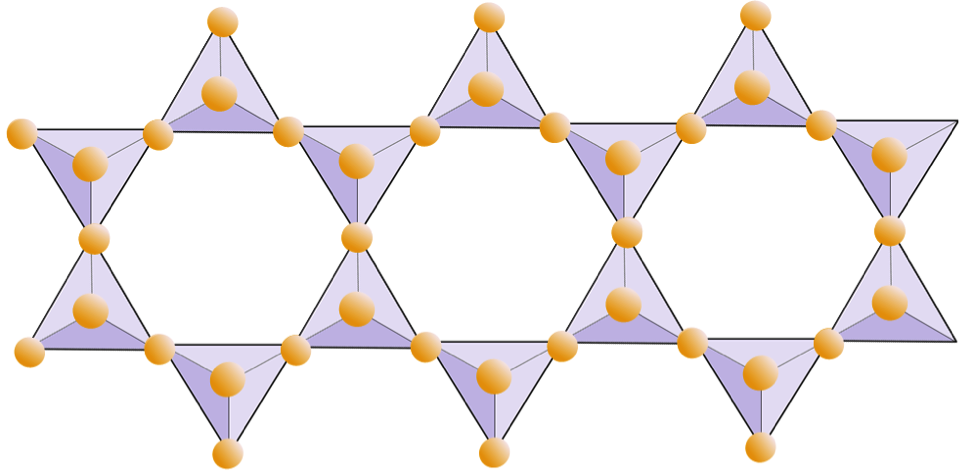
W strukturach amfiboli, tetraedry krzemionki są połączone podwójnym łańcuchem, którego stosunek tlenu do krzemu jest niższy niż piroksenu, a zatem do zrównoważenia ładunku potrzeba jeszcze mniej kationów. Amfibol jest jeszcze bardziej permisywny niż piroksen, a jego skład może być bardzo złożony. Na przykład Hornblende może zawierać sód, potas, wapń, magnez, żelazo, glin, krzem, tlen, fluor i jon hydroksylowy (OH–).
W strukturach miki tetraedry krzemionki są ułożone w ciągłe arkusze, gdzie każdy czworościan dzieli trzy aniony tlenu z sąsiednimi czworościanami. Istnieje jeszcze większy udział tlenu między sąsiednimi czworościanami, a zatem mniej kationów równoważących ładunek jest potrzebnych w przypadku minerałów krzemianów warstwowych. Wiązanie między arkuszami jest stosunkowo słabe, co odpowiada za dobrze rozwinięte jednokierunkowe rozszczepienie (rysunek 2.14). Mika biotytowa może zawierać żelazo i / lub magnez, co czyni ją minerałem krzemianu ferromagnezu (jak oliwin, piroksen i amfibol). Chloryn to kolejny podobny minerał, który zwykle zawiera magnez. W mice muskowitowej jedynymi obecnymi kationami są glin i potas; stąd jest to minerał nieferromagnezji krzemianowy.

Oprócz muskowitu, biotytu i chlorynu istnieje wiele innych krzemianów warstwowych (lub krzemianów warstwowych), które zwykle występują w postaci fragmentów wielkości gliny (tj. mniej niż 0,004 mm). Należą do nich minerały ilaste: kaolinit, illit i smektyt i chociaż są trudne do zbadania ze względu na ich bardzo mały rozmiar, są niezwykle ważnymi składnikami skał, a zwłaszcza gleb.
Cały krzemian warstwowy minerały zawierają również wodę w swojej strukturze.
Czworościany krzemionki są związane w trójwymiarowych strukturach zarówno w skaleniach, jak i w kwarcu. Są to minerały nieferromagnezowe – nie zawierają żelaza ani magnezu.Oprócz tetraedrów krzemionkowych, skalenie zawierają kationy glinu, potasu, sodu i wapnia w różnych kombinacjach. Kwarc zawiera tylko tetraedry krzemionkowe.
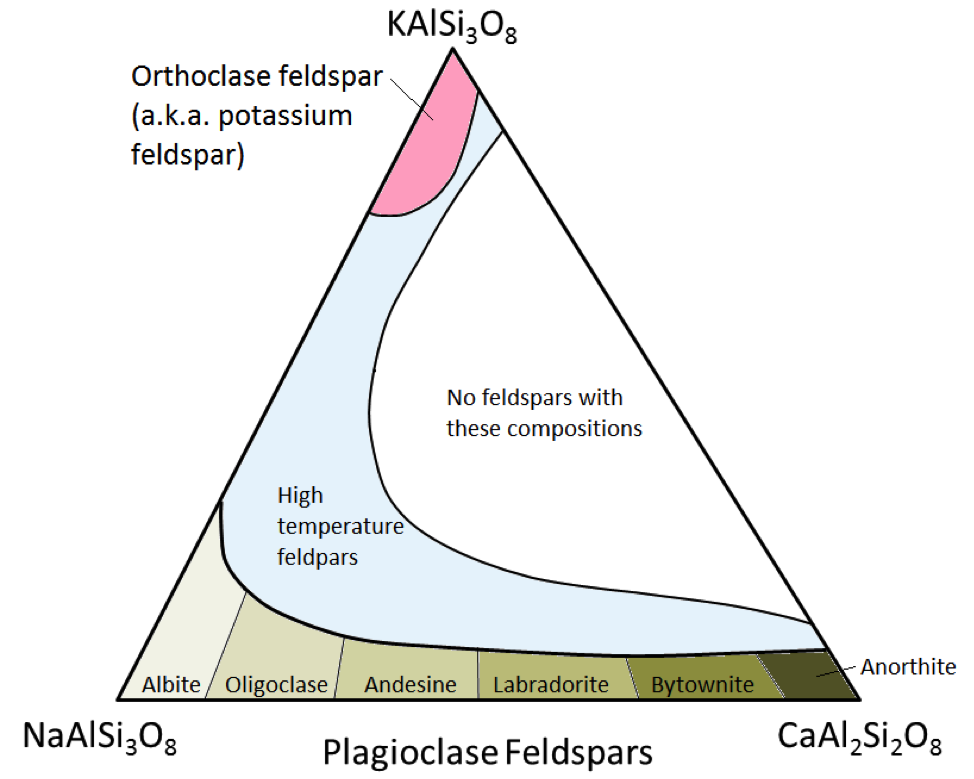
Trzy główne minerały skalenia to skaleń potasowy (znany również jako skaleń K lub spar K) oraz dwa rodzaje skalenia plagioklazowego: albit (tylko sód) i anortyt (tylko wapń) . Podobnie jak w przypadku żelaza i magnezu w oliwinie, istnieje ciągły zakres składów (szereg stałych roztworów) między albitem i anortytem w plagioklazie. Dzieje się tak, ponieważ jony wapnia i sodu mają prawie identyczną wielkość (1,00 A w porównaniu z 0,99 A). Mogą istnieć dowolne składy pośrednie między CaAl2Si3O8 i NaAlSi3O8 (rysunek 2.15). Jest to trochę zaskakujące, ponieważ chociaż są bardzo podobne pod względem wielkości, jony wapnia i sodu nie mają tego samego ładunku (Ca2 + w porównaniu z Na +). Ten problem jest wyjaśniony przez odpowiednie podstawienie Al3 + za Si4 +. Dlatego albit to NaAlSi3O8 (jeden Al i trzy Si), anortyt to CaAl2Si2O8 (dwa Al i dwa Si), a skalenie plagioklazowe o pośrednim składzie ma pośrednie proporcje Al i Si. Nazywa się to „substytucją sprzężoną”.
Skaleń plagioklazów o pośrednim składzie to oligoklaz (10% do 30% Ca), andezyna (30% do 50% Ca), labradoryt (50% do 70 % Ca) i bytownit (70% do 90% Ca). Skaleń K (KAlSi3O8) ma nieco inną strukturę niż plagioklaz, ze względu na większy rozmiar jonu potasowego (1,37 Å) i ze względu na tak duży rozmiar , potas i sód nie zastępują się łatwo, z wyjątkiem wysokich temperatur. Te wysokotemperaturowe skalenie można znaleźć tylko w skałach wulkanicznych, ponieważ natrętne skały magmowe ochładzają się wystarczająco wolno do niskich temperatur, aby skalenie zmieniły się w jeden z formy o niższej temperaturze.
W kwarcu (SiO2) tetraedry krzemionki są połączone w „doskonałej” trójwymiarowej ramie. Każdy czworościan jest związany z czterema innymi czworościanami (z tlenem dzielonym w każdym rogu każdego czworościanu), w wyniku czego stosunek krzemu do tlenu wynosi 1: 2. Ponieważ jeden kation krzemu ma ładunek +4, a każdy z dwóch anionów tlenu ma ładunek –2, ładunek jest zrównoważony. Nie ma potrzeby stosowania glinu ani żadnych innych kationów, takich jak sód lub potas. Twardość i brak rozszczepienia w kwarcu wynikają z silnych wiązań kowalencyjnych / jonowych charakterystycznych dla czworościanu krzemionki.
Ćwiczenie 2.5 Krzemiany żelazomagnezu?
Minerały krzemianowe są klasyfikowane jako ferromagnezowe lub nieferromagnezowe w zależności od tego, czy zawierają żelazo (Fe) i / lub magnez (Mg). Poniżej wymieniono szereg minerałów i ich formuł. Dla każdego z nich wskaż, czy jest to krzemian ferromagnezu.
| Mineralny | Formuła | Krzemian żelazomagnezu? |
|---|---|---|
| oliwin | (Mg, Fe) 2SiO4 | |
| piryt | FeS2 | |
| plagioclase | CaAl2Si2O8 | |
| piroksen | MgSiO3 | |
| hematyt | Fe2O3 | |
| orthoclase | KAlSi3O8 | |
| kwarc | SiO2 |
| Mineralne | Formuła * | Krzemian żelazomagnezu? |
|---|---|---|
| amfibole | Fe7Si8O22 (OH) 2 | |
| muscovite | K2Al4 Si6Al2O20 (OH) 4 | |
| magnetyt | Fe3O4 | |
| biotite | K2Fe4Al2Si6Al4O20 (OH) 4 | |
| dolomit | (Ca, Mg) CO3 | |
| granat | Fe2Al2Si3O12 | |
| serpentine | Mg3Si2O5 (OH) 4 |
* Niektóre formuły, zwłaszcza te bardziej skomplikowane, zostały uproszczone.
- Angstrem to jednostka powszechnie używana do wyrażenia atomowej -wymiary w skali. Jeden angstrem ma 10–10 m lub 0,0000000001 m. Symbolem angstremów jest Å. ↵