Poszerzenie aorty w chorobie dwupłatkowej zastawki aortalnej | Revista Española de Cardiología (wydanie angielskie)
Wprowadzenie
Dwupłatkowa zastawka aortalna (BAV) to najczęstsza wrodzona wada serca, występująca u 0,5–1,4% populacji ; ta anomalia jest sporadycznie przenoszona genetycznie drogą autosomalną dominującą, z przewagą mężczyzn 3: 1.1 BAV ma znaczenie kliniczne, nie tylko ze względu na powikłania zastawkowe (dysfunkcja zastawek, infekcyjne zapalenie wsierdzia), ale także ze względu na wiele nieprawidłowości naczyniowych, w tym rozszerzenie aorty2 (ryc. 1).
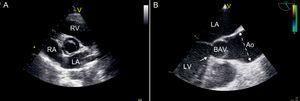
Rycina 1. Obrazy echokardiograficzne oceniające dwupłatkową zastawkę aortalną. Odp .: Przezklatkowy rzut przymostkowy w krótkiej osi przedstawiający dwupłatkową zastawkę aortalną z konfiguracją przednio-tylną. B: Widok przezprzełykowy w osi długiej pokazujący nieprawidłowy skurczowy otwór („kopułę”) dwupłatkowej zastawki aortalnej. Widoczne poszerzenie aorty, rozpoczynające się powyżej połączenia zatokowo-cylindrycznego i maksymalne w środkowej części wstępującej aorty rurowej (linia przerywana). obecne jest zwężenie z włóknistym grzbietem wychodzącym z przegrody drogi odpływu lewej komory (strzałka). Ao, aorta; BAV, dwupłatkowa zastawka aortalna; LA, lewy przedsionek; LV, lewa komora; RA, prawy przedsionek; prawej komory.
Zgłaszana częstość poszerzenia aorty związanego z BAV waha się od 33% -80%. Odchylenie to jest oparte na progach stosowanych do określenia rozszerzenia, normalnych wartościach dla wieku i powierzchni ciała oraz regionu aorty. Opisano różne typy tętniaków aorty w zależności od zajętego obszaru, 3 to poszerzenie środkowego odcinka wstępującego (poszerzenie samego odcinka wstępującego rurkowatego), najczęściej obserwowany wzorzec.4 Wiek i morfologia BAV również zostały powiązane. z wymiarem aorty wstępującej (AscAo), chociaż rola morfologii nie jest jasno zdefiniowana.5, 6
Patofizjologia
Trwają kontrowersje między dwiema teoriami dotyczącymi patogenezy poszerzenia aorty u pacjentów z BAV. Jedna z teorii twierdzi, że poszerzenie AscAo może być konsekwencją turbulencji przepływu krwi, przy czym pierwotny efekt hemodynamiczny oddziałuje na życie płodu i skutkuje różnym stopniem zwyrodnienia aorty wywołanego stresem. Chociaż ta hipoteza ma tę zaletę, że jest względnie prosta, niektóre badania sugerują, że same zmiany hemodynamiczne nie mogą być wyłącznie odpowiedzialne za poszerzenie aorty u tych pacjentów.7 Druga teoria podnosi hipotezę o obecności wrodzonej wrodzonej wady struktury aorty. Związek między układem guzków a chorobą AscAo można wytłumaczyć nieprawidłowymi wzorcami rozwoju komórek grzebienia nerwowego, a nieprawidłowości strukturalne wystąpiłyby na poziomie komórki niezależnie od zmiany hemodynamicznej.8 Ta teoria stała się coraz bardziej popularna w ciągu ostatniej dekady i doprowadziła do bardziej agresywne zalecenia dotyczące leczenia proksymalnej aorty u tych pacjentów. Istnieje kilka dowodów potwierdzających dominującą wrodzoną wadę ściany:
-
• U pacjentów z BAV (w tym dzieci) z prawidłowo funkcjonującą zastawką aortalną zaobserwowano znaczne powiększenie proksymalnej aorty w porównaniu z normalne kontrole dopasowane do wieku. Jednak „normalnie” funkcjonujący BAV jest samoistnie zwężony, z przepływem nieosiowym i turbulentnym, nawet jeśli nie występuje międzyzastawkowy gradient ciśnienia. Przepływ ten jest wysoce ekscentryczny, powodując nieprawidłowe spiralne wzorce przepływu w proksymalnej aorcie.9 Te nieprawidłowe wzorce hemodynamiczne działają przez długi czas i mogą prowadzić do asymetrycznych uszkodzeń ściany aorty wywołanych stresem, a następnie poszerzenia określonych odcinków aorty.
-
• Wykazano, że pacjenci z BAV mają większe średnice korzenia aorty i AscAo niż pacjenci z trójdzielną zastawką aortalną (TAV), nawet po dopasowaniu hemodynamicznej ciężkości zmian zastawkowych.5 Jednak ekscentryczność która występuje przez BAV, nie została przeanalizowana.
-
• Rozszerzenie AscAo może wystąpić nawet po wymianie zastawki aortalnej.10
-
• Wewnętrzna nieprawidłowość ściany byłaby poparta wykazaniem nieprawidłowości histopatologicznej leżącej u podstaw powikłań AscAo w BAV, a mianowicie torbielowatej degeneracji przyśrodkowej. To patologiczne odkrycie obserwowano w aortach pacjentów z BAV przed wystąpieniem tętniaka i obejmuje ono zmniejszoną składową macierzy zewnątrzkomórkowej i zwiększoną degradację enzymów macierzy w aorcie.11, 12, 13 Co ciekawe, chociaż podobne zmiany histologiczne i biomolekularne występują u W aortach BAV i Marfana rozkład tych zmian różni się w obu stanach, a nawet w tętniakach TAV (Tabela 1), co sugeruje podstawową rolę hemodynamiki w rozwoju reaktywnej przebudowy ściany aorty.
Tabela 1 .Histopatologia torbielowatego zwyrodnienia środkowego
Charakterystyka Tętniak BAV Tętniak Marfana Tętniak TAV Redukcja składników ECM Zwiększenie apoptozy VSMC: zmniejszenie produkcji białek ECM Fragmentacja elastyny: utrata wsparcia strukturalnego i elastyczności Niedobór FB-1: oderwanie VSMC od macierzy elastyny i kolagenu (rozerwanie macierzy) Mniejszy stopień zmian Zwiększyć enzymy degradujące macierz Zwiększyć MMP -2 Zwiększ MMP-9 Zwiększ MMP2 / TIMP-1 Zwiększ MMP-12 Zwiększ MMP-13 Przestrzenna dystrybucja CMD Asymetryczny Obwodowy Ograniczony do obszaru tętniaka BAV , dwupłatkowa zastawka aortalna; CMD, torbielowate zwyrodnienie przyśrodkowe; ECM, macierz zewnątrzkomórkowa; FB, fibrylina; MMP, metaloproteinaza macierzy; TAV, trójdzielna zastawka aortalna; TIMP, tkankowy inhibitor metaloproteinazy; VSMC, komórki mięśni gładkich naczyń krwionośnych.
-
• Wreszcie, zasugerowano, że choroba BAV jest wysoce dziedziczna, a determinacja jest prawie całkowicie genetyczna. W dużych badaniach rodzinnych częstość występowania BAV u krewnych pierwszego stopnia (FDR) osoby z BAV wynosi 9%. Ponadto w niektórych badaniach odnotowano poszerzenie korzenia aorty, tętniak aorty piersiowej lub rozwarstwienie aorty u nawet jednej trzeciej FDR pacjentów z BAV, niezależnie od tego, czy BAV był obecny, czy nie.14, 15 Chociaż istnieje wiele potencjalnych miejsc genów tętniaków BAV i AscAo. zasugerowano, że nie ustalono jednoznacznie miejsca odpowiedzialnego za poszerzenie aorty w BAV.
Współczynnik rozszerzenia w historii naturalnej
Poszerzenie aorty zostało udokumentowane w dzieciństwie, co sugeruje, że proces zaczyna się we wczesnym okresie życia. Informacje na temat tempa progresji choroby aorty związanej z BAV są bardzo zróżnicowane, a badania podają około 0,3–1,1 mm na rok (mm / rok) .7 W badaniu Olmsted County częstość występowania poszerzenia AscAo (> 40 mm) wynosiło 15%, aw podgrupie pacjentów z powtórzonymi pomiarami częstość wzrosła do 39% .16 Chociaż wiele czynników ryzyka jest związanych z poszerzeniem aorty (wysokie ciśnienie krwi, płeć męska, znaczne choroby zastawek), najważniejszą zmienną jest prawdopodobnie wiek. Zarówno w badaniach pediatrycznych, jak i dorosłych wykazano, że w porównaniu z tętniakami związanymi z TAV tętniak związany z BAV powiększa się szybciej i objawia się w znacznie młodszym wieku.6,7 Ponadto postępujące poszerzenie aorty występuje częściej u pacjentów z większe aorty na początku badania.
Rozwarstwienie i pęknięcie aorty
Chociaż najbardziej przerażającym powikłaniem aorty u pacjentów z BAV jest rozwarstwienie aorty, faktyczna częstość występowania tego powikłania pozostaje przedmiotem dyskusji. Częstość występowania różni się w zależności od badanej kohorty, z łączną oceną przypadków 4% .17,18 Niektóre raporty z ośrodków referencyjnych sugerowały 5-9-krotnie większe ryzyko rozwarstwienia aorty w BAV niż w TAV, podczas gdy inne nie obserwowały takiego związku .7, 19 Ostatnie badania wykazały mniejsze ryzyko. W serii Toronto20 częstość rozwarstwienia wynosiła 0,1% na pacjenta-rok obserwacji, a w badaniu Olmsted County 25-letnie ryzyko rozwarstwienia aorty po rozpoznaniu echokardiograficznym wynosiło 0,5%.
W rzeczywistości tętniaki AscAo związane z BAV wycinają i pękają w zakresie wielkości porównywalnym do tętniaków o innej etiologii (średnia: 60 ± 12 mm; zakres: 30-108 mm) .22 Zwiększone ryzyko rozcięcia i pęknięcia związane z BAV wynika z większej częstości występowania i częstości poszerzenia aorty, które występuje w znacznie młodszym wieku niż idiopatyczne tętniaki AscAo. 1,9 vs 1,3 mm / rok), częstość pęknięć i rozwarstwień była podobna.7 Dlatego, pomimo szybszego tempa wzrostu, zdarzenia ujemne występują z podobną częstością i przy podobnych średnicach aorty.
Pacjenci z zespołem Marfana mają znacznie większe prawdopodobieństwo rozwarcia aorty w ciągu całego życia n (40%) niż pacjenci z BAV. Jednakże, ponieważ choroba BAV jest około 100 razy częstsza niż zespół Marfana, choroba BAV jest odpowiedzialna za taką samą lub większą liczbę rozwarstwień aorty niż zespół Marfana.22
Diagnoza i nadzór
Echokardiogram przezklatkowy (TTE) jest zwykle Podstawową techniką obrazowania do diagnozowania BAV (ryc. 1), ponieważ identyfikuje pacjentów, u których rdzeń aorty lub AscAo jest powiększony i ocenia ich progresję w czasie. Normalny zakres (AscAo i średnica korzenia aorty2) należy skorygować ze względu na wiek i płeć.Te pomiary TTE są ściśle skorelowane z pomiarami wykonanymi za pomocą tomografii komputerowej (CT) (ang. Multidetector computed tomography) 23 i rezonansu magnetycznego (MRI), 24 co sugeruje, że TTE jest dokładną metodą obrazowania. Niemniej jednak standardowy TTE może nie uwidocznić całego AscAo i może nie wykryć jego największej średnicy, zwykle najbardziej widocznej w proksymalnym lub środkowym AscAo. W przypadku niedostatecznej wizualizacji za pomocą echokardiogramu zaleca się wykonanie badania MRI lub CT w celu oceny całego AscAo. Zasadne jest również wykonanie wyjściowego skanu MRI lub TK, gdy po raz pierwszy zdiagnozowane jest poszerzenie aorty (≥45 mm), co służyłoby jako miara referencyjna podczas obserwacji w przypadku stwierdzenia rozbieżności między seryjnymi echokardiogramami. Skan MRI może dokładnie wykryć i zmierzyć tętniaki aorty oraz potwierdzić anatomię zastawki, unikając kontrastu i ekspozycji na promieniowanie. Ostatnio w 4-wymiarowym rezonansie magnetycznym wykazano nieprawidłowy skurczowy przepływ helikalny, a stopień i kierunek ekscentryczności strumienia przepływu mogą mieć kluczowe znaczenie dla określenia ryzyka powstania tętniaka odcinkowego.9 Specyficzna anatomia aorty może decydować o tym, które badanie obrazowe jest optymalne. Na przykład, gdy tętniak obejmuje rdzeń aorty, rezonans magnetyczny jest korzystniejszy niż tomografia komputerowa, ponieważ CT obrazuje go gorzej i jest mniej dokładny w określaniu jego średnicy. Jeśli istnieje przeciwwskazanie do TK i MR, TEE jest rozsądną alternatywą, która jest wyraźnie lepsza od TTE w ocenie tętniaków zlokalizowanych w korzeniu aorty (ryc. 1), łuku aorty i aorcie zstępującej. Połączenie TTE i angiogramu wielorzędowego TK może dostarczyć wszystkich informacji wymaganych, jeśli planowana jest operacja.
Po wykryciu tętniaka aorty piersiowej po raz pierwszy nie jest możliwe określenie jego tempa wzrostu. jest zatem właściwe, aby uzyskać powtórne badanie obrazowe 6 miesięcy po badaniu wstępnym. Jeśli wielkość tętniaka pozostaje niezmieniona, w większości przypadków uzasadnione jest coroczne badanie obrazowe.25 Dotyczy to również wymiany zastawki aortalnej, ponieważ może dojść do postępującego poszerzenia aorty. Dalszą ocenę należy rozważać w krótszych odstępach czasu, w zależności od wymiarów aorty, szybkości rozszerzania się i aktywności fizycznej. U pacjentów z BAV bez znacznych zmian zastawkowych i prawidłowej średnicy aorty badanie echokardiograficzne co 2 lata może być wystarczające.
Na koniec należy rozważyć badanie przesiewowe FDR u pacjentów z BAV w celu wykrycia wad rozwojowych zastawki aortalnej i rozszerzonego AscAo. TTE może wiarygodnie identyfikować FDR z nieprawidłowościami strukturalnymi serca14, 26 (ryc. 2). Jednak naturalna historia FDR z lekko rozszerzonym korzeniem aorty i fenotypem TAV jest nieznana. Dlatego potrzebne są długoterminowe badania kontrolne tej populacji, zarówno w celu określenia stopnia poszerzenia, jak iz kolei w celu ustalenia częstości wykonywania seryjnych badań przesiewowych TTE, które w rozsądny sposób wykryłyby poszerzenie aorty przed wystąpieniem powikłań14
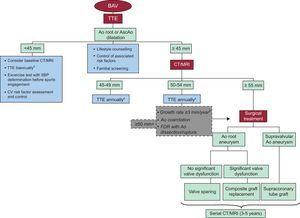
Rysunek 2. Algorytm pokazujący ogólne podejście do postępowania i nadzoru dylatacji aorty. Ao, aorta; AscAo, aorta wstępująca; BAV, dwupłatkowa zastawka aortalna; CT, tomografia komputerowa; CV, układ sercowo-naczyniowy; FDR, krewni pierwszego stopnia; MRI, obrazowanie metodą rezonansu magnetycznego; SBP, skurczowe ciśnienie krwi; TTE, echokardiogram przezklatkowy. A Rozważ wcześniejszą obserwację, jeśli występuje dysfunkcja zastawek. B Porównania seryjne obrazów wykonanych tą samą techniką obrazowania, obok siebie, na tym samym poziomie aorty.
Postępowanie Leczenie medyczne
Oprócz rutynowa ocena obrazowa, pacjenci z BAV powinni otrzymać informacje o ryzyku rozwarstwienia i powstawaniu tętniaka, a także o typowych objawach ostrego rozwarstwienia aorty (ryc. 2).
Należy zmodyfikować aktywność lub styl życia, ponieważ są one bardzo intensywne , sporty wyczynowe i zderzeniowe są potencjalnie niebezpieczne i mogą przyspieszyć rozwarstwienie aorty lub pęknięcie aorty z większym niż nieznacznym rozszerzeniem (45 mm) .27
U tych pacjentów należy agresywnie kontrolować czynniki ryzyka sercowo-naczyniowego, takie jak wysokie ciśnienie krwi. β-blokery można podawać w celu opóźnienia lub zapobieżenia rozszerzeniu lub progresji korzenia aorty u pacjentów z BAV (w przypadku braku ciężkiej niedomykalności aorty) .25, 26 Jednakże uzasadnienie dla tego zalecenia opiera się na efekcie leczenia β-adrenolitykami w preparacie Marfan , 28 i dlatego powinny zostać potwierdzone w dalszych badaniach. Chociaż niektóre badania przyniosły korzyści z leczenia blokerami receptora angiotensyny i inhibitorami konwertazy angiotensyny u osób z zespołem Marfana, 29, 30 obecnie nie ma danych wskazujących na podobną korzyść z tych terapii w chorobie tętniaka BAV.
Leczenie choroby BAV obecnie nie obejmuje statyn, które mogą potencjalnie ograniczać poszerzenie aorty poprzez zmniejszenie ekspresji metaloproteinazy macierzy i poprawę funkcji śródbłonka poprzez zwiększoną śródbłonkową syntazę tlenku azotu.31 Niedawne, randomizowane, kontrolowane placebo badanie z udziałem uczestników z łagodnym lub umiarkowanym zwężeniem aorty wykazało, że statyny nie zmieniają zdarzeń związanych z zastawką aortalną ani progresji zwężenia zastawki aortalnej.31 Jednak tylko ≈5% uczestników badania miało BAV. Dalsze badania skoncentrowane na wpływie statyn na rozszerzenie, rozwarstwienie i pęknięcie AscAo u pacjentów z chorobą BAV są uzasadnione.
Chirurgia
Optymalny czas operacji aorty u pacjentów z BAV bez wskazania do operacji zastawki pozostaje niepewny ze względu na ograniczone dane na temat historii naturalnej bezobjawowego poszerzenia aorty (ryc. 2). Średnica AscAo jest najczęściej wykorzystywanym wymiarem do określania wielkości poszerzonej aorty i stanowi główne kryterium rekomendacji operacji planowej u bezobjawowych chorych z tętniakiem aorty. W aktualnych wytycznych stwierdza się, że operacja naprawy korzenia aorty lub wymiany AscAo jest wskazana u pacjentów z TAV, jeśli średnica aorty lub AscAo wynosi ≥55 mm, oraz że wzory uwzględniające wysokość i pole przekroju poprzecznego aorty dla pacjentów o niskim wzroście 25, 32, 33 Dolny próg (≥50 mm) jest zalecany u pacjentów z Marfanem i BAV. Jednak na podstawie ostatnich długoterminowych badań obserwacyjnych różnice między obiema jednostkami są znaczące. Pacjenci z BAV prawdopodobnie mieszczą się pomiędzy dwoma skrajnościami spektrum schorzeń reprezentowanych przez zespół Marfana i tętniaka zwyrodnieniowego AscAo, a kryteria wielkości interwencji chirurgicznej mogą znajdować się pośrodku między tymi ustalonymi dla obu chorób (odpowiednio 50 i 55 mm). U pacjentów z BAV z czynnikami ryzyka, takimi jak koarktacja aortalna, ciężkie zwężenie aorty lub FDR z wywiadem pęknięcia lub rozwarstwienia aorty, operacja jest wskazana, gdy AscAo wynosi ≥50 mm, a u pacjentów poddawanych planowej wymianie zastawki aortalnej, gdy wynosi ≥45 mm. Wykazano, że tempo ekspansji jest kolejnym ważnym czynnikiem prognostycznym pęknięcia. Tempo wzrostu powyżej 10 mm / rok było tradycyjnie uważane za wskazanie do zabiegu operacyjnego.34 Ostatnie postępy w dziedzinie obrazowania układu sercowo-naczyniowego poprawiły powtarzalność pomiarów seryjnych. W związku z tym panuje ogólna zgoda co do przyjęcia tempa rozszerzania powyżej 3 mm / rok jako wartości odcięcia wskazującej na operację, pod warunkiem, że porównania zostały wykonane dokładnie obok siebie, przy użyciu tej samej techniki obrazowania i na tym samym poziomie aorta. Na koniec należy dokładnie rozważyć kryteria interwencji w stosunku do ryzyka chirurgicznego, zarówno dla pacjenta (wiek, choroby współistniejące itp.), Jak i dla ośrodka. W najlepszych ośrodkach obecna śmiertelność szpitalna z powodu planowego zabiegu ascAo u młodych pacjentów bez chorób współistniejących wynosi około 2% .34,35 Charakterystyka pacjentów, dysfunkcja zastawkowa aorty, lokalizacja poszerzenia aorty i rodzaj operacji powinny być brane pod uwagę w procesie podejmowania decyzji .
Istnieje kilka możliwych opcji chirurgicznych, a wybór zależy od lokalizacji tętniaka, dystalnego zasięgu zajęcia aorty i pożądanego stanu antykoagulacji (Tabela 2). 36, 37 Jeśli naprawa zastawki lub Rozważana jest interwencja oszczędzająca zastawkę, TEE można wykonać przed lub śródoperacyjnie w celu określenia anatomii guzków i AscAo.38
Tabela 2. Opcje chirurgiczne w przypadku choroby dwupłatkowej zastawki aortalnej
| Technika chirurgiczna | Rozważania |
| Aortoplastyka redukcyjna z / bez zewnętrznego owinięcia syntetycznego | • Generalnie niezalecane (ryzyko nawrotu dylatacji) • Alternatywa dla pacjentów z wysokim s pilne ryzyko (zwłaszcza jeśli zatoki nie są znacząco rozszerzone) |
| Zastąpienie korzenia aorty i AscAo reimplantacją ujść wieńcowych (procedura Bentalla) | Standardowa technika w pacjenci ze znaczną chorobą zastawkową i rozszerzeniem AscAo |
| Wymiana zastawki aortalnej i oddzielna naprawa aorty nadwieńcowej | • Generalnie nie zaleca się (ryzyko postępującego poszerzenia zatoki) • Alternatywa dla starszych pacjentów ze zwężeniem BAV, normalną wielkością zatok i poszerzeniem nadwieńcowej AscAo |
| Zastawkowa wymiana aorty | Dopuszczalna opcja dla młodych pacjentów z prawidłową funkcjonujący BAV |
| Autoprzeszczep płucny | • Generalnie niezalecany (ryzyko rozszerzenia autoprzeszczepu) • Alternatywa dla dzieci, nastolatków lub młodych kobiet, które chcą zajść w ciążę |
| Naprawa zastawki aortalnej | Dopuszczalna opcja przy starannym doborze pacjenta |