Poloniumelement-Fakten
Das chemische Element Polonium wird als Chalkogen und Metalloid klassifiziert. Es wurde 1898 von Marie und Pierre Curie entdeckt.

Datenzone
| Klassifizierung: | Polonium ist ein Chalkogen und ein Metalloid. |
| Farbe: | silbergrau |
| Atomgewicht : | (209), keine stabilen Isotope |
| Zustand: | fest |
| Schmelzpunkt: | 254 oC, 527 K |
| Siedepunkt: | 960 oC, 1233 K |
| Elektronen: | 84 |
| Protonen: | 84 |
| Neutronen in den am häufigsten vorkommenden Isotopen: | 125 |
| Elektronenhüllen: | 2,8 , 18,32,18,6 |
| Elektronenkonfiguration: | 4f14 5d10 6s2 6p4 |
| Dichte bei 20 ° C: | 9,4 g / cm3 |
Mehr anzeigen, einschließlich: Wärme, Energie, Ochse idation,
Reaktionen, Verbindungen, Radien, Leitfähigkeiten
| Atomvolumen: | 22,23 cm3 / mol |
| Struktur: | einfache kubische |
| Härte: | – |
| Spezifische Wärmekapazität | 0,12 J g-1 K-1 0,12 |
| Schmelzwärme | 13 kJ mol-1 |
| Zerstäubungswärme | 142 kJ mol-1 |
| Verdampfungswärme | 120 kJ mol-1 |
| 1. Ionisierungsenergie | 812 kJ mol-1 |
| 2. Ionisierungsenergie | – |
| 3. Ionisierungsenergie | – |
| Elektronenaffinität | 180 kJ mol-1 |
| Minimale Oxidationszahl | -2 |
| min. gemeinsame Oxidationsnummer | -2 |
| Maximale Oxidationszahl | 6 |
| max. gemeinsame Oxidation Nr. | 4 |
| Elektronegativität (Pauling-Skala) | 2.0 |
| Polarisierbarkeit Volumen | 6,8 Å3 |
| Reaktion mit Luft | mild, ⇒ PoO2 |
| Reaktion mit 15 M HNO3 | – |
| Reaktion mit 6 M HCl | mild, ⇒ PoCl2 |
| Reaktion mit 6 M NaOH | keine |
| Oxid (e) | PoO2, PoO2 |
| Hydrid (e) | PoH2 |
| Chlorid (e) | PoCl2 |
| Atomradius | 190 pm |
| Ionenradius (1+ Ion) | – |
| Ionenradius (2+ Ionen) | – |
| Ionen Radius (3+ Ion) | – |
| Ionenradius (1-Ion) | – |
| Ionenradius (2-Ionen) | – |
| Ionenradius (3-Ionen) | – |
| Wärmeleitfähigkeit | 0,2 W m-1 K-1 |
| Elektrische Leitfähigkeit | 0,7 × 10 6 S m-1 |
| Gefrier- / Schmelzpunkt: | 254 oC, 527 K |

Marie Curie 1883, 16 Jahre alt. Polonium war das erste Element, das sie 15 Jahre später entdeckte.
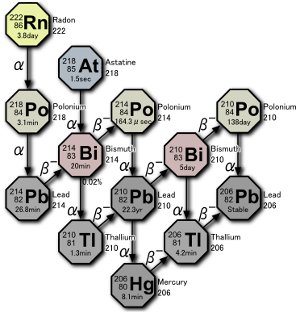
Teil des Uranzerfallsreihe. In der Natur entstehen drei Isotope von Polonium, entweder durch den Zerfall des Radongases selbst oder durch den Zerfall der Atome infolge des Zerfalls des Radons. Bild von Tosaka.
Entdeckung von Polonium
Polonium war das erste von Marie und Pierre Curie entdeckte Element.
Sie entdeckten 1898 in Paris Polonium und dann Radium, während sie die Radioaktivität in Pechblende (Uranoxid) untersuchten / p>
Sie schrieben: „Wir glauben, dass die Substanz, die wir aus Pechblende extrahiert haben, ein noch nie bekanntes Metall enthält, ähnlich wie Wismut in seinen analytischen Eigenschaften. Wenn die Existenz dieses neuen Metalls bestätigt wird, schlagen wir vor, dass dies der Fall sein sollte.“ Polonium genannt nach dem Namen des Herkunftslandes eines von uns. “
Entsprechend den Wünschen der Curies ist Polonium nach Polen benannt, wo Marie Curie geboren und aufgewachsen ist.
Die Gefahren der Arbeit mit radioaktiven Elementen waren bei den Curies nicht bekannt machten ihre Entdeckungen. Ihre Laborhefte aus dieser Zeit sind so radioaktiv, dass sie jetzt in einem mit Blei ausgekleideten Gehäuse aufbewahrt werden. (1)
Aussehen und Eigenschaften
Schädliche Wirkungen:
Polonium ist sowohl aufgrund seiner chemischen Toxizität als auch seiner Radioaktivität schädlich. Polonium-210 ist ein Alpha-Emitter. Als solches ist es sehr gefährlich, wenn es verschluckt oder eingeatmet wird.Die Exposition gegenüber Polonium erhöht das Risiko, an verschiedenen Krebsarten zu erkranken.
Eigenschaften:
Polonium ist ein seltenes, silbergraues, radioaktives, niedrigschmelzendes Metalloid.
Polonium reagiert leicht mit verdünnten Säuren, jedoch nur geringfügig mit Alkalien.
Alle seine Isotope sind radioaktiv.
210Po strahlt blau, da die Luft um ihn herum durch den Zerfall angeregt wird Produkte. 1 Gramm Po emittiert so viele Alpha-Partikel wie 5 Kilogramm Radium. ] Die durch den Alpha-Zerfall von Polonium freigesetzte Energie ist beträchtlich und erwärmt den Raum um ihn herum. Die freigesetzte Energie ist so groß (140 W / g), dass eine Kapsel mit etwa einem halben Gramm eine Temperatur über 500 ° C erreicht.
Verwendung von Polonium
Die von emittierten Alphastrahlen Polonium kann verwendet werden, um statische Elektrizität zu eliminieren, die bei Prozessen wie Rollen von Papier, Draht und Blech erzeugt wird. Allerdings werden Betastrahlenquellen häufiger verwendet, da sie weniger gefährlich sind.
210Po kann als Atomwärmequelle verwendet werden, aber aufgrund der kurzen Halbwertszeit des Isotops (138,4 Tage) liefert es keinen Strom für Langzeitanwendungen.
] Polonium wird auch in antistatischen Bürsten verwendet, um Staub auf fotografischem Film zu beseitigen. Es ist in Bürsten versiegelt, um die radioaktiven Emissionen zu kontrollieren.
Überfluss und Isotope
Überfluss Erdkruste: In der Größenordnung von 1 Teil pro Billiarde.
Überfluss Sonnensystem: vernachlässigbar
Kosten , rein: pro 100 g
Kosten, Masse: pro 100 g
Quelle: Polonium ist aufgrund der kurzen Halbwertszeit aller seiner Isotope ein sehr seltenes Element. Es kommt in winzigen Mengen in Uranerzen vor. Es kann erhalten werden, indem natürliches Wismut 209Bi mit Neutronen bombardiert wird, um 210Bi zu ergeben, das dann über β-Zerfall auf 210Po zerfällt. Jedes Jahr werden ungefähr 100 g Polonium synthetisiert.
Isotope: Polonium hat 29 Isotope, deren Halbwertszeiten bekannt sind, mit Massenzahlen von 190 bis 218. Keine ist stabil. Das stabilste Isotop ist 209Po, mit einer Halbwertszeit von 102 Jahren.

Zitieren Sie diese Seite
Für Online-Links kopieren Sie bitte eine der folgenden Seiten und fügen Sie sie ein:
<a href="https://www.chemicool.com/elements/polonium.html">Polonium</a>
oder
<a href="https://www.chemicool.com/elements/polonium.html">Polonium Element Facts</a>
Um diese Seite in einem akademischen Dokument zu zitieren, verwenden Sie bitte das folgende MLA-konforme Zitat:
"Polonium." Chemicool Periodic Table. Chemicool.com. 08 Oct. 2012. Web. <https://www.chemicool.com/elements/polonium.html>.