Análise de custo-benefício do uso de alta frequência de oscilação da parede torácica (HFCWO) em pacientes com não cística Bronquiectasia de fibrose
Resumo
Bronquiectasia é uma doença crônica progressiva caracterizada por dilatação patológica irreversível dos brônquios pulmonares. Os tratamentos para bronquiectasias visam mobilizar as secreções das vias aéreas, reduzir a inflamação, prevenir infecções respiratórias, melhorar a ventilação, minimizar o número de exacerbações e melhorar a qualidade de vida de uma pessoa. A oscilação da parede torácica de alta frequência (HFCWO) é um tratamento de desobstrução das vias aéreas usado atualmente para uma série de doenças crônicas que comprometem as vias aéreas, incluindo bronquiectasia de fibrose não cística. Este estudo avaliou o impacto econômico do tratamento de HFCWO administrado pelo SmartVest® Airway Clearance System na utilização e custo de cuidados de saúde relacionados à bronquiectasia.
Métodos
Os resultados de um resultado de revisão de caso publicado anteriormente um estudo clínico baseado nos autores forneceu a base para esta análise de custo-eficácia. Exacerbações relacionadas à bronquiectasia, incluindo o número de hospitalizações, visitas ao departamento de emergência (ED) e frequência de prescrições de antibióticos foram registradas para cada paciente por um período de um ano antes do uso de SmartVest (controle de padrão de cuidado) e por um período de um ano após o início do SmartVest usar. As taxas de exacerbação para um ano pré-SmartVest e um ano pós-SmartVest foram comparadas. As exacerbações foram verificadas nos prontuários médicos do paciente e por entrevista por telefone. Os custos com antibióticos foram determinados usando “preços de farmácia com desconto on-line”, enquanto os custos de internação e de emergência foram determinados usando o Resumo Estatístico do Projeto de Custo e Utilização de Saúde (HCUP) # 146 e o banco de dados HCUP National Inpatient Sample (NIS) 2013.
Resultados
Os resultados clínicos publicados anteriormente de cinquenta e nove pacientes SmartVest com bronquiectasia não fibrose cística serviram de base para esta análise. Quando os dados dos resultados foram analisados, use o SmartVest, em comparação com o padrão de controle de cuidados, foi associado a resultados estatisticamente significativos; uma redução de 58% no custo do antibiótico, uma redução de 63% no custo da consulta de emergência e uma redução de 60% no custo de hospitalização. No total, a análise de custo resultou em uma economia anual de $ 3.045 por paciente por ano de uso do SmartVest.
Conclusões
A eficácia clínica do uso do SmartVest como tratamento para pacientes com bronquiectasia não fibrose cística foi previamente verificada por uma redução significativa n nas exacerbações relacionadas à bronquiectasia, o que se traduz diretamente em uma redução geral significativa de 60% na utilização e nos custos de saúde nessa população. Além disso, benefícios secundários, como o potencial para reduzir as readmissões hospitalares e o potencial de impacto na dissuasão da resistência aos antibióticos, podem ter benefícios ainda maiores do que diminuir o custo.
Palavras-chave
SmartVest, tórax de alta frequência oscilação de parede, HFCWO, bronquiectasia, custo
Introdução
Bronquiectasia é uma doença crônica e etiologicamente heterogênea. As características comuns da bronquiectasia são falta de ar, exacerbações frequentes, tosse crônica, hemoptise e produção excessiva de expectoração. A doença é tipicamente caracterizada por ciclos de eliminação mucociliar prejudicada, infecção brônquica e inflamação, resultando em dano estrutural às vias aéreas com dilatação permanente e anormal.1 A bronquiectasia pode ser o resultado de uma ampla gama de doenças respiratórias e sistêmicas, incluindo fibrose cística, síndromes ciliares discinéticas, lesões por inalação / aspiração, estados de imunodeficiência primária e adquirida e uma série de condições reumáticas e inflamatórias.2 Bronquiectasia é observada em 7% a 52% dos pacientes com asma ou doença pulmonar obstrutiva crônica (DPOC) .3,4 , 37
Seitz, et al, analisou uma amostra de 5% do banco de dados de sinistros ambulatoriais do Medicare para bronquiectasia entre beneficiários com idade ≥65 anos de 2000 a 2007.6 O banco de dados contém informações sobre o nível de sinistros de serviços ambulatoriais não institucionais fornecedores. Bronquiectasia foi identificada pelo banco de dados usando os códigos da Classificação Internacional de Doenças, Nona Revisão, Modificação Clínica (CID-9-CM). A população do estudo incluiu > 2 milhões de indivíduos únicos inscritos no Medicare Parte B por pelo menos um mês de 2000 a 2007. O estudo determinou que a prevalência de bronquiectasia na população geral era de 1.106 casos por 100.000 pessoas durante o período de revisão de oito anos. O estudo também descobriu que a prevalência de bronquiectasia em beneficiários do Medicare aumentou 8,7% entre 2000 e 2007 e a taxa de hospitalização por bronquiectasia aumentou anualmente a uma taxa de 2.4% entre os homens e 3,0% entre as mulheres.
A carga geral da doença pulmonar avançada está aumentando e, onde existem dados, os custos relacionados à morbidade e mortalidade dessas doenças parecem significativos.2 Isso pode, em parte, ser um reflexo do crescente envelhecimento da população com doença pulmonar crônica, que tem um aumento desproporcional nos custos de saúde; a taxa de hospitalização devido a doença pulmonar crônica aumenta acentuadamente acima dos 50 anos de idade, e particularmente em mulheres mais velhas.2,7 Usando registros de alta de 1997-2010, estimou-se o custo médio hospitalar para cuidados hospitalares em pacientes com um a exacerbação da pneumonia foi de $ 9.300.28 Em 2001, também se estimou que o custo médico anual de cuidados para pessoas nos Estados Unidos com bronquiectasia era de $ 13.244, que é maior do que o custo anual para muitas outras doenças crônicas, como doenças cardíacas ($ 12.000) e DPOC (US $ 11.000) .38 Um estudo de 2005 descobriu que os pacientes com bronquiectasia de fibrose não cística tiveram em média 2,0 dias adicionais por ano no hospital, tiveram 6,1 consultas ambulatoriais adicionais e 27,2 dias a mais de antibioticoterapia em comparação com pacientes sem a doença.9 Em 2005 , os custos do tratamento para bronquiectasia de não fibrose cística foram de $ 630 milhões anualmente.5
Pacientes com bronquiectasia de não fibrose cística podem ter dificuldade para limpar o arw todas as secreções e podem se beneficiar significativamente da terapia de desobstrução das vias aéreas.2 Os objetivos do tratamento para bronquiectasias são mobilizar as secreções das vias aéreas para reduzir a inflamação, prevenir infecções respiratórias, melhorar a ventilação, minimizar o número de exacerbações e melhorar a qualidade de vida do paciente. 10-12 Vários métodos terapêuticos são usados atualmente para limpar as secreções das vias aéreas em pacientes com doença pulmonar, comprometimento da limpeza do muco respiratório ou que estão em risco de desenvolver qualquer uma dessas condições.8 Esses métodos geralmente visam promover a limpeza das secreções reduzindo viscosidade do muco e usando forças de cisalhamento para liberar o muco da parede pulmonar para facilitar a mobilização para facilitar a expectoração. O tratamento padrão envolve terapia combinada com agentes mucolíticos e mucocinéticos, broncodilatadores, terapia antiinflamatória e alguma forma de terapia física / mecânica de desobstrução das vias aéreas.2 A terapia de desobstrução das vias aéreas desempenha um papel crítico, pois ajuda a evitar a retenção de muco carregado de patógenos, que é a origem subjacente da infecção recorrente que causa deterioração pulmonar progressiva.2,13,14 Os métodos de desobstrução das vias aéreas desempenham um papel crítico na manutenção da saúde respiratória ao longo da vida do paciente.
Uma série de desobstrução das vias aéreas métodos estão disponíveis, incluindo fisioterapia respiratória, máscaras de pressão expiratória final positiva, dispositivos orais de alta frequência e oscilação da parede torácica de alta frequência (HFCWO) .2 Máscaras de pressão expiratória final positiva e dispositivos orais de alta frequência requerem esforço ativo, domínio do técnica e / ou agilidade física que pode limitar seu uso.2
HFCWO é usado para desobstrução das vias aéreas em pacientes com uma ampla gama de comprometimento das vias aéreas ng doenças e condições, incluindo distúrbios genéticos e imunológicos, doenças neuromusculares e condições pulmonares obstrutivas, como asma e DPOC.15-18 Em contraste com alguns outros métodos, HFCWO requer atividade mínima do usuário e não é dependente de um provedor de saúde técnica para ser eficaz.2 Estudos clínicos, principalmente em pacientes com fibrose cística, mostraram que o HFCWO é seguro e eficaz.2,15,19-22 O HFCWO fornece pulsos de compressão para a parede torácica por meio de um colete inflável conectado a um gerador de pulsos de ar .2 O gerador produz um fluxo alternado de ar para dentro e para fora do colete que comprime e libera rapidamente a parede torácica dentro de uma faixa de frequências e pressões selecionáveis. A compressão oscilatória transmitida à parede torácica foi relatada para afinar o muco viscoso, desconectar o muco da parede do pulmão e impulsionar o muco das vias aéreas menores em direção às vias aéreas principais, onde pode ser expectorado ou aspirado.2,23, 24 HFCWO pode levar a uma melhora significativa no volume pulmonar de 15 a 57mL e no fluxo de até 1,6L / seg.22
Um estudo de revisão de caso anterior avaliou os resultados clínicos da terapia do SmartVest® Airway Clearance System na exacerbação utilização de cuidados de saúde relacionados com a bronquiectasia e uso de medicamentos em indivíduos com bronquiectasia não fibrose cística.25 O estudo descobriu que o uso de SmartVest resultou em uma redução estatisticamente significativa de 60% nas exacerbações relacionadas à bronquiectasia, incluindo uso de antibióticos, visitas ao departamento de emergência (ED) e hospitalizações . O estudo atual foi projetado para avaliar o impacto econômico da terapia SmartVest nos custos de saúde e antibióticos relacionados à bronquiectasia.
Métodos
Um SmartVest recente (Electromed, Inc., New Prague, MN , EUA) estudo clínico baseado em resultados de revisão de caso serviu de base para esta análise.25 O estudo registrou todas as exacerbações relacionadas à bronquiectasia para incluir o número de hospitalizações, visitas ao pronto-socorro e uso de antibióticos por um período de um ano antes do uso de SmartVest (padrão de controle de cuidados) e, para comparação, por um período de um ano após o início de Uso de SmartVest (tratamento). O estudo incluiu apenas os indivíduos com diagnóstico de bronquiectasia não fibrose cística que usaram SmartVest por pelo menos um ano e cujos prontuários médicos estavam disponíveis por um ano antes do início da terapia SmartVest. Os pacientes foram excluídos se não estivessem em conformidade com o regime de terapia SmartVest prescrito, não pudessem ser contatados por telefone ou tivessem expirado. Todos os dados coletados antes do uso do SmartVest foram capturados por meio dos registros médicos do paciente.
Os registros médicos do paciente foram revisados para todas as exacerbações relacionadas à bronquiectasia que ocorreram durante um período de um ano antes do início da terapia com SmartVest. Os indivíduos foram contatados e entrevistados por telefone para coletar exacerbações relacionadas à bronquiectasia durante o período de um ano após o início da terapia SmartVest. O questionário para a pesquisa por telefone foi desenvolvido com o propósito exclusivo do estudo. Durante a entrevista por telefone, foram feitas perguntas específicas ao sujeito sobre o uso de antibióticos respiratórios, visitas ao pronto-socorro e hospitalizações. A entrevista também indagou se o paciente estava usando SmartVest de acordo com o regime de prescrição do médico.
Os custos dos antibióticos foram determinados usando “preços de farmácia com desconto on-line”, no entanto, o custo das visitas ao consultório e honorários médicos não foram incluídos . Os custos de hospitalização e ED foram determinados usando as estimativas nacionais ponderadas do Projeto de Custo e Utilização de Saúde (HCUP) Amostra Nacional de Pacientes Internos (NIS), 2013, Agência de Pesquisa e Qualidade em Saúde (AHRQ), com base em dados coletados por Estados individuais e fornecidos a AHRQ pelos estados.26 O banco de dados NIS inclui uma amostra de probabilidade estratificada de hospitais de bancos de dados de internação estaduais que incluem hospitalizações de pacientes com Medicare, Medicaid, seguros privados e não segurados.27 O NIS contém dados de 5 a 8 milhões de internações hospitalares de cerca de 1000 hospitais. É designado para aproximar uma amostra de 20% dos hospitais de curto prazo não federais dos EUA, conforme definido pela American Medical Associ ação. O NIS é elaborado a partir de estados que participam do Projeto de Custo e Utilização de Saúde. O NIS contém dados uniformes de internação de pacientes internados em bancos de dados de alta hospitalar mantidos por agências estaduais, associações de hospitais e outras organizações privadas. O número total de altas ponderadas nos EUA com base no HCUP NIS foi 35.597.792,28
Resultados
A revisão dos bancos de dados do HCUP e do Medicare revelou custos de saúde associados para uma exacerbação relacionada à bronquiectasia
ser $ 450 (2012) para uma visita de ED e $ 9.300 (2010) para uma hospitalização com pneumonia. A permanência hospitalar prolongada com base em complicações ou comorbidades não foi calculada. Usando cálculos de preços de farmácia com desconto online, o custo de um regime de antibióticos padrão para pneumonia foi de $ 290 (2016). Os honorários médicos para uma visita ao consultório e a prescrição subsequente não estavam disponíveis para cálculo.
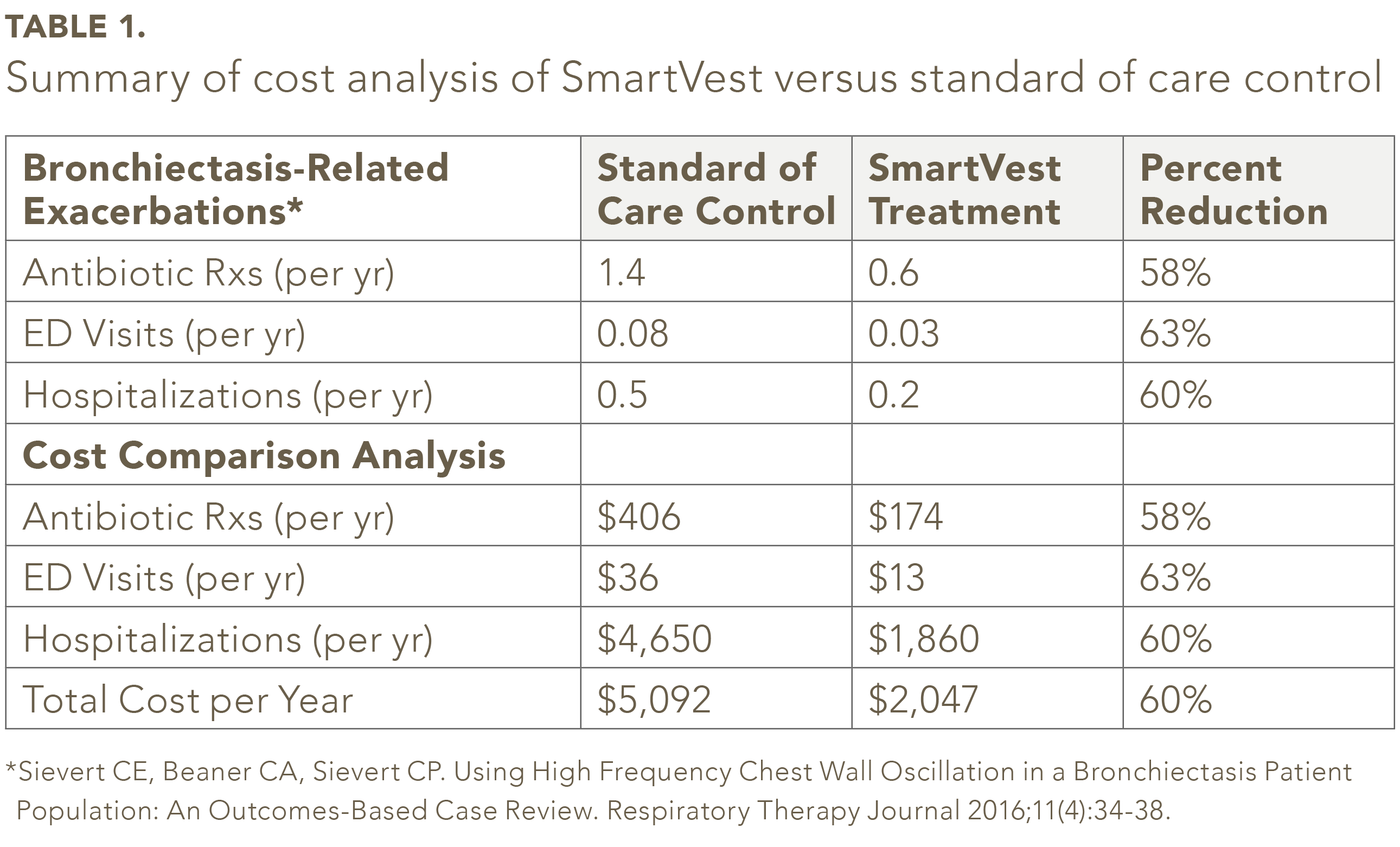
Dos 104 pacientes com bronquiectasia SmartVest identificados, cinquenta e nove pacientes preencheram os critérios de inclusão / exclusão.25 Na população do estudo, o número médio de prescrições de antibióticos por ano foi 58% menor para SmartVest (0,6 / ano) em comparação com o controle de tratamento padrão (1,4 / ano) (ver Tabela 1). O uso de SmartVest também reduziu significativamente as visitas ao pronto-socorro em 63% (0,08 / ano versos 0,03 / ano) e as hospitalizações em 60% (0,5 / ano versos 0,2 / ano). Os custos anuais por paciente para antibióticos para pacientes tratados com SmartVest foram cerca de US $ 233 mais baixos em comparação com aqueles tratados com o tratamento padrão (ver Tabela 1). As hospitalizações, após um ano de uso do SmartVest, também foram reduzidas significativamente em $ 2.790 por paciente por ano. No total, os resultados gerais revelaram uma economia anual de $ 3.045 por paciente por ano de uso do SmartVest.
A análise não contabilizar quaisquer despesas médicas / consultivas incorridas para obter uma prescrição de antibióticos sem hospitalização. Além disso, a análise não levou em consideração uma visita ao consultório para uma potencial exacerbação que não resultou em prescrição ou hospitalização. Além disso, a análise não levou em conta despesas adicionais se a exacerbação foi uma pneumonia de cepa bacteriana resistente a antibióticos que supostamente pode custar mais de US $ 15.000 para cada episódio.
Discussão
O propósito de a análise foi avaliar o impacto econômico do uso do SmartVest nos custos médicos associados à bronquiectasia em comparação com um padrão de controle de tratamento. Até onde sabemos, este é o primeiro estudo a avaliar os custos de saúde do tratamento de pacientes com bronquiectasia não fibrose cística com HFCWO.O custo geral incluiu o custo de antibióticos, visitas ao pronto-socorro e hospitalizações relacionadas a exacerbações associadas à bronquiectasia não fibrose cística. O estudo demonstrou uma redução significativa na utilização de serviços de saúde e seus custos associados quando pacientes com bronquiectasia foram tratados com SmartVest por um ano. O custo geral foi reduzido em 60%, o que se traduz em uma economia de $ 3.045 por paciente por ano.
Um estudo recente que avaliou altas hospitalares, readmissões e visitas ao pronto-socorro para DPOC ou bronquiectasia em adultos nos Estados Unidos encontraram de 2001 a 2012 o número de altas hospitalares em 88.000.31 O estudo também descobriu que cerca de 7% dos pacientes com DPOC ou bronquiectasias foram readmitidos em 30 dias com DPOC ou bronquiectasias como o diagnóstico principal.31 Em contraste, a taxa de alta diminuiu para outras doenças.31 A razão para o aumento significativo na DPOC e nas consultas de bronquiectasias no hospital e no pronto-socorro não está clara, pois foi observada uma redução significativa nas taxas de tabagismo. No entanto, pode refletir o potencial subdiagnóstico da doença e a natureza de longo prazo da DPOC e bronquiectasia em uma população em envelhecimento.31
Um estudo anterior baseado em resultados de revisão de caso relatou que o uso de SmartVest reduziu as hospitalizações em 1,5 vezes, 25 indicando o benefício de custo de HFCWO na redução da carga de utilização de cuidados de saúde. Outros estudos também avaliaram fatores (tanto do sistema quanto do paciente) que podem diminuir a readmissão em pacientes com DPOC e são, pelo menos em parte, relevantes para pacientes com bronquiectasia. Esses fatores incluem a continuidade dos cuidados primários prestados aos pacientes ou pneumologista, intervenção do coordenador de altas e a extensão ou tipo de terapia respiratória.32-34
A redução no número de exacerbações relacionadas à bronquiectasia também pode afetar a qualidade de vida do paciente.35,36 Em uma população de pacientes com DPOC, o uso de SmartVest foi associado a melhora significativa no escore de cinco sintomas P = 0,002 (classificação de escarro, sibilo, tosse, falta de ar e tolerância ao exercício ) .36 O tratamento SmartVest também demonstrou uma melhora significativa no Questionário Respiratório de St. George (SGRQ) P = 0,02, enquanto nenhuma melhora foi observada em pacientes tratados com tratamento convencional.36 Da mesma forma, nosso estudo anterior baseado em resultados de revisão de caso descobriu que 68 % dos sujeitos indicaram durante a entrevista por telefone que o uso de SmartVest melhorou significativamente sua qualidade de vida.25
Diversas limitações ao desenho do estudo devem ser consideradas vermelho ao interpretar os resultados. O tamanho do paciente do estudo foi pequeno, e as hospitalizações, visitas ao pronto-socorro e dados de uso de antibióticos após o início da terapia SmartVest foram obtidos principalmente por meio de entrevista com o paciente. O estudo pode ser considerado conservador devido a nenhum custo adicionado para honorários médicos associados a uma visita ao consultório que resulte em uma prescrição de antibióticos ou, nenhum custo adicionado para uma visita ao consultório que não resultou em uma prescrição de antibiótico. Além disso, a confiança nas bases de dados HCUP, NIS e AHRQ, que dependem dos diagnósticos inseridos nas reivindicações, podem ser codificados incorretamente ou não codificados de forma alguma, potencialmente introduzindo um erro de medição em relação às variáveis baseadas em ICD-9-CM.
Reduzir os custos de utilização da saúde, como o uso de antibióticos, visitas ao pronto-socorro e hospitalizações são objetivos prioritários de diretivas recentes de saúde, como a Lei de Cuidados Acessíveis (ACA). Por exemplo, a ACA estabeleceu o Programa de Redução de Readmissões de Hospitais (HRRP), que instruiu a CMS a penalizar hospitais reduzindo os pagamentos de reembolso por excesso de readmissões de pacientes para a mesma condição. HRRP identificou originalmente as três principais “condições aplicáveis” para a medição de readmissão focada para incluir infarto agudo do miocárdio, insuficiência cardíaca e pneumonia. Além disso, o CMS finalizou recentemente a expansão de condições adicionais aplicáveis começando com o programa do ano fiscal de 2015 para incluir pacientes readmitidos por um exacerbação aguda da DPOC. A redução significativa na utilização de cuidados de saúde e hospitalizações para pacientes com bronquiectasia não cística usando SmartVest, conforme demonstrado neste estudo e em outros, pode desempenhar um papel crítico em ajudar os hospitais a reduzir as readmissões e, portanto, não ser penalizado.
Para pacientes com infecções das vias aéreas resistentes a antibióticos orais, o fardo é muito maior e mais sério. Os antibióticos intravenosos complicam muito o cuidado porque é necessário hospitalização ou monitoramento domiciliar. O tratamento para esses pacientes inclui a colocação de um cateter venoso central e coordenação de as doses de medicamentos que muitas vezes devem ser administradas ple vezes por dia, exames de sangue regulares para monitorar os efeitos colaterais e medição dos níveis de sangue do antibiótico por muitos dias, etapas que se tornam caras e perturbam a vida dos pacientes.
A Organização Mundial da Saúde (OMS) declarou que a resistência microbiana aos antibióticos representa uma “grande ameaça global com implicações devastadoras para a saúde pública”. A resistência antimicrobiana ameaça a prevenção e o tratamento eficazes de uma gama cada vez maior de infecções causadas não apenas por bactérias, mas também por vírus e fungos. Os Centros dos EUA para Controle e Prevenção de Doenças (CDC) consideram a resistência antimicrobiana uma de suas principais preocupações e prioridades. Só nos Estados Unidos, pelo menos 2 milhões de pessoas são infectadas por bactérias resistentes a antibióticos e pelo menos 23.000 pessoas morrem a cada ano como resultado direto dessas infecções.39 Em resposta à preocupação mundial, os Centros de Medicare & Medicaid Services (CMS) lançou recentemente uma proposta de mudança de regra em suas Condições de Participação que, entre outras mudanças, exigiria que os hospitais implementassem programas de administração de antibióticos para participar dos programas Medicare e Medicaid. A administração de antibióticos inclui a melhoria dos resultados do paciente pela adoção de processos e procedimentos que reduzem a incidência de infecções por pa atenção especial à pneumonia, como tratamento preventivo. Como um benefício secundário aos resultados de custo-benefício deste estudo, uma redução significativa na necessidade de antibióticos em pacientes com bronquiectasia pelo uso de SmartVest pode ter benefícios ainda maiores do que diminuir o custo. Um tratamento disponível que poderia reduzir significativamente as infecções respiratórias e, portanto, a necessidade de antibióticos se encaixa bem nos programas de controle de infecção do hospital.
Em resumo, a eficácia clínica da limpeza das vias aéreas HFCWO demonstrada pelo SmartVest em pacientes com DPOC36 e aqueles com bronquiectasia, 25 e a redução significativa nos custos com antibióticos, DE e hospitalização observada neste estudo apóia o custo-benefício do uso do SmartVest e defende a cobertura de seguro do SmartVest pelos pagadores. Além disso, benefícios secundários, como o potencial de reduzir as readmissões hospitalares e o potencial de impacto na dissuasão da resistência aos antibióticos, podem ter benefícios ainda maiores do que diminuir o custo.
Baixe o texto do estudo
Agradecimentos
Os autores gostariam de agradecer a Elizabeth Goodwin, PhD, pelo apoio editorial.
- King P. Patogênese da bronquiectasia. Paediatr Respir Rev 2011; 12 (2): 104-110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Compressão torácica de alta frequência: uma terapia prática para pacientes com bronquiectasia. Respiratory Therapy 2008; 3 (1): 22-26.
- Patel IS, Vlahos I, Wilkinson TM, et al. Bronquiectasia, índices de exacerbação e inflamação na doença pulmonar obstrutiva crônica. Am J Respir Crit Care Med 2004; 170 (4): 400-407. 10.1164 / rccm.200305-648OC
- Gono H, Fujimoto K, Kawakami S, et al. Avaliação da espessura da parede das vias aéreas e do aprisionamento aéreo por TCAR em asma assintomática. Eur Respir J 2003; 22 (6): 965-971.
- Weycker D, Edelsberg J, Oster G, et al. Prevalência e custo econômico da bronquiectasia. Clinical Pulmonary Medicine 2005; 12 (4): 205-209.
- Seitz AE, Olivier KN, Adjemian J, et al. Tendências em bronquiectasia entre beneficiários do Medicare nos Estados Unidos, 2000 a 2007. CHEST Journal 2012; 142 (2): 432-439.
- Seitz AE, Olivier KN, Steiner CA, et al. Tendências e carga de hospitalizações associadas à bronquiectasia nos Estados Unidos, 1993-2006. Chest 2010; 138 (4): 944-949. 10.1378 / chest.10-0099
- Seitz AE, Olivier KN, Steiner CA, et al. Tendências e carga de hospitalizações associadas à bronquiectasia nos Estados Unidos, 1993-2006. CHEST Journal 2010; 138 (4): 944-949.
- Weycker D, Edelsberg J, Oster G, et al. Prevalência e custo econômico da bronquiectasia. Clinical Pulmonary Medicine 2005; 12: 205-209.
- Fibrose. AoCPiC. Normas de atendimento e boas práticas clínicas para o manejo da fisioterapia da fibrose cística 2011. Disponível em: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio 11 de junho.
- O’Donnell AE. Bronquiectasia. Chest 2008; 134 (4): 815-823. 10.1378 / chest.08-0776
- Barker AF. Bronquiectasia. N Engl J Med 2002; 346 (18): 1383-1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Terapias não farmacológicas de desobstrução das vias aéreas: diretrizes de prática clínica baseadas em evidências ACCP. Chest 2006; 129 (1 Supl): 250S-259S. 10.1378 / chest.129.1 suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Treatment of mucociliary dysfunction. Chest 1996; 110 (4): 1048-1057.
- Arens R, Gozal D, Omlin KJ, et al. Comparação da compressão torácica de alta frequência e fisioterapia respiratória convencional em pacientes hospitalizados com fibrose cística. Am J Respir Crit Care Med 1994; 150 (4): 1154-1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Oscilação de alta frequência das vias aéreas e da parede torácica. Respir Care 2002; 47 (7): 797-807.
- Hansen LG, Warwick WJ.Sistema de compressão torácica de alta frequência para auxiliar na eliminação do muco do pulmão. Biomed Instrum Technol 1990; 24 (4): 289-294.
- Lange DJ, Lechtzin N, Davey C, et al. Oscilação da parede torácica de alta frequência em ALS: um estudo exploratório randomizado controlado. Neurology 2006; 67 (6): 991-997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. O efeito de longo prazo da terapia de compressão torácica de alta frequência nas complicações pulmonares da fibrose cística. Pediatr Pulmonol 1991; 11 (3): 265-271.
- Kluft J, Beker L, Castagnino M, et al. Uma comparação de tratamentos de drenagem brônquica na fibrose cística. Pediatr Pulmonol 1996; 22 (4): 271-274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P
- Scherer TA, Barandun J, Martinez E, et al. Efeito das vias respiratórias orais de alta frequência e da oscilação da parede torácica e da fisioterapia respiratória convencional na expectoração em pacientes com fibrose cística estável. Chest 1998; 113 (4): 1019-1027.
- Nicolini A, Cardini F, Landucci N, et al. Eficácia do tratamento com oscilação torácica de alta frequência em pacientes com bronquiectasia. BMC Pulm Med 2013; 13: 21. 10.1186 / 1471-2466-13-21
- Osman LP, Roughton M, Hodson ME, et al. Estudo comparativo de curto prazo da oscilação da parede torácica de alta frequência e técnicas europeias de desobstrução das vias aéreas em pacientes com fibrose cística. Thorax 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Desobstrução das vias aéreas assistida por alta frequência. Respir Care 2007; 52 (9): 1224-1235; discussão 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Usando a oscilação da parede torácica de alta frequência em uma população de pacientes com bronquiectasia: uma revisão de caso baseada em resultados. Respiratory Therapy Journal 2016; 11 (4): 34-38.
- HCUP. Visão geral da amostra do departamento de emergência nacional (NEDS) 2016. Disponível em: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Visão geral das amostras nacionais (nacionais) de pacientes internados. Disponível em: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C. Custos para estadias em hospitais no Estados Unidos, 2010: Resumo Estatístico # 146. Resumos estatísticos do Projeto de Custo e Utilização de Saúde (HCUP). Rockville (MD): Agency for Healthcare Research and Quality (EUA); 2006.
- Stein PD, Matta F. Custos de visitas a serviços de emergência e hospitalizações por hipertensão arterial pulmonar.
J Epidemiol Public Health Rev 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Reembolso de gerenciamento de cuidados transitórios para reduzir a readmissão da DPOC. Chest
2014; 145 (1): 149-155. 10.1378 / chest.13-0787 - Ford ES. Altas hospitalares, readmissões e visitas ao pronto-socorro para DPOC ou bronquiectasia entre adultos nos EUA: resultados da amostra de pacientes internados em todo o país de 2001 a 2012 e da amostra do Departamento de Emergência em todo o país de 2006-2011 Chest 2015; 147 (4): 989-998. 10.1378 / chest.14-2146
- Sharma G, Kuo YF, Freeman JL, et al. Consulta de acompanhamento ambulatorial e visita ao departamento de emergência de 30 dias e readmissão em pacientes hospitalizados por doença pulmonar obstrutiva crônica. Arch Intern Med 2010; 170 (18): 1664-1670. 10.1001 / archinternmed.2010.345
- Lainscak M, Kadivec S, Kosnik M, et al. A intervenção do coordenador de alta evita hospitalizações em pacientes com DPOC: um ensaio clínico randomizado. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O, Sewell L, Morgan MD, et al. Programa de reabilitação pulmonar ambulatorial de curta duração reduz a readmissão após uma hospitalização por exacerbação de doença pulmonar obstrutiva crônica. Respirology 2013; 18 (7): 1063-1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. A terapia de umidificação do ar de longo prazo é econômica para pacientes com doença pulmonar obstrutiva crônica moderada ou grave ou bronquiectasia. Value Health 2014; 17 (4): 320-327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. Um estudo piloto do impacto da oscilação da parede torácica de alta frequência em pacientes com doença pulmonar obstrutiva crônica com hipersecreção de muco. Int J Chron Obstruct Pulmon Dis 2011; 6: 693-699. 10.2147 / COPD. S22896.
- Martınez-Garcıa MA, et al. Valor prognóstico da bronquiectasia em pacientes com doença pulmonar obstrutiva crônica moderada a grave. Am J Respir Crit Care Med 2013; Vol 187, Iss. 8, pp 823-831.
- O’Donnell AE. Bronquiectasia. Chest 2008; 134: 815–82.
- Site do Centro de Controle e Prevenção de Doenças – Resistência a antibióticos / antimicrobianos https://www .cdc.gov / drugresistance /