Analiza rentabilă a utilizării oscilației peretelui toracic cu frecvență înaltă (HFCWO) la pacienții cu non-chistic Bronșiectazie prin fibroză
Rezumat
Bronșiectazia este o boală cronică progresivă caracterizată prin dilatarea patologică ireversibilă a bronhiilor pulmonare. Tratamentele pentru bronșiectazii vizează mobilizarea secrețiilor căilor respiratorii, reducerea inflamației, prevenirea infecțiilor respiratorii, creșterea ventilației, minimizarea numărului de exacerbări și îmbunătățirea calității vieții unei persoane. Oscilația peretelui toracic de înaltă frecvență (HFCWO) este un tratament de eliminare a căilor respiratorii utilizat în prezent pentru o serie de boli cronice care compromit căile respiratorii, inclusiv bronșiectazii cu fibroză non-chistică. Acest studiu a evaluat impactul economic al tratamentului HFCWO furnizat de sistemul de eliminare a căilor aeriene SmartVest® asupra utilizării și costului asistenței medicale legate de bronșiectazii.
Metode
Rezultatele unui rezultat al revizuirii cazului publicat anterior -studiul clinic realizat de autori a oferit baza acestei analize a rentabilității. Exacerbările legate de bronșiectazii, inclusiv numărul de spitalizări, vizitele secției de urgență (DE) și frecvența prescripțiilor de antibiotice au fost înregistrate pentru fiecare pacient pentru o perioadă de un an înainte de utilizarea SmartVest (standard de control al îngrijirii) și pentru o perioadă de un an după începerea SmartVest. utilizare. Ratele de exacerbare pentru un an pre-SmartVest și un an după SmartVest au fost comparate. Exacerbările au fost verificate atât din dosarele medicale ale pacientului, cât și prin interviu telefonic. Costurile antibioticelor au fost determinate folosind „prețuri online pentru farmacii cu reducere”, în timp ce costurile de spitalizare și ED au fost determinate utilizând Raportul statistic # 146 al HealthCost and Utilization Project (HCUP) și al bazei de date HCUP National Inpatient Sample (NIS) 2013.
Rezultate
Rezultatele clinice publicate anterior a cincizeci și nouă de pacienți SmartVest cu bronșiectazie cu fibroză non-chistică au servit ca bază pentru această analiză. Când au fost analizate datele de rezultat, utilizarea SmartVest, comparativ cu standardul controlul îngrijirii, a fost asociat cu rezultate semnificative statistic; o scădere cu 58% a costului antibioticelor, o scădere cu 63% a costului vizitei ED și o scădere cu 60% a costului spitalizării. În total, analiza costurilor a avut ca rezultat o economie anuală de 3.045 USD pe pacient pe an de utilizare a SmartVest.
Concluzii
Eficacitatea clinică a utilizării SmartVest ca tratament pentru pacienții cu bronșiectazie cu fibroză non-chistică a fost verificată anterior printr-o reducere semnificativă n în exacerbările legate de bronșiectazii, ceea ce se traduce direct într-o reducere globală semnificativă cu 60% a utilizării asistenței medicale și a costurilor la această populație. În plus, beneficiile secundare, cum ar fi potențialul de a reduce readmiterea spitalelor și potențialul de a influența descurajarea rezistenței la antibiotice, pot avea beneficii chiar mai mari decât scăderea costurilor. oscilația peretelui, HFCWO, bronșiectazie, cost
Introducere
Bronșiectazia este o boală cronică și etiologic eterogenă. Caracteristicile comune ale bronșiectaziei sunt dificultăți de respirație, exacerbări frecvente, tuse cronică, hemoptizie și producție excesivă de spută. Boala este caracterizată de obicei prin cicluri de clearance mucociliar afectat, infecție bronșică și inflamație care rezultă în afectarea structurală a căilor respiratorii cu dilatare permanentă și anormală.1 Bronșiectaziile pot fi rezultatul unei game variate de boli respiratorii și sistemice, inclusiv fibroza chistică, sindroame ciliare diskinetice, leziuni prin inhalare / aspirație, stări de imunodeficiență primară și dobândită și o serie de afecțiuni reumatice și inflamatorii.2 Bronhiectaziile sunt observate la 7% până la 52% dintre pacienții cu astm sau boală pulmonară obstructivă cronică (BPOC) .3,4 , 37
Seitz, și colab., Au analizat un eșantion de 5% din baza de date Medicare a cererilor de ambulatoriu pentru bronșiectazii în rândul beneficiarilor cu vârsta ≥ 65 de ani, din 2000 până în 2007. furnizori. Bronșiectaziile au fost identificate prin baza de date folosind codurile de clasificare internațională a bolilor, revizuirea a noua, coduri de modificare clinică (ICD-9-CM). Populația studiată a inclus > 2 milioane de indivizi unici înscriși în Medicare Partea B timp de cel puțin o lună între 2000 și 2007. Studiul a determinat prevalența bronșiectaziei în populația generală ca fiind 1.106 de cazuri la 100.000 de persoane pe parcursul perioadei de examinare de opt ani. De asemenea, studiul a constatat că prevalența bronșiectaziei la beneficiarii Medicare a crescut cu 8,7% între 2000 și 2007, iar rata de spitalizare pentru bronșiectazii a crescut anual la o rată de 2.4% în rândul bărbaților și 3,0% în rândul femeilor.
Povara generală a bolilor pulmonare avansate este în creștere și acolo unde există date, costurile legate de morbiditatea și mortalitatea acestor boli par semnificative.2 în parte, să fie o reflectare a îmbătrânirii populației în creștere cu boli pulmonare cronice, care are o creștere disproporționată a costurilor asistenței medicale; rata spitalizării din cauza bolilor cronice pulmonare crește semnificativ peste vârsta de 50 de ani, în special la femeile în vârstă.2,7. Utilizând înregistrările externărilor din perioada 1997-2010, sa estimat costul mediu al spitalului pentru îngrijirea internată la pacienții cu exacerbarea pneumoniei a fost de 9.300,28 dolari. În 2001, s-a estimat, de asemenea, că costul medical anual pentru îngrijirea persoanelor din Statele Unite cu bronșiectazie a fost de 13.244 dolari, ceea ce este mai mare decât costul anual pentru multe alte boli cronice, cum ar fi bolile de inimă (12.000 dolari) și BPOC (11.000 de dolari) .38 Un studiu din 2005 a constatat că pacienții cu bronșiectazie cu fibroză non-chistică au avut în medie 2,0 zile suplimentare pe an în spital, au avut 6,1 întâlniri suplimentare în ambulator și încă 27,2 zile de tratament cu antibiotice comparativ cu pacienții fără boală. , costurile tratamentului pentru bronșiectazii cu fibroză non-chistică au fost de 630 milioane dolari anual.5
Pacienții cu bronșiectazii cu fibroză non-chistică pot avea dificultăți în eliminarea aerului au secreții și pot beneficia semnificativ de terapia de eliminare a căilor respiratorii.2 Scopul tratamentului pentru bronșiectazii este de a mobiliza secrețiile căilor respiratorii, astfel încât să reducă inflamația, să prevină infecțiile respiratorii, să mărească ventilația, să reducă la minimum numărul de exacerbări și să îmbunătățească calitatea vieții unui pacient. 10-12 O serie de metode terapeutice sunt utilizate în prezent pentru a elimina secrețiile căilor respiratorii la pacienții cu afecțiuni pulmonare, cu insuficiență de eliminare a mucusului respirator sau care sunt expuși riscului de a dezvolta oricare dintre aceste afecțiuni.8 Aceste metode vizează, în general, promovarea clearance-ului secreției prin reducerea vâscozitatea mucusului și utilizarea forțelor de forfecare pentru a elibera mucusul din peretele pulmonar pentru a facilita mobilizarea pentru a ușura expectorarea. Standardul de îngrijire implică terapia combinată cu agenți mucolitici și mucokinetici, bronhodilatatoare, terapie antiinflamatoare și o formă de terapie fizică / mecanică de eliminare a căilor respiratorii.2 Terapia de eliminare a căilor respiratorii joacă un rol critic, deoarece ajută la evitarea retenției mucusului încărcat de agenți patogeni, care este originea de bază a infecției recurente care determină deteriorarea pulmonară progresivă.2,13,14 Metodele de eliminare a căilor respiratorii joacă un rol critic în menținerea sănătății respiratorii pe tot parcursul vieții pacientului.
Un număr de clearance-ul căilor respiratorii sunt disponibile metode, inclusiv fizioterapia toracică, măștile de presiune finală expiratorie pozitive, dispozitivele orale-de înaltă frecvență și oscilația peretelui toracic de înaltă frecvență (HFCWO). tehnică și / sau agilitate fizică care le poate limita utilizarea.2
HFCWO este utilizat pentru eliminarea căilor respiratorii la pacienții cu o gamă largă de compromisuri ale căilor respiratorii boli și afecțiuni, inclusiv afecțiuni genetice și imunologice, afecțiuni neuromusculare și afecțiuni pulmonare obstructive, cum ar fi astmul și BPOC.15-18 Spre deosebire de alte metode, HFCWO necesită o activitate minimă de la utilizator și nu depinde de un furnizor de servicii medicale tehnica să fie eficientă.2 Studiile clinice, în principal la pacienții cu fibroză chistică, au arătat că HFCWO este sigur și eficient.2,15,19-22 HFCWO furnizează impulsuri de compresie pe peretele toracic printr-o vestă gonflabilă conectată la un generator de impulsuri de aer .2 Generatorul produce un flux alternativ de aer în și din vesta care comprimă și eliberează rapid peretele toracic într-o gamă de frecvențe și presiuni selectabile. Compresia oscilatorie transmisă peretelui toracic a fost raportată la mucus vâscos subțire, deconectează mucusul de peretele plămânului și propulsează mucusul din căile respiratorii minore ale plămânilor către căile respiratorii majore unde poate fi expectorat sau aspirat.2,23, 24 HFCWO poate duce la o îmbunătățire semnificativă a volumului pulmonar de 15 până la 57 mL și a debitului de până la 1,6 L / sec.22
Un studiu anterior de revizuire a cazurilor a evaluat rezultatele clinice ale terapiei SmartVest® Airway Clearance System pe exacerbare Utilizarea asistenței medicale și utilizarea medicamentelor legate de subiecții cu bronșiectazie cu fibroză non-chistică.25 Studiul a constatat că utilizarea SmartVest a dus la o reducere semnificativă statistic cu 60% a exacerbărilor legate de bronșiectazie, inclusiv utilizarea antibioticelor, vizitele serviciilor de urgență (DE) și spitalizările. . Studiul actual este conceput pentru a evalua impactul economic al terapiei SmartVest asupra asistenței medicale legate de bronșiectazie și a costurilor cu antibiotice.
Metode
Un SmartVest recent (Electromed, Inc., New Prague, MN , SUA) studiul clinic bazat pe rezultatele revizuirii cazului a servit ca bază pentru această analiză.25 Studiul a înregistrat toate exacerbările legate de bronșiectazie pentru a include numărul de spitalizări, vizite ED și utilizarea antibioticelor pentru o perioadă de un an înainte de utilizarea SmartVest (standard de control al îngrijirii) și, pentru comparație, pentru o perioadă de un an după începerea Utilizarea SmartVest (tratament). Studiul a inclus doar acei subiecți cu diagnostic de bronșiectazie cu fibroză non-chistică care foloseau SmartVest de cel puțin un an și ale căror fișe medicale erau disponibile timp de un an înainte de inițierea terapiei SmartVest. Pacienții au fost excluși dacă nu au respectat schema de terapie prescrisă SmartVest, nu au putut fi contactați telefonic sau au expirat. Toate datele colectate înainte de utilizarea SmartVest au fost capturate prin dosarele medicale ale pacientului.
Dosarele medicale ale pacientului au fost revizuite pentru toate exacerbările legate de bronșiectazie care au avut loc într-o perioadă de un an înainte de începerea terapiei SmartVest. Subiecții au fost contactați și intervievați telefonic pentru a colecta exacerbări legate de bronșiectazie pentru perioada de un an după începerea terapiei SmartVest. Chestionarul pentru sondajul telefonic a fost elaborat în scopul exclusiv al studiului. În timpul interviului telefonic, subiectului i s-au pus întrebări specifice cu privire la utilizarea antibioticelor legate de căile respiratorii, vizitele ED și spitalizările. De asemenea, interviul a întrebat dacă pacientul utilizează SmartVest conform schemei de prescripție a medicului.
Costurile antibioticelor au fost determinate utilizând „prețuri online la farmacii cu reducere”, totuși, costul vizitelor la birou și taxele medicului nu au fost incluse Spitalizarea și costurile ED au fost determinate utilizând estimările naționale ponderate din eșantionul național pentru pacienți internați (NIS), 2013, Agenția pentru cercetare și calitate a asistenței medicale (AHRQ), pe baza datelor colectate de către fiecare stat și furnizate către AHRQ de către state.26 Baza de date NIS include un eșantion de probabilitate stratificat de spitale din bazele de date de stat pentru pacienți care includ spitalizări de către pacienți cu Medicare, Medicaid, asigurare privată și neasigurate.27 NIS conține date de la 5 la 8 milioane de spitalizări de la aproximativ 1000 de spitale. Este desemnat să aproximeze un eșantion de 20% din spitalele non-federale, pe termen scurt, din SUA, astfel cum sunt definite de American Medical Associ acțiune. INS este extras din statele participante la proiectul de utilizare a costului și utilizării asistenței medicale. INS conține date uniforme privind șederea pacienților internați din bazele de date privind descărcarea de gestiune a spitalelor, întreținute de agențiile de stat, asociațiile de spitale și alte organizații private. Numărul total de descărcări ponderate în SUA pe baza HCUP NIS a fost de 35.597.792,28
Rezultate
Revizuirea bazelor de date HCUP și Medicare a relevat costurile asociate asistenței medicale pentru o exacerbare legată de bronșiectazie 450 USD (2012) pentru o vizită ED și 9.300 USD (2010) pentru o spitalizare cu pneumonie. Nu au fost calculate spitalizările prelungite pe bază de complicații sau comorbidități. Folosind calcule de preț online pentru farmacii cu reducere, costul unui regim standard de antibiotice pentru pneumonie a fost de 290 USD (2016). Taxele medicului pentru o vizită la birou și prescripția ulterioară nu au fost disponibile pentru calcul.
Din cei 104 pacienți cu bronșiectazie SmartVest identificați, cincizeci și nouă de pacienți au îndeplinit criteriile de includere / excludere.25 În populația studiată, numărul mediu de prescripții de antibiotice pe an a fost cu 58% mai puțin pentru SmartVest (0,6 / an) comparativ cu standardul de control al îngrijirii (1,4 / an) (vezi Tabelul 1). Utilizarea SmartVest a redus în mod semnificativ vizitele ED cu 63% (0,08 / an versuri 0,03 / an) și internările cu 60% (0,5 / an versete 0,2 / an). Costurile anuale pe pacient pentru antibiotice pentru pacienții tratați cu SmartVest au fost cu aproximativ 233 USD mai mici comparativ cu cei tratați cu standard de îngrijire (vezi Tabelul 1). Spitalizările, după un an de utilizare SmartVest, au fost, de asemenea, reduse semnificativ cu 2.790 USD pe pacient pe an. În total, rezultatele generale au relevat o economie anuală de 3.045 USD pe pacient pe an de utilizare SmartVest.
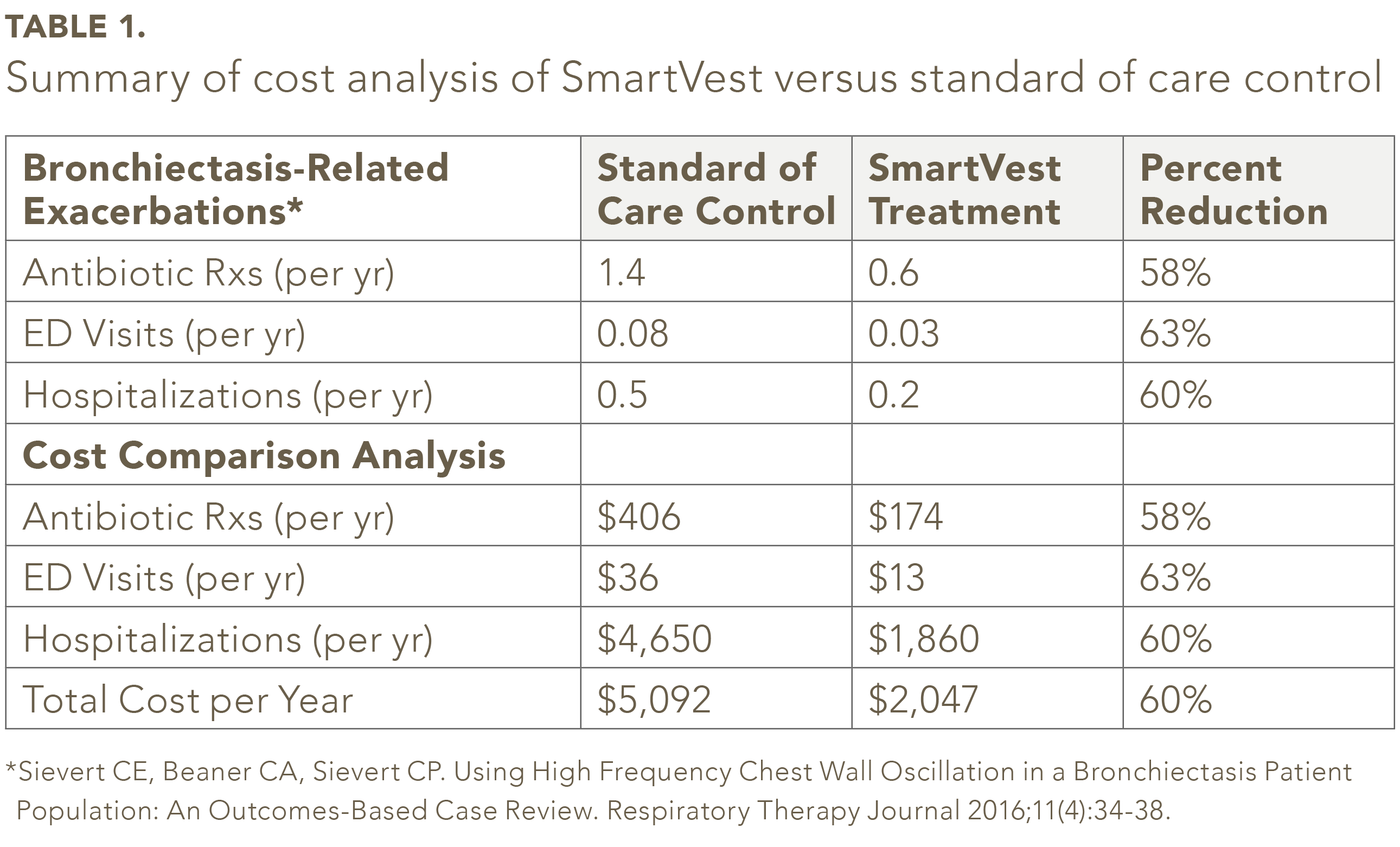
Analiza nu a făcut luați în considerare toate taxele medicului / cabinetului efectuate pentru a obține o rețetă cu antibiotice fără spitalizare. De asemenea, analiza nu a luat în considerare o vizită la birou pentru o potențială exacerbare care nu a dus la o rețetă sau la spitalizare. În plus, analiza nu a luat în considerare cheltuielile suplimentare dacă exacerbarea a fost o pneumonie cu tulpină bacteriană rezistentă la antibiotice, care se pare că poate costa mai mult de 15.000 USD pentru fiecare episod.
Discuție
Scopul analiza a fost de a evalua impactul economic al utilizării SmartVest asupra costurilor medicale asociate bronșiectaziei, comparativ cu un standard de control al îngrijirii. Din câte știm, acesta este primul studiu care evaluează costurile de asistență medicală pentru tratarea pacienților cu bronșiectazie cu fibroză non-chistică cu HFCWO.Costul global a inclus costul antibioticelor, vizitelor ED și spitalizărilor legate de exacerbări asociate cu bronșiectazii cu fibroză non-chistică. Studiul a demonstrat o reducere semnificativă a utilizării asistenței medicale și a costurilor asociate acesteia atunci când pacienții cu bronșiectazie au fost tratați cu SmartVest timp de un an. Costul total a fost redus cu 60%, ceea ce se traduce printr-o economie de 3.045 USD pe pacient pe an.
Un studiu recent care a evaluat externările la spital, readmiterile și vizitele ED pentru BPOC sau bronșiectazii la adulți în Statele Unite a constatat din 2001 până în 2012 numărul externărilor spitalicești a crescut cu 88.000,31 Studiul a constatat, de asemenea, că aproximativ 7% dintre pacienții cu BPOC sau bronșiectazii au fost readmise în decurs de 30 de zile cu BPOC sau bronșiectazii ca diagnostic principal.31 În schimb, rata externării a scăzut pentru alte boli.31 Motivul creșterii semnificative a spitalelor BPOC și bronșiectaziei și a vizitelor ED nu este clar, deoarece s-a observat o scădere semnificativă a ratelor de fumat. Cu toate acestea, poate reflecta potențialul sub diagnostic al bolii și natura pe termen lung a BPOC și bronșiectazii la o populație îmbătrânită.31
Un studiu anterior bazat pe rezultatele studiului cazului a raportat că utilizarea SmartVest a redus spitalizările prin De 1,5 ori, 25 indicând avantajul costului HFCWO pentru reducerea sarcinii de utilizare a asistenței medicale. Alte studii au evaluat, de asemenea, factori (atât de sistem, cât și de pacienți) care pot reduce readmisia la pacienții cu BPOC și sunt, cel puțin parțial, relevanți pentru pacienții cu bronșiectazie. Acești factori includ continuitatea cu îngrijirea primară a pacienților sau pneumolog, intervenția coordonatorului externărilor și amploarea sau tipul terapiei respiratorii.32-34
Reducerea numărului de exacerbări legate de bronșiectazii poate avea, de asemenea, un impact asupra calitatea vieții pacientului.35,36 Într-o populație de pacienți cu BPOC, utilizarea SmartVest a fost asociată cu o îmbunătățire semnificativă a scorului cu cinci simptome P = 0,002 (evaluarea sputei, respirației șuierătoare, tusei, respirației dificile și toleranței la efort ) .36 Tratamentul SmartVest a demonstrat, de asemenea, o îmbunătățire semnificativă a chestionarului respirator Sf. Gheorghe (SGRQ) P = 0,02, în timp ce nu s-a observat nicio îmbunătățire la pacienții tratați cu tratament convențional.36 În mod similar, studiul nostru anterior al studiului bazat pe rezultate a constatat că 68 % dintre subiecți au indicat în timpul interviului telefonic că utilizarea SmartVest și-a îmbunătățit semnificativ calitatea vieții.25
Ar trebui luate în considerare mai multe limitări ale designului studiului roșu la interpretarea rezultatelor. Mărimea pacientului din studiu a fost mică, iar datele privind spitalizările, vizitele ED și utilizarea antibioticelor după inițierea terapiei SmartVest au fost obținute în principal prin interviul cu pacienții. Studiul poate fi considerat conservator datorită faptului că nu s-au adăugat costuri pentru onorariile medicului asociate unei vizite la birou care rezultă în rețeta cu antibiotice sau, nu s-au adăugat costuri pentru o vizită la birou care nu a dus la o rețetă cu antibiotice. În plus, dependența de bazele de date HCUP, NIS și AHRQ, care depind de diagnosticele introduse în revendicări, pot fi codificate incorect sau deloc codificate, introducând astfel o eroare de măsurare în ceea ce privește variabilele bazate pe ICD-9-CM.
Reducerea costurilor de utilizare a asistenței medicale, cum ar fi utilizarea antibioticelor, vizitele ED și spitalizările sunt obiective prioritare ale directivelor recente de asistență medicală, cum ar fi Affordable Care Act (ACA). De exemplu, ACA a instituit Programul de Reducere a Spitalelor (HRRP), care a condus CMS să penalizeze spitalele prin reducerea plăților de rambursare pentru readmisia în exces a pacienților pentru aceeași afecțiune. HRRP a identificat inițial primele trei „condiții aplicabile” pentru măsurarea focalizată a readmisiei pentru a include infarctul miocardic acut, insuficiența cardiacă și pneumonia. În plus, CMS a finalizat recent extinderea condițiilor suplimentare aplicabile începând cu anul fiscal 2015 program pentru a include pacienții readmiși pentru o exacerbarea acută a BPOC. Reducerea semnificativă a utilizării asistenței medicale și a spitalizărilor pentru pacienții cu bronșiectazii non-chistice care utilizează SmartVest, așa cum s-a demonstrat în acest studiu și în alții, poate juca un rol esențial în a ajuta spitalele să reducă readmisia și, prin urmare, să nu fie penalizate.
Pentru pacienții care au infecții ale căilor respiratorii rezistente la antibiotice orale, sarcina este mult mai mare și mai gravă. Antibioticele intravenoase complică foarte mult îngrijirea, deoarece este necesară spitalizarea sau monitorizarea la domiciliu. Tratamentul pentru acești pacienți include plasarea unui cateter venos central, coordonarea dozele de medicamente care adesea trebuie administrate multi de mai multe ori pe zi, teste regulate de sânge pentru a monitoriza efectele secundare și măsurarea nivelului sanguin al antibioticului timp de multe zile, pași care devin costisitori și perturbă viața pacienților.
Organizația Mondială a Sănătății (OMS) a declarat că rezistența microbiană la antibiotice reprezintă o „amenințare globală majoră cu implicații devastatoare pentru sănătatea publică”. Rezistența antimicrobiană amenință prevenirea și tratamentul eficient al unei game tot mai mari de infecții cauzate nu numai de bacterii, ci și de viruși și ciuperci. Centrele SUA pentru Controlul și Prevenirea Bolilor (CDC) consideră rezistența antimicrobiană una dintre preocupările și prioritățile lor de top. Numai în SUA, cel puțin 2 milioane de persoane se infectează cu bacterii rezistente la antibiotice și cel puțin 23.000 de persoane mor în fiecare an ca urmare a acestor infecții.39 Ca răspuns la îngrijorarea mondială, Centrele SUA pentru Medicare & Serviciile Medicaid (CMS) au lansat recent o modificare a regulilor propuse la condițiile sale de participare, care ar necesita, printre alte modificări, spitale să implementeze programe de administrare a antibioticelor pentru a participa la programele Medicare și Medicaid. Administrarea antibioticelor include îmbunătățirea rezultatelor pacienților prin adoptarea de procese și proceduri care reduc incidența infecțiilor cu pa o atenție deosebită la pneumonie, cum ar fi îngrijirea tratamentului preventiv. Ca un beneficiu secundar al rezultatelor cost-beneficiu ale acestui studiu, o reducere semnificativă a necesității de antibiotice la pacienții cu bronșiectazii prin utilizarea SmartVest poate avea beneficii chiar mai mari decât scăderea costului. Un tratament disponibil care ar putea reduce în mod semnificativ infecțiile respiratorii și, prin urmare, necesitatea antibioticelor se potrivește bine în programele de control al infecțiilor din spital. bronșiectazii, 25 și reducerea semnificativă a costurilor cu antibiotice, ED și spitalizare, observată în acest studiu, susține beneficiul din punct de vedere al costului utilizării SmartVest și susține acoperirea asigurării SmartVest de către plătitori. Mai mult, beneficiile secundare, cum ar fi potențialul de a reduce readmiterile în spitale și potențialul de a afecta descurajarea rezistenței la antibiotice, pot avea beneficii chiar mai mari decât scăderea costurilor.
Descarcă textul studiului
Mulțumiri / h4>
Autorii vor să mulțumească doctorului Elizabeth Goodwin pentru sprijin editorial.
- Regele P. Patogenia bronșiectaziei. Paediatr Respir Rev 2011; 12 (2): 104-110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Compresie toracică de înaltă frecvență: o terapie practică pentru pacienții cu bronșiectazii. Terapia respiratorie 2008; 3 (1): 22-26.
- Patel IS, Vlahos I, Wilkinson TM și colab. Bronșiectazii, indici de exacerbare și inflamație în boala pulmonară obstructivă cronică. Am J Respir Crit Care Med 2004; 170 (4): 400-407. 10.1164 / rccm.200305-648OC
- Gono H, Fujimoto K, Kawakami S și colab. Evaluarea grosimii peretelui căilor respiratorii și a captării aerului prin HRCT în astmul asimptomatic. Eur Respir J 2003; 22 (6): 965-971.
- Weycker D, Edelsberg J, Oster G și colab. Prevalența și povara economică a bronșiectaziei. Clinical Pulmonary Medicine 2005; 12 (4): 205-209.
- Seitz AE, Olivier KN, Adjemian J, și colab. Tendințe în bronșiectazii în rândul beneficiarilor de asistență medicală în Statele Unite, 2000 – 2007. CHEST Journal 2012; 142 (2): 432-439.
- Seitz AE, Olivier KN, Steiner CA și colab. Tendințele și povara spitalizărilor asociate bronșiectaziei în Statele Unite, 1993-2006. Piept 2010; 138 (4): 944-949. 10.1378 / chest.10-0099
- Seitz AE, Olivier KN, Steiner CA și colab. Tendințele și povara spitalizărilor asociate bronșiectaziei în Statele Unite, 1993-2006. CHEST Journal 2010; 138 (4): 944-949.
- Weycker D, Edelsberg J, Oster G și colab. Prevalența și povara economică a bronșiectaziei. Medicină pulmonară clinică 2005; 12: 205-209.
- Fibroză. AoCPiC. Standarde de îngrijire și bune practici clinice pentru gestionarea fizioterapiei ff fibroză chistică 2011. Disponibil de la: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio Jun 11.pdf.
- O’Donnell AE. Bronșiectazii. Piept 2008; 134 (4): 815-823. 10.1378 / chest.08-0776
- Barker AF. Bronșiectazii. N Engl J Med 2002; 346 (18): 1383-1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Terapii de eliminare a căilor respiratorii nonfarmacologice: ghiduri de practică clinică bazate pe dovezi ACCP. Piept 2006; 129 (1 supliment): 250S-259S. 10.1378 / chest.129.1 suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Tratamentul disfuncției mucociliare. Chest 1996; 110 (4): 1048-1057.
- Arens R, Gozal D, Omlin KJ și colab. Compararea compresiei toracice de înaltă frecvență și a fizioterapiei toracice convenționale la pacienții spitalizați cu fibroză chistică. Am J Respir Crit Care Med 1994; 150 (4): 1154-1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Oscilația de înaltă frecvență a căilor respiratorii și a peretelui toracic. Respir Care 2002; 47 (7): 797-807.
- Hansen LG, Warwick WJ.Sistem de compresie toracică de înaltă frecvență pentru a ajuta la eliminarea mucusului din plămâni. Biomed Instrum Technol 1990; 24 (4): 289-294.
- Lange DJ, Lechtzin N, Davey C și colab. Oscilația peretelui toracic de înaltă frecvență în SLA: un studiu explorator randomizat, controlat. Neurologie 2006; 67 (6): 991-997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. Efectul pe termen lung al terapiei de compresie toracică de înaltă frecvență asupra complicațiilor pulmonare ale fibrozei chistice. Pediatr Pulmonol 1991; 11 (3): 265-271.
- Kluft J, Beker L, Castagnino M și colab. O comparație a tratamentelor de drenaj bronșic în fibroza chistică. Pediatr Pulmonol 1996; 22 (4): 271-274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P
- Scherer TA, Barandun J, Martinez E și colab. Efectul căilor respiratorii orale de înaltă frecvență și oscilația peretelui toracic și a terapiei fizice convenționale a toracelui asupra expectorației la pacienții cu fibroză chistică stabilă. Chest 1998; 113 (4): 1019-1027.
- Nicolini A, Cardini F, Landucci N și colab. Eficacitatea tratamentului cu oscilație de înaltă frecvență a peretelui toracic la pacienții cu bronșiectazie. BMC Pulm Med 2013; 13:21. 10.1186 / 1471-2466-13-21
- Osman LP, Roughton M, Hodson ME și colab. Studiu comparativ pe termen scurt al oscilației peretelui toracic de înaltă frecvență și tehnici europene de eliminare a căilor respiratorii la pacienții cu fibroză chistică. Torace 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Distanța asistată de înaltă frecvență a căilor respiratorii. Respir Care 2007; 52 (9): 1224-1235; discuție 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Utilizarea oscilației peretelui toracic de înaltă frecvență într-o populație de pacienți cu bronșiectazie: o analiză a cazurilor bazată pe rezultate. Jurnalul de terapie respiratorie 2016; 11 (4): 34-38.
- HCUP. Prezentare generală a eșantionului departamentului de urgență la nivel național (NEDS) 2016. Disponibil de la: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Prezentare generală a probelor de internare naționale (la nivel național). Disponibil de la: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C. Costuri pentru sejururi de spital în Statele Unite, 2010: Statistic Brief # 146. Rezumate statistice ale proiectului de cost și utilizare a asistenței medicale (HCUP). Rockville (MD): Agenția pentru cercetare și calitate în domeniul sănătății (SUA); 2006.
- Stein PD, Matta F. Costurile vizitelor la secții de urgență și spitalizări pentru hipertensiunea arterială pulmonară.
J Epidemiol Public Health Rev 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Rambursarea managementului de îngrijire tranzitorie pentru a reduce readmisia BPOC. Chest
2014; 145 (1): 149-155. 10.1378 / chest.13-0787 - Ford ES. Descărcări de spital, readmisii și vizite ED pentru BPOC sau bronșiectazie în rândul adulților din SUA: constatări din eșantionul internat la nivel intern de pacienți 2001-2012 și eșantion la nivel național al Departamentului de Urgență 2006-2011. Piept 2015; 147 (4): 989-998. 10.1378 / chest.14-2146
- Sharma G, Kuo YF, Freeman JL și colab. Vizita de urmărire ambulatorie și vizita secției de urgență de 30 de zile și readmisia la pacienții spitalizați pentru boală pulmonară obstructivă cronică. Arch Intern Med 2010; 170 (18): 1664-1670. 10.1001 / archinternmed.2010.345
- Lainscak M, Kadivec S, Kosnik M și colab. Intervenția coordonatorului externării previne spitalizarea la pacienții cu BPOC: un studiu controlat randomizat. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O, Sewell L, Morgan MD și colab. Programul scurt de reabilitare pulmonară ambulatorie reduce readmisia în urma unei spitalizări pentru o exacerbare a bolii pulmonare obstructive cronice. Respirologie 2013; 18 (7): 1063-1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. Terapia de umidificare a aerului pe termen lung este rentabilă pentru pacienții cu boală pulmonară cronică obstructivă moderată sau severă sau bronșiectazii. Value Health 2014; 17 (4): 320-327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. Un studiu pilot al impactului oscilației peretelui toracic de înaltă frecvență la pacienții cu boli pulmonare obstructive cronice cu hipersecreție de mucus. Int J Chron Obstruct Pulmon Dis 2011; 6: 693-699. 10.2147 / BPOC. S22896.
- Martınez-Garcıa MA și colab. Valoarea prognostică a bronșiectaziei la pacienții cu boală pulmonară obstructivă cronică moderată până la severă. Am J Respir Crit Care Med 2013; Vol. 187, Iss. 8, pp. 823–831.
- O’Donnell AE. Bronșiectazii. Chest 2008; 134: 815-82.
- Centers for Disease Control and Prevention – Antibiotic / Antimicrobial Resistance website https://www .cdc.gov / drugresistance /