Date despre elementele de cadmiu
Elementul chimic cadmiu este clasificat ca un metal de tranziție. A fost descoperit în 1817 de Friedrich Stromeyer.

Zona de date
| Clasificare: | Cadmiu este un metal de tranziție |
| Culoare: | alb-albăstruie |
| Greutate atomică: | 112.41 |
| Stat: | solid |
| Punct de topire: | 321,1 oC, 594,3 K |
| Punct de fierbere: | 765 oC, 1038 K |
| Electroni: | 48 |
| Protoni: | 48 |
| Neutroni în izotopul cel mai abundent: | 66 |
| Cochilii de electroni: | 2,8,18,18,2 |
| Configurare electron: | 4d10 5s2 |
| Densitate @ 20oC: | 8,65 g / cm3 |
Afișați mai multe, inclusiv: încălziri, energii, oxidare, reacții, compuși
, raze, Conductivități
| Volumul atomic: | 13,1 cm3 / mol |
| Structură: | hcp: hexagonal închis |
| Duritate: | 2.0 mohs |
| Capacitate de căldură specifică | 0,23 J g-1 K-1 |
| Căldură de fuziune | 6,192 kJ mol-1 |
| Căldura de atomizare | 112 kJ mol-1 |
| Căldura de vaporizare | 99,87 kJ mol-1 |
| Prima energie de ionizare | 867,7 kJ mol-1 |
| A doua energie de ionizare | 1631,4 kJ mol-1 |
| A treia energie de ionizare | 3616,2 kJ mol-1 |
| Afinitate electronică | – |
| Număr minim de oxidare | 0 |
| Min. nr. obișnuit de oxidare. | 0 |
| Numărul maxim de oxidare | 2 |
| Max. oxidare comună nr. | 2 |
| Electronegativitate (Pauling Scale) | 1.69 |
| Polarizabilitate volum | 7.2 Å3 |
| Reacție cu aer | ușoară, cu greutate ⇒ CdO |
| Reacție cu 15 M HNO3 | ușoară ⇒ Cd (NO3) 2, NOx |
| Reacție cu 6 M HCl | ușoară, ⇒ H2, CdCl2 |
| Reacție cu NaOH 6 M | niciunul |
| Oxid (s) | CdO, CdO2 |
| Hidrură (e) | CdH2 |
| Clorură (e) | CdCl2 |
| Raza atomică | 151 pm |
| Raza ionică (1+ ion) | – |
| Raza ionică (2+ ion) | 109 pm |
| Raza ionică (3+ ion) | – |
| Raza ionică (1- ion) | – |
| Raza ionică (2- ion) | – |
| Raza ionică (3-ion) | – |
| conductivitate termică | 96,6 W m-1 K-1 |
| Conductivitate electrică | 14,7 x 106 S m-1 |
| Punct de îngheț / topire: | 321,1 oC, 594,3 K |

O bilă mică de cadmiu metalic, cu o monedă pentru referință la dimensiune.

Friedrich Stromeyer, care a descoperit cadmiul în 1817.
Vecinătatea tabelului periodic al cadmiului
| Grup 11 |
Grupul 12 | Grupul 13 | |
| 4 | 29 Cu |
30 Zn |
31 Ga |
| 5 | 47 Ag |
48 Cd |
49 În |
| 6 | 79 Au |
80 Hg |
81 Tl |
Descoperirea cadmiului
Cadmiul a fost descoperit de chimistul german Friedrich Stromeyer în 1817 ca impuritate în oxidul de zinc. (1)
Stromeyer și-a făcut descoperirea după o cerere din partea guvernului de a inspecta farmaciile din orașul Hildesheim, Germania.
În acele vremuri, oxidul de zinc era folosit, așa cum este, pentru tratarea afecțiunilor pielii. Din anumite motive, farmaciile din Hildesheim vindeau mai degrabă carbonat de zinc decât oxidul obișnuit de zinc.
Stromeyer era conștient că încălzirea carbonatului de zinc până când arde roșu îl va transforma în oxid. A făcut asta cu probe de la farmacii. El a descoperit că carbonatul alb strălucitor s-a transformat într-un oxid care ar fi trebuit să fie alb, dar de fapt galben / portocaliu.
În mod normal, această culoare ar sugera contaminarea cu fier sau plumb, dar Stromeyer nu a putut găsi nici o urmă. din aceste elemente.
A vizitat fabrica din Salzgitter de unde farmaciile cumpăraseră carbonatul de zinc. El a întrebat de ce vând carbonat de zinc în loc de oxidul obișnuit.
Managerul i-a explicat că carbonatul lor de zinc era culoarea așteptată – alb – și a fost ușor de vândut.
Când au încercat să transforme carbonatul în oxid prin încălzire, a devenit întotdeauna galben. Deoarece oxidul de zinc ar trebui să fie alb, nu l-ar putea vinde. L-au analizat cu atenție pentru contaminarea fierului, dar nu au găsit niciunul.
Stromeyer a decis apoi că va analiza el însuși cu grijă acest oxid galben de zinc. El a descoperit că culoarea galbenă a fost cauzată de „prezența unui oxid metalic deosebit, a cărui existență nu fusese suspectată până acum”.
El a extras acest nou oxid metalic din oxidul de zinc și apoi l-a redus pentru a izola primul cadmiu metalic din lume. A comparat aspectul său cu cel al platinei și i-a măsurat densitatea la 8,75 g / cm3 – foarte aproape de ziua de azi a acceptat valoarea.
El a continuat să lucreze și a constatat că și alți compuși ai zincului conțineau noul său metal. El a analizat zincul „pur” și a constatat că noul său metal era prezent chiar și în acest lucru.
l a estimat că noul metal era prezent între 0,1% și 1% în zinc și compușii acestuia, din care a reușit să izoleze 3 grame de metal cadmiu pur.
Stromeyer a sugerat numele de cadmiu după „cadmia”, denumirea în latină a calaminei. Calamina este un nume vechi pentru un minereu de zinc.
Cadmiul a fost descoperit independent de chimistul german Karl Hermann în 1818. Hermann observase o culoare galbenă neașteptată în sulfura de zinc. Se presupunea că galbenul provine din impurități de arsen, dar Hermann și-a dat seama că de fapt se datora unui element necunoscut anterior. ment. (2)


Telurura de cadmiu este utilizată pentru a produce celule solare cu film subțire, care pot absorb mai mult de 90% din lumina vizibilă. Imagine: NREL
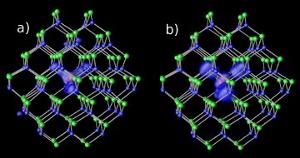
Impuritățile de magneziu din nanocristalele cadmiu-seleniu la două niveluri de decalaj diferite : (a) rezonant și (b) hibrid. Imagine: NERSC
Aspect și caracteristici
Efecte nocive:
Cadmiu și compușii săi sunt foarte toxice.
Caracteristici:
Cadmiul este un metal moale, maleabil, ductil, alb-albăstrui, care este ușor de tăiat cu un cuțit. Este un conductor electric excelent și prezintă o bună rezistență la coroziune și la atacul substanțelor chimice.
Este similar în multe privințe cu zincul prin proprietățile sale chimice.
Cadmiul se murdărește în aer și este solubil în acizi, dar nu și în alcalii.
Metalul arde în aer pentru a forma oxid de cadmiu maro (CdO).
Utilizările de cadmiu
Utilizarea majoră a cadmiului este în baterii (în special reîncărcabile nichel-cadmiu, NiCad, baterii).
Ca urmare a coeficientului său redus de frecare și a rezistenței sale ridicate la oboseală, cadmiul este utilizat în aliajele pentru rulmenți. Cadmiul este utilizat în aliajele cu topire scăzută și este o componentă a mai multor tipuri de lipire. Este, de asemenea, utilizat în galvanizare.
Compușii care conțin cadmiu sunt utilizați în fosforii de televiziune alb-negru, și în fosforii albastru și verde pentru tuburile de televiziune color. Sulfura de cadmiu este utilizată ca pigment galben, iar selenura de cadmiu este folosită ca pigment roșu, adesea numit roșu de cadmiu. producerea de celule solare. Acestea au un cost relativ scăzut și au o distanță de bandă aproape perfectă pentru recoltarea energiei solare.
Abundența și izotopii
Abundența scoarței terestre: 150 părți pe miliard în greutate, 30 părți pe miliard în alunițe
Sistem solar cu abundență: 6 părți pe miliard în greutate, 70 părți pe trilion de moli
Cost pur: 46 USD per 100g
Cost, vrac: 0,77 USD pe 100g
Sursă: Cadmiul apare cel mai adesea în cantități mici asociate cu minereuri de zinc, cum ar fi sfalerita (ZnS). Greenockitul (CdS) este singurul mineral de cadmiu cu orice consecință. Aproape tot cadmiul este obținut ca produs secundar al operațiilor de rafinare a minereului de zinc, cupru și plumb.

- Friedrich Stromeyer, Annals of Philosophy, editat de Thomas Thomson, volumul XIII, 1819, Robert Baldwin, p108
- JW Mellor, A Comprehensive Treatise in Anorganic and Theoretical Chemistry, Volumul IV, 1929, Longmans, Green and Co. Ltd., p404
Citați această pagină
Pentru conectarea online , vă rugăm să copiați și să lipiți unul dintre următoarele:
<a href="https://www.chemicool.com/elements/cadmium.html">Cadmium</a>
sau
<a href="https://www.chemicool.com/elements/cadmium.html">Cadmium Element Facts</a>
To citați această pagină într-un document academic, vă rugăm să utilizați următoarea citare conformă MLA:
"Cadmium." Chemicool Periodic Table. Chemicool.com. 16 Oct. 2012. Web. <https://www.chemicool.com/elements/cadmium.html>.