ATP-molekyl (Svenska)
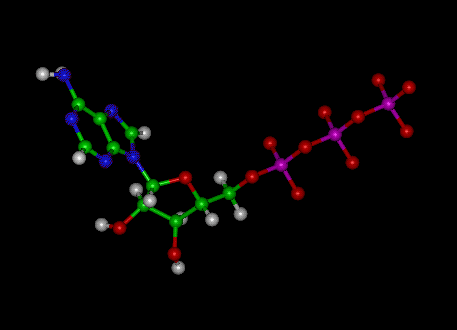
Adenosintrifosfat (ATP) -molekylen är den kända nukleotiden inom biokemi som ”molekylär valuta” för intracellulär energiöverföring; ATP kan lagra och transportera kemisk energi i celler. ATP spelar också en viktig roll i syntesen av nukleinsyror.
För 3D-struktur av denna bild med Jsmol Klicka här
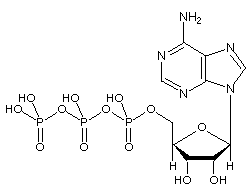
Bild: Molekylär struktur av ATP
Energi frigörs genom hydrolys av den tredje fosfatgruppen. Efter att denna tredje fosfatgrupp släppts kan det resulterande ADP (adenosindifosfat) absorbera energi och återfå gruppen och därigenom regenerera en ATP-molekyl; detta tillåter ATP att lagra energi som ett uppladdningsbart batteri.
Fosforylpositioner
Fosforylgrupperna som börjar med den på AMP kallas alfa-, beta- och gammafosfaterna.
Fysiska och kemiska egenskaper
ATP består av adenosin – sammansatt av en adeninring och ett ribosocker – och tre fosfatgrupper (trifosfat). Fosforylgrupperna, som börjar med gruppen närmast ribosen, kallas alfa (a), beta (β) och gamma (γ) fosfater. Följaktligen är den nära besläktad med adeninnukleotiden, en monomer av RNA. ATP är mycket lösligt i vatten och är ganska stabilt i lösningar mellan pH 6,8 och 7,4, men hydrolyseras snabbt vid extremt pH. Följaktligen lagras ATP bäst som ett vattenfritt salt.
ATP är en instabil molekyl i obuffert vatten, där den hydrolyserar till ADP och fosfat. Detta beror på att styrkan hos bindningarna mellan fosfatgrupperna i ATP är mindre än styrkan hos vätebindningarna (hydratiseringsbindningar), mellan dess produkter (ADP och fosfat) och vatten. Således, om ATP och ADP är i kemisk jämvikt i vatten kommer nästan hela ATP så småningom att omvandlas till ADP. Ett system som är långt ifrån jämvikt innehåller Gibbs fri energi och kan utföra arbete. Levande celler upprätthåller förhållandet ATP till ADP vid en punkt tio storleksordningar från jämvikt, med ATP-koncentrationer fem gånger högre än koncentrationen av ADP. Denna förskjutning från jämvikt innebär att hydrolysen av ATP i cellen frigör en stor mängd fri energi.
Två fosfoanhydridbindningar (de som förbinder intilliggande fosfater) i en ATP-molekyl är ansvariga för det höga energiinnehållet i denna molekyl. I samband med biokemiska reaktioner kallas dessa anhydridbindningar ofta – och ibland kontroversiellt – högenergibindningar (trots att det tar energi att bryta bindningar). Energi lagrad i ATP kan frigöras vid hydrolys av anhydridbindningarna. Den primära fosfatgruppen på ATP-molekylen som hydrolyseras när energi behövs för att driva anabola reaktioner är γ-fosfatgruppen. Ligger längst bort från ribossockret, har det en högre energi för hydrolys än antingen α- eller β-fosfatet. Bindningarna som bildas efter hydrolys – eller fosforylering av en rest med ATP – har lägre energi än ATP: s fosfanohydridbindningar. Under enzymkatalyserad hydrolys av ATP eller fosforylering med ATP kan den tillgängliga fria energin utnyttjas av ett levande system för att utföra arbete.
Alla instabila system med potentiellt reaktiva molekyler kan potentiellt fungera som ett sätt att lagra gratis energi, om cellen behöll sin koncentration långt från reaktionens jämviktspunkt. Men som det är fallet med de flesta polymera biomolekyler drivs nedbrytningen av RNA, DNA och ATP till enklare monomerer av både energi-frigörings- och entropiökningsöverväganden, i både standardkoncentrationer och även de koncentrationer som påträffas i cellen.
Standardmängden energi som frigörs från hydrolys av ATP kan beräknas utifrån förändringarna i energi under icke-naturliga (standard) förhållanden och sedan korrigeras till biologiska koncentrationer. Nettoförändringen i värmeenergi (entalpi) vid standardtemperatur och tryck för sönderdelningen av ATP till hydratiserad ADP och hydratiserat oorganiskt fosfat är -30,5 kJ / mol, med en förändring i fri energi på 3,4 kJ / mol. Energin som frigörs genom klyvning av antingen en fosfat (Pi) eller pyrofosfat (PPi) enhet från ATP vid standardtillstånd 1 M är:
ATP + H
2O → ADP + Pi ΔG ° = −30,5 kJ / mol (−7,3 kcal / mol)
ATP + H
2O → AMP + PPi ΔG ° = −45,6 kJ / mol (−10,9 kcal / mol)
Dessa värden kan vara används för att beräkna förändringen i energi under fysiologiska förhållanden och det cellulära ATP / ADP-förhållandet. Emellertid används ett mer representativt värde (som tar hänsyn till AMP) som kallas energiladdningen. Värdena som ges för Gibbs fri energi för denna reaktion är beroende av ett antal faktorer, inklusive total jonstyrka och närvaron av jordalkalimetalljoner, såsom Mg2 +
och Ca2 +
.Under typiska cellulära förhållanden är ΔG ungefär -57 kJ / mol (-14 kcal / mol).
Syntes
ATP kan produceras genom olika cellulära processer, oftast i mitokondrier av oxidativ fosforylering under katalytisk påverkan av ATP-syntas eller i fall av växter i kloroplaster genom fotosyntes.
Huvudbränslen för ATP-syntes är glukos och fettsyror. Ursprungligen bryts glukos ner till pyruvat i cytosolen. Två molekyler ATP genereras för varje molekyl glukos. De terminala stadierna av ATP-syntes utförs i mitokondrionen och kan generera upp till 34 ATP.
ATP i människokroppen
Den totala mängden ATP i människokroppen är ungefär 0,1 mol. Den energi som en vuxen använder dagligen kräver hydrolys av 200 till 300 mol ATP. Detta innebär att varje ATP-molekyl måste återvinnas 2000 till 3000 gånger under dagen. ATP kan inte lagras och därför måste dess syntes noggrant följa konsumtionen.
Andra trifosfater
Levande celler har också andra ”högenergi” nukleosidtrifosfater, såsom guanintrifosfat. Mellan dem och ATP kan energi lätt överföras med reaktioner som de som katalyseras av nukleosiddifosfokinas: Energi frigörs när hydrolys av fosfat-fosfatbindningarna utförs. Denna energi kan användas av en mängd olika enzymer, motorproteiner och transportproteiner för att utföra arbetet i cellen. Hydrolysen ger också fritt oorganiskt fosfat och adenosindifosfat, som kan brytas ned ytterligare till en annan fosfatjon och adenosinmonofosfat. ATP kan också brytas ner direkt till adenosinmonofosfat med bildandet av pyrofosfat. Denna sista reaktion har fördelen att det är en effektivt irreversibel process i vattenlösning.
Reaktion av ADP med GTP
ADP + GTP > ATP + BNP