Kostnadseffektiv analys av användning av högfrekvent bröstväggoscillation (HFCWO) hos patienter med icke-cystisk Fibros Bronchiectasis
Abstrakt
Bronchiectasis är en kronisk progressiv sjukdom som kännetecknas av irreversibel patologisk utvidgning av lungbronkier. Behandlingar för bronkiektas syftar till att mobilisera luftvägsutsöndringar, minska inflammation, förhindra luftvägsinfektioner, förbättra ventilation, minimera antalet förvärringar och förbättra en persons livskvalitet. Högfrekvent bröstväggsvängning (HFCWO) är en luftvägsavskiljningsbehandling som för närvarande används för ett antal kroniska luftvägar som komprometterar sjukdomar inklusive icke-cystisk fibros bronkiektas. Denna studie utvärderade den ekonomiska inverkan av HFCWO-behandling som levererats av SmartVest® Airway Clearance System på bronkiektasrelaterat vårdutnyttjande och kostnad.
Metoder
Resultaten av ett tidigare publicerat fall -baserad klinisk studie av författarna gav grunden för denna kostnadseffektivitetsanalys. Bronkiektasrelaterade exacerbationer inklusive antalet sjukhusvistelser, akutmottagningsbesök och frekvensen av antibiotikarecept registrerades för varje patient under ett år före SmartVest-användning (standard för vårdkontroll) och under ett års tid efter att SmartVest startat. använda sig av. Förvärringsgraden för ett år före SmartVest och ett år efter SmartVest jämfördes. Förvärringar verifierades både från patientens journaler och via telefonintervju. Antibiotikakostnader bestämdes med hjälp av ”on-line rabatt apotek prissättning” medan sjukhusvård och ED kostnader bestämdes med hjälp av Healthcare Cost and Utilization Project (HCUP) Statistical Brief # 146 och HCUP National Inpatient Sample (NIS) 2013 database.
Resultat
De tidigare publicerade kliniska resultaten från femtiofem SmartVest-patienter med icke-cystisk fibrosbronkiektas fungerade som grund för denna analys. När resultatdata analyserades använde SmartVest jämfört med standarden vårdkontroll, var associerat med statistiskt signifikanta resultat, en minskning av antibiotikakostnaderna med 58%, en minskning av kostnaden för ED-besök med 63% och en minskning av sjukhuskostnaden med 60%. Totalt sett resulterade kostnadsanalysen i en årlig besparing på 3 045 dollar per patient per år av SmartVest-användning.
Slutsatser
Den kliniska effekten av att använda SmartVest som en behandling för patienter med icke-cystisk fibrosbronkiektas verifierades tidigare med en signifikant reduktio n vid bronkiektasrelaterade förvärringar, vilket direkt leder till en signifikant minskning på 60% av vårdutnyttjandet och kostnaden i denna befolkning. Dessutom kan sekundära fördelar som potentialen att minska återintag på sjukhus och potentialen att påverka för att avskräcka antibiotikaresistens ha ännu större fördelar än att minska kostnaden.
Nyckelord
SmartVest, högfrekvent bröstkorg väggoscillation, HFCWO, bronkiektas, kostnad
Inledning
Bronkiektas är en kronisk och etiologiskt heterogen sjukdom. Vanliga kännetecken för bronkiektas är andfåddhet, frekventa förvärringar, kronisk hosta, hemoptys och överdriven sputumproduktion. Sjukdomen kännetecknas vanligtvis av cykler med nedsatt slemhinnaclearance, bronkial infektion och inflammation som resulterar i strukturell skada på luftvägarna med permanent och onormal utvidgning.1 Bronkiektas kan vara resultatet av en mängd olika andnings- och systemiska sjukdomar, inklusive cystisk fibros, dyskinetiska ciliära syndrom, inandnings- / aspirationsskador, primära och förvärvade immunbristtillstånd och ett antal reumatiska och inflammatoriska tillstånd.2 Bronkiektas observeras hos 7% till 52% av patienterna med astma eller kronisk obstruktiv lungsjukdom (KOL). , 37
Seitz, et al, analyserade ett 5% urval av databasen Medicare för öppenvårdsanspråk för bronkiektas bland förmånstagare i åldern ≥65 år från 2000 till 2007.6 Databasen innehåller information om anspråksnivå från icke-institutionell öppenvård leverantörer. Bronchiectasis identifierades av databasen med användning av International Classification of Diseases, Ninth Revision, Clinical Modification codes (ICD-9-CM) -koder. Studiepopulationen inkluderade > 2 miljoner unika individer som registrerades i Medicare del B i minst en månad från 2000 till 2007. Studien bestämde förekomsten av bronkiektas i den totala populationen till 1 106 fall per 100 000 personer under åttaårsgranskningsperioden. Studien fann också att förekomsten av bronkiektas hos Medicare-mottagare ökade med 8,7% mellan 2000 och 2007 och sjukhusvistelsen för bronkiektas ökade årligen med en hastighet på 2.4% bland män och 3,0% bland kvinnor.
Den totala bördan för avancerad lungsjukdom ökar, och där det finns data förefaller kostnaderna relaterade till sjukligheten och dödligheten hos dessa sjukdomar betydande.2 Detta kan, delvis vara en återspegling av den ökande åldrande befolkningen med kronisk lungsjukdom som har en oproportionerlig ökning av hälso- och sjukvårdskostnaderna; andelen sjukhusvistelser på grund av kronisk lungsjukdom ökar markant över 50 års ålder, och särskilt hos äldre kvinnor.2,7 Med hjälp av urladdningsregister från 1997-2010 beräknades den genomsnittliga sjukhuskostnaden för slutenvård hos patienter med Förvärring av lunginflammation var 9 300 $ 288. Det beräknades också att den årliga medicinska kostnaden för vård för personer i USA med bronkiektas var 13 244 $, vilket är högre än den årliga kostnaden för många andra kroniska sjukdomar, såsom hjärtsjukdom (12 000 $) och KOL (11 000 USD) .38 En studie från 2005 visade att patienter med icke-cystisk fibros bronkiektas i genomsnitt var 2,0 dagar per år på sjukhuset, hade 6,1 extra polikliniska möten och 27,2 fler dagar med antibiotikabehandling jämfört med patienter utan sjukdomen.9 2005 var behandlingskostnaderna för icke-cystisk fibros bronkiektas 630 miljoner dollar årligen.5
Patienter med icke-cystisk fibros bronkiektas kan ha svårt att rensa luften ay utsöndringar och kan avsevärt dra nytta av luftvägarens behandling.2 Syftet med behandling för bronkiektas är att mobilisera luftvägsutsöndringar för att minska inflammation, förhindra luftvägsinfektioner, förbättra ventilation, minimera antalet förvärringar och förbättra patientens livskvalitet. 10-12 Ett antal terapeutiska metoder används för närvarande för att rensa luftvägsutsöndringar hos patienter med lungsjukdom, nedsatt andningsslemutsläpp eller som riskerar att utveckla något av dessa tillstånd.8 Dessa metoder syftar i allmänhet till att främja utsöndringsclearance genom att minska slemviskositet och användning av skjuvkrafter för att frigöra slem från lungväggen för att underlätta mobilisering för att underlätta expectoration. Vårdstandard innefattar kombinationsbehandling med mucolytiska och mucokinetiska medel, bronkdilaterande medel, antiinflammatorisk terapi och någon form av fysisk / mekanisk luftvägsavskiljningsterapi.2 Luftvägsavskiljningsterapi spelar en avgörande roll eftersom det hjälper till att undvika kvarhållande av patogenbelastat slem som är det underliggande ursprunget till återkommande infektion som orsakar progressiv lungförsämring.2,13,14 Luftvägsavskiljningsmetoder spelar en avgörande roll för att upprätthålla andningshälsan under hela patientens livstid.
Ett antal luftvägsavstånd Metoder finns tillgängliga inklusive bröstfysioterapi, positiva ändexpiratoriska tryckmasker, orala högfrekventa apparater och högfrekventa bröstväggsvängningar (HFCWO) .2 Positiva slututandningstrycksmasker och orala högfrekventa enheter kräver aktiv ansträngning, behärskning av teknik och / eller fysisk smidighet som kan begränsa deras användning.2
HFCWO används för luftvägsavstånd hos patienter med ett brett spektrum av luftvägskompromisser ng sjukdomar och tillstånd, inklusive genetiska och immunologiska störningar, neuromuskulära sjukdomar och obstruktiva lungsjukdomar, såsom astma och KOL.15-18 Till skillnad från vissa andra metoder kräver HFCWO minimal aktivitet från användaren och är inte beroende av en vårdgivares teknik för att vara effektiv.2 Kliniska studier, främst på patienter med cystisk fibros, har visat att HFCWO är säker och effektiv.2,15,19-22 HFCWO levererar kompressionspulser till bröstväggen genom en uppblåsbar väst ansluten till en luftpulsgenerator .2 Generatorn producerar ett växlande luftflöde in i och ut ur västen som snabbt komprimerar och släpper ut bröstväggen inom ett antal valbara frekvenser och tryck. Den oscillerande kompressionen som förmedlas till bröstväggen har rapporterats tunt visköst slem, kopplar bort slem från lungans vägg och driver slem från de mindre luftvägarna i lungorna mot de större luftvägarna där det kan expektoreras eller sugas bort.2,23, 24 HFCWO kan leda till signifikant förbättring av lungvolymen på 15 till 57 ml och i flöde upp till 1,6 liter / sek. 22
En tidigare fallstudie utvärderade de kliniska resultaten av SmartVest® Airway Clearance System-terapi vid exacerbation -relaterat vårdutnyttjande och läkemedelsanvändning hos försökspersoner med icke-cystisk fibros bronkiektas.25 Studien visade att användningen av SmartVest resulterade i en statistiskt signifikant minskning med 60% av bronkiektasrelaterade exacerbationer inklusive antibiotikaanvändning, akutmottagning (ED) och sjukhusvistelser . Den aktuella studien är utformad för att bedöma den ekonomiska effekten av SmartVest-terapi på bronkiektasrelaterade sjukvårdskostnader och antibiotikakostnader.
Metoder
En nyligen genomförd SmartVest (Electromed, Inc., New Prague, MN , USA) resultatgranskning av fallbaserad klinisk studie fungerade som grund för denna analys.25 Studien registrerade alla bronkiektasrelaterade förvärringar för att inkludera antalet sjukhusvistelser, ED-besök och antibiotikaanvändning under ett år före SmartVest-användning (standard för vårdkontroll) och, för jämförelse, under ett års period efter början av SmartVest-användning (behandling). Studien inkluderade endast de personer med diagnos av icke-cystisk fibrosbronkiektas som använt SmartVest i minst ett år och vars medicinska register fanns tillgängliga i ett år innan SmartVest-behandlingen inleddes. Patienter uteslöts om de inte hade följt sin föreskrivna SmartVest-terapiregim, inte kunde kontaktas per telefon eller hade gått ut. All data som samlades in före SmartVest-användning registrerades via patientens journaler.
Patientens journaler granskades med avseende på alla bronkiektasrelaterade förvärringar som inträffade under ett års period innan SmartVest-behandlingen påbörjades. Ämnen kontaktades och intervjuades per telefon för att samla bronkiektasrelaterade exacerbationer under ettårsperioden efter att SmartVest-behandlingen påbörjats. Frågeformuläret för telefonundersökningen utvecklades för studiens exklusiva syfte. Under telefonintervjun ställdes ämnet specifika frågor angående andningsrelaterad antibiotikaanvändning, ED-besök och sjukhusvistelser. Intervjun frågade också om patienten använde SmartVest enligt läkarens receptregim.
Antibiotikakostnaderna bestämdes med hjälp av ”on-line rabatt apotekspriser”, men kostnaden för kontorsbesök och avgifter för läkare inkluderades inte. Kostnader för sjukhusvård och ED bestämdes med hjälp av de viktade nationella uppskattningarna från Healthcare Cost and Utilization Project (HCUP) National Inpatient Sample (NIS), 2013, Agency for Healthcare Research and Quality (AHRQ), baserat på data som samlats in av enskilda stater och lämnats till AHRQ från States.26 NIS-databasen innehåller ett stratifierat sannolikhetsprov av sjukhus från statliga sjukhusdatabaser som inkluderar sjukhusvistelser av patienter med Medicare, Medicaid, privat försäkring och de oförsäkrade.27 NIS innehåller data från 5 till 8 miljoner sjukhusvistelser från cirka 1000 sjukhus. Det är avsett att ungefär ett 20% -prov av amerikanska, icke-federala, kortvariga sjukhus som definierats av American Medical Associ attion. NIS hämtas från stater som deltar i Healthcare Cost and Utilization Project. NIS innehåller enhetliga data om slutenvistelse från databaser för sjukhusutskrivningar som underhålls av statliga myndigheter, sjukhusföreningar och andra privata organisationer. Totalt antal viktade utsläpp i USA baserat på HCUP NIS var 35 597 792,28
Resultat
Granskning av HCUP- och Medicare-databaser avslöjade tillhörande sjukvårdskostnader för en bronkiektasrelaterad exacerbation – att vara 450 $ (2012) för ED-besök och 9 300 $ (2010) för sjukhusvistelse med lunginflammation. Förlängda sjukhusvistelser baserade på komplikationer eller comorbiditeter beräknades inte. Med hjälp av on-line rabatterade apotekspriser, var kostnaden för en standard antibiotikabehandling för lunginflammation $ 290 (2016). Läkaravgifter för ett kontorsbesök och efterföljande recept var inte tillgängliga för beräkning.
Av de 104 identifierade SmartVest-patienterna med bronkiektik uppfyllde femtiofem patienter inkludering / uteslutningskriterierna.25 I studiepopulationen var det genomsnittliga antalet av antibiotikarecept per år var 58% mindre för SmartVest (0,6 / år) jämfört med standard för vårdkontroll (1,4 / år) (se tabell 1). SmartVest-användning minskade också signifikant ED-besök med 63% (0,08 / år vers 0,03 / år) och sjukhusvistelser med 60% (0,5 / år vers 0,2 / år). Den årliga kostnaden per patient för antibiotika för patienter som behandlades med SmartVest var cirka 233 dollar lägre än de som behandlades med standardvård (se tabell 1). Sjukhusvistelser, efter ett års användning av SmartVest, minskade också betydligt med 2 790 dollar per patient och år. Totalt visade de övergripande resultaten en årlig besparing på 3 045 dollar per patient per år av SmartVest-användning.
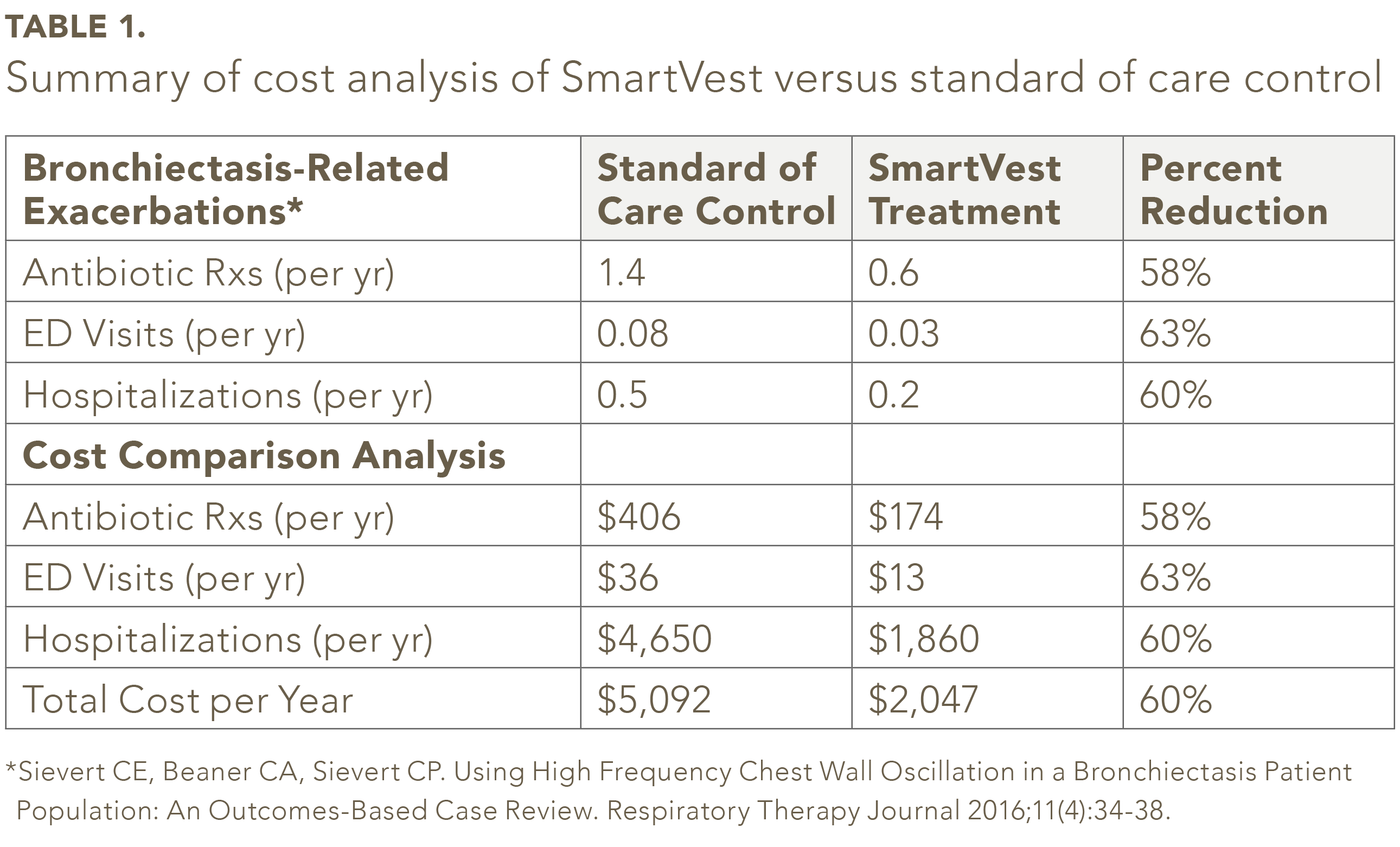
Analysen gjorde inte redovisa eventuella avgifter för läkare / kontor för att få ett antibiotikarecept utan sjukhusvistelse. Analysen redogjorde inte heller för ett kontorsbesök för en potentiell förvärring som inte ledde till recept eller sjukhusvistelse. Dessutom redogjorde inte analysen för extra kostnader om förvärringen var en antibiotikaresistent bakteriell stam lunginflammation som enligt uppgift kan kosta mer än $ 15 000 för varje avsnitt.
Diskussion
Syftet med analysen var att utvärdera den ekonomiska effekten av SmartVest-användning på bronkiektasrelaterade medicinska kostnader jämfört med en standard för vårdkontroll. Såvitt vi vet är detta den första studien för att bedöma sjukvårdskostnaderna för behandling av icke-cystisk fibros bronkiektaspatienter med HFCWO.Totalkostnaden inkluderade kostnaden för antibiotika, ED-besök och sjukhusvistelser relaterade till förvärringar associerade med icke-cystisk fibros bronkiektas. Studien visade en signifikant minskning av vårdutnyttjandet och dess därmed sammanhängande kostnad när patienter med bronkiektas behandlades med SmartVest i ett år. Den totala kostnaden minskade med 60%, vilket innebär en besparing på 3 045 dollar per patient och år.
En nyligen genomförd studie som utvärderade sjukhusutskrivningar, återintag och ED-besök för KOL eller bronkiektas hos vuxna i USA hittades från 2001 till 2012 ökade antalet utskrivningar på sjukhus med 88 000,31 Studien visade också att cirka 7% av patienterna med KOL eller bronkiektas återinlämnades inom 30 dagar med KOL eller bronkiektas som principdiagnos.31 Däremot minskade urladdningshastigheten för andra sjukdomar.31 Anledningen till den signifikanta ökningen av KOL- och bronkiektasbesök på sjukhus och ED är inte tydlig eftersom en signifikant minskning av rökningsgraden har observerats. Det kan dock återspegla potentialen under diagnosen av sjukdomen och den långsiktiga karaktären av KOL och bronkiektas i en åldrande befolkning.31
En tidigare fallstudie resultatbaserad studie rapporterade att SmartVest-användning minskade sjukhusvistelser med 1,5 gånger, 25 som indikerar kostnadsfördelarna med HFCWO för att minska bördan för vårdutnyttjandet. Andra studier har också utvärderat faktorer (både system och patient) som kan sänka återupptagande hos patienter med KOL, och är åtminstone delvis relevanta för patienter med bronkiektas. Dessa faktorer inkluderar kontinuitet med patientens primärvård eller lungläkare, urladdningskoordinatorintervention och omfattningen eller typen av andningsterapi.32-34
Minskning av antalet bronkiektasrelaterade exacerbationer kan också påverka en patientens livskvalitet.35,36 I en population av patienter med KOL var användningen av SmartVest associerad med signifikant förbättring av poängen med fem symtom P = 0,002 (betyg av sputum, väsande andning, hosta, andfåddhet och träningstolerans ) .36 SmartVest-behandling visade också en signifikant förbättring i St. George’s Respiratory Questionnaire (SGRQ) P = 0,02, medan ingen förbättring observerades hos patienter som behandlades med konventionell behandling.36 På samma sätt visade vår tidigare fallstudie resultatbaserad studie att 68 % av försökspersonerna indikerade under telefonsamtalssamtalet att användningen av SmartVest avsevärt hade förbättrat deras livskvalitet.25
Flera begränsningar för studiens design bör beaktas rött när man tolkar resultaten. Patientens storlek på studien var liten och sjukhusvistelser, ED-besök och antibiotikaanvändningsdata efter initiering av SmartVest-terapi erhölls främst genom patientintervju. Studien kan betraktas som konservativ på grund av att ingen kostnad läggs till för avgifter för läkare i samband med ett kontorsbesök vilket resulterar i ett antibiotikarecept eller ingen kostnad till för ett kontorsbesök som inte resulterar i ett antibiotikarecept. Dessutom kan beroende av HCUP-, NIS- och AHRQ-databaser, som beror på diagnoserna på fordringar, kodas felaktigt eller inte kodas alls, vilket möjligen introducerar mätfel med avseende på ICD-9-CM-baserade variabler. / p>
Att minska kostnaden för vårdutnyttjande, såsom antibiotikaanvändning, ED-besök och sjukhusinläggningar, är prioriterade mål i de senaste hälso- och sjukvårdsdirektiven, såsom Acord. Till exempel har ACA inrättat reduktionsprogrammet för sjukhusåtertagningar (HRRP), som har uppmanat CMS att straffa sjukhus genom att minska ersättningsbetalningarna för överskott av patientintag för samma tillstånd. HRRP identifierade ursprungligen de tre bästa ”tillämpliga förhållandena” för fokuserad återtagandemätning för att inkludera akut hjärtinfarkt, hjärtsvikt och lunginflammation. Dessutom slutförde CMS nyligen utvidgningen av ytterligare tillämpliga tillstånd som börjar med räkenskapsåret 2015 för att inkludera patienter som tagits in för en akut förvärring av KOL. Den signifikanta minskningen av sjukvårdsutnyttjande och sjukhusvistelser för icke-cystisk bronkiektaspatienter som använder SmartVest, vilket visas i denna studie och andra, kan spela en viktig roll för att hjälpa sjukhus att minska återintag och därmed inte straffas.
För patienter som har luftvägsinfektioner som är resistenta mot orala antibiotika är bördan mycket större och mer allvarlig. Intravenösa antibiotika komplicerar vården mycket eftersom sjukhusvistelse eller hemkontroll krävs. Behandling för dessa patienter inkluderar placering av en central venkateter, samordning av doserna av läkemedel som ofta måste ges flera flera gånger per dag, regelbundna blodprov för att övervaka biverkningar och mätning av antibiotikans blodnivåer under många dagar, steg som blir dyra och stör patienternas liv.
Världshälsoorganisationen (WHO) har förklarat att mikrobiell resistens mot antibiotika utgör ett ”stort globalt hot med förödande konsekvenser för folkhälsan.” Antimikrobiell resistens hotar effektivt förebyggande och behandling av ett ständigt ökande antal infektioner orsakade av inte bara bakterier utan även virus och svampar. De amerikanska centren för sjukdomsbekämpning och förebyggande (CDC) anser att antimikrobiell resistens är en av deras viktigaste problem och prioriteringar. Bara i USA blir minst 2 miljoner människor infekterade med bakterier som är resistenta mot antibiotika och minst 23 000 människor dör varje år som ett direkt resultat av dessa infektioner.39 Som svar på den världsomspännande oron, US Centers for Medicare & Medicaid Services (CMS) släppte nyligen en föreslagen regeländring av sina villkor för deltagande, som bland annat skulle kräva att sjukhus skulle genomföra antibiotikabehandlingsprogram för att delta i Medicare- och Medicaid-programmen. Antibiotikastyrning inkluderar förbättring av patientresultat genom antagande av processer och procedurer som minskar förekomsten av infektioner med pa särskilt uppmärksamhet på lunginflammation, såsom förebyggande behandling. Som en sekundär fördel för kostnadseffektivitetsresultaten för denna studie kan en signifikant minskning av behovet av antibiotika hos bronkiektaspatienter genom användning av SmartVest ha ännu större fördelar än att minska kostnaden. En tillgänglig behandling som avsevärt kan minska luftvägsinfektioner och därmed behovet av antibiotika passar väl inom sjukhusets infektionskontrollprogram.
Sammanfattningsvis visade den kliniska effekten av HFCWO-luftvägsclearance av SmartVest hos patienter med COPD36 och de med bronkiektas, 25 och den signifikanta minskningen av antibiotikakostnader, ED och sjukhuskostnader som observerats i denna studie stöder kostnadsnyttan av SmartVest-användning och argumenterar för försäkring av SmartVest av betalare. Dessutom kan sekundära fördelar som potentialen att minska återintag på sjukhus och potentialen att påverka för att avskräcka antibiotikaresistens ha ännu större fördelar än att minska kostnaden.
Ladda ner studieteksten
Bekräftelser
Författarna vill tacka Elizabeth Goodwin PhD för redaktionellt stöd.
- King P. Pathogenesis of bronchiectasis. Paediatr Respir Rev 2011; 12 (2): 104-110. 10.1016 / j.prrv.2010.10.011
- Braverman J, Miller H. Högfrekvent bröstkompression: en praktisk terapi för patienter med bronkiektas. Andningsterapi 2008; 3 (1): 22-26.
- Patel IS, Vlahos I, Wilkinson TM, et al. Bronkiektas, förvärringsindex och inflammation vid kronisk obstruktiv lungsjukdom. Am J Respir Crit Care Med 2004; 170 (4): 400-407. 10.1164 / rccm.200305-648OC
- Gono H, Fujimoto K, Kawakami S, et al. Utvärdering av luftväggens tjocklek och luftfångande genom HRCT vid asymptomatisk astma. Eur Respir J 2003; 22 (6): 965-971.
- Weycker D, Edelsberg J, Oster G, et al. Förekomst och ekonomisk börda vid bronkiektas. Klinisk lungmedicin 2005; 12 (4): 205-209.
- Seitz AE, Olivier KN, Adjemian J, et al. Trender inom bronkiektas bland läkarmottagare i USA, 2000 till 2007. CHEST Journal 2012; 142 (2): 432-439.
- Seitz AE, Olivier KN, Steiner CA, et al. Trender och bördor för bronkiektasassocierade sjukhusvistelser i USA, 1993-2006. Bröst 2010; 138 (4): 944-949. 10.1378 / chest.10-0099
- Seitz AE, Olivier KN, Steiner CA, et al. Trender och bördor för bronkiektasassocierade sjukhusvistelser i USA, 1993-2006. CHEST Journal 2010; 138 (4): 944-949.
- Weycker D, Edelsberg J, Oster G, et al. Förekomst och ekonomisk börda vid bronkiektas. Klinisk lungmedicin 2005; 12: 205-209.
- Fibros. AoCPiC. Vårdstandarder och god klinisk praxis för sjukgymnastikhantering för cystisk fibros 2011. Tillgänglig från: https://www. cysticfibrosis.org.uk/media/82076/CD Standards of Care Physio 11. juni. pdf.
- O’Donnell AE. Bronkiektas. Bröstet 2008; 134 (4): 815-823. 10.1378 / chest.08-0776
- Barker AF. Bronkiektas. N Engl J Med 2002; 346 (18): 1383-1393. 10.1056 / NEJMra012519
- McCool FD, Rosen MJ. Icke-farmakologiska behandlingar för luftvägsavslutning: ACCP evidensbaserade kliniska riktlinjer. Bröst 2006; 129 (1 Suppl): 250S-259S. 10.1378 / chest.129.1 suppl.250S
- Salathe M, O’Riordan TG, Wanner A. Behandling av mucociliär dysfunktion. Bröst 1996; 110 (4): 1048-1057.
- Arens R, Gozal D, Omlin KJ, et al. Jämförelse av högfrekvent bröstkompression och konventionell bröstfysioterapi hos sjukhuspatienter med cystisk fibros. Am J Respir Crit Care Med 1994; 150 (4): 1154-1157. 10.1164 / ajrccm.150.4.7921452
- Fink JB, Mahlmeister MJ. Högfrekvent svängning av luftvägarna och bröstväggen. Respir Care 2002; 47 (7): 797-807.
- Hansen LG, Warwick WJ.Högfrekvent bröstkompressionssystem för att underlätta slemhinnan från lungan. Biomed Instrum Technol 1990; 24 (4): 289-294.
- Lange DJ, Lechtzin N, Davey C, et al. Högfrekvent bröstväggsvängning i ALS: en explorativ randomiserad, kontrollerad studie. Neurologi 2006; 67 (6): 991-997. 10.1212 / 01. wnl.0000237439.78935.46
- Warwick WJ, Hansen LG. Den långsiktiga effekten av högfrekvent bröstkompressionsterapi på lungkomplikationer av cystisk fibros. Pediatr Pulmonol 1991; 11 (3): 265-271.
- Kluft J, Beker L, Castagnino M, et al. En jämförelse av bronkiala dräneringsbehandlingar vid cystisk fibros. Pediatr Pulmonol 1996; 22 (4): 271-274. 10.1002 / (SICI) 1099-0496 (199610) 22: 4 < 271 :: AID-PPUL7 > 3.0.CO; 2- P
- Scherer TA, Barandun J, Martinez E, et al. Effekt av högfrekvent oral luftvägs- och bröstväggsvängning och konventionell sjukgymnastik på bröstkorg hos patienter med stabil cystisk fibros. Bröstet 1998; 113 (4): 1019-1027.
- Nicolini A, Cardini F, Landucci N, et al. Effektivitet av behandling med högfrekvent svängning i bröstväggen hos patienter med bronkiektas. BMC Pulm Med 2013; 13: 21. 10.1186 / 1471-2466-13-21
- Osman LP, Roughton M, Hodson ME, et al. Kortvarig jämförande studie av högfrekvent oscillation av bröstväggen och europeisk luftvägsteknik hos patienter med cystisk fibros. Thorax 2010; 65 (3): 196-200. 10.1136 /
thx.2008.111492 - Chatburn RL. Högfrekvensassisterad luftvägsavstånd. Respir Care 2007; 52 (9): 1224-1235; diskussion 1235-1227.
- Sievert CE, Beaner CA, Sievert CP. Använda högfrekventa bröstväggoscillationer i en bronkiektaspatientpopulation: En resultatbaserad fallgranskning. Respiratory Therapy Journal 2016; 11 (4): 34-38.
- HCUP. Översikt över det riksomfattande räddningsavdelningsprovet (NEDS) 2016. Tillgängligt från: https://www .hcup-us.ahrq.gov / nedsoverview.jsp.
- Översikt över de nationella (rikstäckande) dagproverna. Tillgänglig från: https://www .hcup-us.ahrq.gov / nisoverview.jsp.
- Pfuntner A, Wier LM, Steiner C. Kostnader för sjukhusvistelser i USA, 2010: Statistisk sammanfattning # 146. Projekt (HCUP) för hälso- och sjukvårdskostnader och -utnyttjande. Rockville (MD): Agency for Healthcare Research and Quality (US); 2006.
- Stein PD, Matta F. Kostnader för akutavdelningsbesök och sjukhusvistelser för pulmonell arteriell hypertoni.
J Epidemiol Public Health Rev 2016; 1 (3). doi http://dx.doi. org / 10.16966 / 2471-8211.120 - Kangovi S, Grande D. Ersättning för övergångsvårdshantering för att minska KOL-återtagande. Bröstet 2014, 145 (1): 149-155. 10.1378 / chest.13-0787
- Ford ES. Sjukhusutsläpp, återintag och ED-besök för KOL eller bronkiektasi bland amerikanska vuxna: resultat från det rikstäckande slutprovet 2001-2012 och Nationwide Emergency Department Sample 2006-2011. Bröst 2015; 147 (4): 989-998. 10.1378 / chest.14-2146
- Sharma G, Kuo YF, Freeman JL, et al. Polikliniskt uppföljningsbesök och 30-dagars akutavdelningsbesök och återtagande hos patienter på sjukhus för kronisk obstruktiv lungsjukdom. Arch Intern Med 2010; 170 (18): 1664-1670. 10.1001 / archinternmed.2010.345
- Lainscak M, Kadivec S, Kosnik M, et al. Utsläppskoordinatorintervention förhindrar sjukhusvistelser hos patienter med KOL: en randomiserad kontrollerad studie. J Am Med Dir Assoc 2013; 14 (6): 450 e451-456. 10.1016 / j.jamda.2013.03.003
- Revitt O, Sewell L, Morgan MD, et al. Kort polikliniskt rehabiliteringsprogram minskar återintag efter sjukhusvistelse för en förvärring av kronisk obstruktiv lungsjukdom. Respirologi 2013; 18 (7): 1063-1068. 10.1111 / resp.12141
- Milne RJ, Hockey H, Rea H. Långvarig luftfuktningsterapi är kostnadseffektiv för patienter med måttlig eller svår kronisk obstruktiv lungsjukdom eller bronkiektas. Värdehälsa 2014; 17 (4): 320-327. 10.1016 / j.jval.2014.01.007
- Chakravorty I, Chahal K, Austin G. En pilotstudie av effekten av högfrekvent bröstväggsvängning hos kronisk obstruktiv lungsjukdomspatienter med slemhypersekretion. Int J Chron Obstruct Pulmon Dis 2011; 6: 693-699. 10.2147 / KOL. S22896.
- Martınez-Garcıa MA, et al. Prognostiskt värde av bronkiektas hos patienter med måttlig till svår kronisk obstruktiv lungsjukdom. Am J Respir Crit Care Med 2013; Vol 187, utg. 8, s 823–831.
- O’Donnell AE. Bronkiektas. Bröst 2008; 134: 815–82.
- Centers for Disease Control and Prevention – Antibiotic / Antimicrobial Resistance website https://www .cdc.gov / drugresistance /